Десмопластическая мелкокруглоклеточная опухоль брюшной полости прогноз жизни
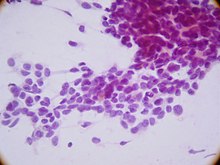
Гистологически десмопластическая мелкоклеточная опухоль детей состоит из гнезд и тяжей мелких округлых клеток, окруженных хорошо развитой десмопластической стромой. Местами клетки могут формировать розеткоподобные структуры.
Опухолевые клетки десмопластической мелкоклеточной опухоли детей экспрессируют различные антигены, включая цитокератины, нейронспецифическую энолазу и десмин.
Дифференциальный диагноз десмопластической мелкоклеточной опухоли детей необходимо проводить с альвеолярной рабдомиосаркомой, саркомой Юинга, нейробластомой, злокачественной лимфомой. Особенно сложно отличить опухоль Аскина от внескелетной саркомы Юинга, так как они имеют сходные иммуногистохимические характеристики. Некоторые авторы считают, что обе эти опухоли относятся к одному пограничному типу новообразований со следами нейроэндокринной функции (периферические примитивные нейроэктодермальные опухоли
При ранней диагностике десмопластической мелкоклеточной опухоли детей в ряде случаев удается провести радикальное хирургическое и комбинированное лечение. В остальных случаях прогноз неблагоприятный. Пять лет живут 15% больных.
Светлоклеточная саркома
Светлоклеточная саркома как самостоятельная нозологическая единица впервые была выделена из группы синовиом F. Enzinger в 1965 г. на основании изучения 21 наблюдения и названа им светлоклеточнои саркомой сухожилии и апоневрозов. В настоящее время доказано, что клетки опухоли продуцируют меланин, в связи с чем она обозначается также термином «меланома мягких тканей».
Светлоклеточные саркомы возникают в зоне сухожилий и апоневрозов преимущественно дистальных отделов конечностей, в основном у лиц молодого возраста. Средний возраст больных к моменту операции составляет 23-27 лет. Лица обоего пола поражаются одинакого часто. F. Enzinger сообщил, что у 5 из 21 больного со светлоклеточнои саркомой в анамнезе имелись указания на травму, хотя другие исследователи не придают травме какого-либо значения.
Макроскопически светлоклеточная саркома представляет собой округлой формы четко очерченное образование плотноватой или мягкоэластической консистенции в толще сухожилия или апоневроза. Диаметр узла варьирует от от 1 до 12 см, но чаще к моменту операции опухоль имеет небольшие размеры. Изъязвление кожи или врастание в кости для светлоклеточной саркомы не характерно.
При гистологическом исследовании светлоклеточная саркома состоит из светлых округлоовальных, реже веретенообразных клеток с округлыми ядрами и выступающими ядрышками. Характерным признаком является наличие многоядерных клеток. Клетки расположены компактно и собраны в пучки и ячейки, окруженные соединительнотканными прослойками. При иммуногистохимическом исследовании опухолевые клетки экспрессируют протеин S-100 и меланин. Реакция на цитокератин отрицательная.
Микроскопически светлоклеточная саркома следует дифференцировать с синовиальной саркомой, иногда с фибросаркомой. В дифференциальном диагнозе ведущая роль принадлежит иммуно-гистохимическому исследованию.
Светлоклеточная саркома характеризуются медленным ростом и сравнительно поздним метастазированием. От момента обнаружения опухоли до первого обращения к врачу проходит от 3 мес до 19 лет, в среднем 3 года.
Лечение светлоклеточной саркомы заключается в хирургическом удалении новообразования в пределах здоровых тканей. Однако в связи с тем, что опухоль имеет четкие границы и небольшие размеры, хирурги часто ограничиваются вылущиванием опухолевого узла. Это, как правило, приводит к рецидивам, нередко многократным, причем опасность метастазирования с каждым рецидивом возрастает, даже если производится радикальное удаление рецидивной опухоли.
СОДЕРЖАНИЕ
Признаки и симптомы
Есть несколько ранних признаков того, что у пациента есть DSRCT. Пациенты часто молоды и здоровы, поскольку опухоли беспрепятственно растут и распространяются в брюшной полости. Это редкие опухоли, и врачи часто неправильно диагностируют симптомы. Образования в брюшной полости могут вырасти до огромных размеров, прежде чем их заметит пациент. Опухоли можно почувствовать как твердые круглые образования при пальпации живота.
Другие зарегистрированные симптомы включают неизвестные опухоли, заболевания щитовидной железы, гормональные нарушения, свертывание крови, проблемы с почками и урологией, образования яичек, груди, матки, влагалища и яичников.
Генетика
Факторов риска, специфичных для данного заболевания, нет. Опухоль, по-видимому, возникает из примитивных клеток детства и считается детским раком.
Патология
По данным иммуногистохимии, эти клетки обладают трилинейной коэкспрессией, включая эпителиальный маркер цитокератин, мезенхимальные маркеры десмин и виментин и нейрональный маркер нейрон-специфической энолазы. Т.о., хотя первоначально предполагалось, что оно имеет мезотелиальное происхождение из-за сайтов презентации, теперь предполагается, что он возникает из клетки-предшественника с мультифенотипической дифференцировкой.
Диагностика
Дифференциальная диагностика
Прогноз
Прогноз для DSRCT остается плохим. Прогноз зависит от стадии рака. Поскольку болезнь может быть неправильно диагностирована или оставаться невыявленной, опухоли часто разрастаются в брюшной полости и метастазируют или распространяются на другие части тела.
Орган или место происхождения неизвестны. DSRCT может метастазировать через лимфатические узлы или кровоток. Места метастазирования включают селезенку, диафрагму, печень, толстую и тонкую кишку, легкие, центральную нервную систему, кости, матку, мочевой пузырь, гениталии, брюшную полость и мозг.
Мультимодальный подход, состоящий из высокодозной химиотерапии, агрессивной хирургической резекции, лучевой терапии и спасения стволовых клеток, улучшает выживаемость некоторых пациентов. Отчеты показали, что пациенты сначала реагируют на химиотерапию и лечение первой линии, но рецидивы являются обычным явлением.
Некоторым пациентам, находящимся в стадии ремиссии или с неоперабельной опухолью, по-видимому, помогает долгосрочная химиотерапия в низких дозах, что превращает DSRCT в хроническое заболевание.
Исследовать
В настоящее время Stehlin Foundation предлагает пациентам DSRCT возможность бесплатно отправлять образцы своих опухолей для тестирования. Ученые-исследователи выращивают образцы на голых мышах и тестируют различные химические вещества, чтобы найти наиболее эффективные против опухоли человека.
В 2002 году Нишио и др. Создали новую линию опухолевых клеток человека, полученную из плеврального выпота пациента с типичным внутрибрюшным DSRCT, названным JN-DSRCT-1, который теперь можно использовать в исследованиях.
В 2018 году Детская исследовательская больница Сент-Джуда предоставила ресурсы из Сети по изучению солидных опухолей у детей, которая по запросу предоставляет доступ к ортотопическим ксенотрансплантатам, полученным от пациентов.
Альтернативные названия
Это заболевание также известно как: десмопластическая маленькая круглая голубоклеточная опухоль; внутрибрюшная десмопластическая мелкая круглая синеклеточная опухоль; десмопластическая мелкоклеточная опухоль; десмопластический рак; десмопластическая саркома; DSRCT.
Стадии рака ободочной кишки
Ободочная кишка, состоящая из четырех отделов: восходящей, поперечной, нисходящей и сигмовидной кишки, занимает около 4/5 от длины толстой кишки. В любом из этих отделов может развиваться злокачественная опухоль.
Рак ободочной кишки обычно диагностируется в возрасте 50-75 лет, одинаково часто возникает как у мужчин, так и женщин. В половине случаев опухоль развивается в сигмовидной ободочной кишке, около 10-12% от всех злокачественных опухолей ободочной кишки приходится на восходящую часть, в 2% случаев злокачественное образование поражает сразу несколько отделов.
Задать вопросы и записаться на консультацию можно
по телефону: 222-10-87
или заполните форму ниже
Спасибо, ваш вопрос успешно отправлен, скоро мы с вами свяжемся!
Классификация
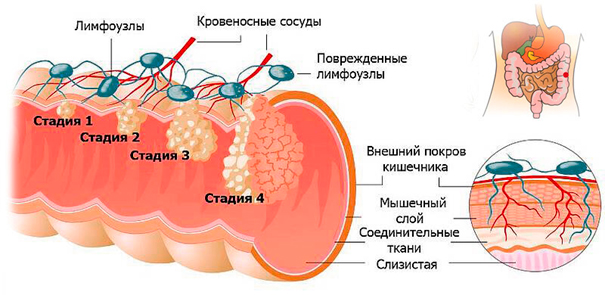
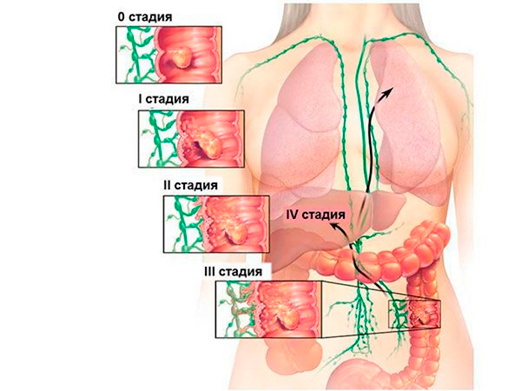
В зависимости от размеров первичной опухоли, степени ее прорастания, распространения на другие структуры организма, различают несколько стадий рака ободочной кишки. Установленная при первичном обследовании, стадия в дальнейшем не изменяется, даже если опухоль уменьшается или увеличивается. В течении рака ободочной кишки различают 4 стадии.
| Стадия | Характеристика опухоли |
|---|---|
| I | опухоль размером не более 1,5 см, локализована в пределах слизистого слоя |
| II | II A — размер опухоли превышает 1,5 см, раковые клетки распространяются на субсерозный слой; II B — клетки опухоли проникают в соседние структуры; III C — опухоль не более 1,5 см, но раковые клетки поражают близлежащие лимфоузлы; |
| III | III А — опухоль распространяется более, чем на половину окружности кишки, выходит за пределы кишечной стенки; II В — опухоль может быть любого размера, имеются множественные метастазы; |
| IV | процесс распространяется на отдаленные органы, независимо от размера первичной опухоли и степени прорастания кишечной стенки. |
Стадирование необходимо для выбора тактики лечения и составления прогноза. Для определения стадии проводится обследование, куда входят различные методы диагностики, позволяющие оценить локализацию патологического очага и степень распространения злокачественных клеток по организму. В нашей клинике пациентам доступны все современные и эффективные методы обследования: колоноскопия, томография, ультрасонография, различные исследования крови, в том числе на онкомаркеры и др.
Основные симптомы
На начальном этапе рака ободочной кишки какие-либо симптомы отсутствуют. Однако с ростом опухоли появляются различные признаки. На что стоит обратить внимание, чтобы распознать заболевание своевременно?
Стоит учитывать, что не бывает одинаковых пациентов с идентичными симптомами, появление признаков при раке ободочной кишки зависит от локализации опухоли. Например, болевой синдром чаще появляется при расположении опухоли в правых отделах кишечника. Отрыжка, дискомфорт в животе чаще беспокоит пациентов при опухоли поперечной ободочной кишки. Запоры, диарея, метеоризм, как правило, появляются в первую очередь при злокачественном образовании в левых отделах кишки. Сигмовидная кишка чаще дает о себе знать появлением слизи и крови в испражнениях. Поэтому при любом недомогании лучше обратиться к специалисту.
Однако существуют симптомы, которые появляются независимо от локализации опухоли. Необъяснимая слабость, потеря аппетита, резкое снижение веса, повышение температуры, которую сложно снижать — эти симптомы связаны с интоксикацией организма, что происходит при запущенной стадии рака любой локализации.
Осложнения
При отсутствии лечения существует риск развития осложнений. Опухоль, достигшая больших размеров, может перекрывать просвет кишки, становясь причиной кишечной непроходимости. В этом случае пациент нуждается в немедленной госпитализации. Помимо ухудшения состояния, существует риск некроза и развития перитонита, что представляет угрозу здоровью пациента.
Непрекращающееся кровотечение может стать причиной анемии, что также способно ухудшить состояние больного. При распространении метастазов в печень возможно нарушении оттока желчи и развитие желтухи. Одним из признаков тяжелой стадии рака также является скопление жидкости в брюшной полости — асцит. Подобные осложнения ухудшают прогноз при раке ободочной кишки.
Лечение
Основным методом лечения рака ободочной кишки является операция, цель которой — удаление опухоли. В ходе оперативного вмешательства вместе с опухолью удаляется часть приводящей и отводящей кишки, регионарные лимфатические узлы и окружающая клетчатка. Методика подбирается в зависимости от локализации опухоли. Существуют следующие виды оперативных вмешательств:
В том случае, если оперативное лечение противопоказано или не может быть проведено, проводится паллиативная операция, целью которой является устранение симптомов заболевания и облегчение состояния больного.
Как проводится операция
Операция выполняется в несколько этапов.
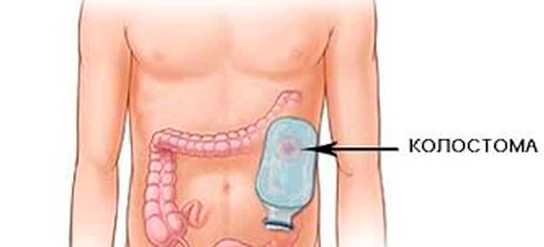
Постоянная колостома накладывается, если опухоль является неоперабельной. В таком случае проходимость кишки восстанавливается с использованием стента. Такая операция относится к паллиативным.
Мой подход к лечению пациентов с раком ободочной кишки
Я подбираю тактику лечения, учитывая результаты обследования, возраст пациента и наличие сопутствующих заболеваний. Если это возможно, я всегда отдаю предпочтение органосохраняющему и малоинвазивному лечению. При опухоли на ранней стадии может быть проведена резекция, при этом дистальный и проксимальный края резекции находятся на достаточном расстоянии от очага патологии, чтобы при микроскопическом исследовании отсутствовали опухолевые клетки; таким образом достигается радикальность операции.
Для диссекции на протяжении многих лет я использую технологию мезоколонэктомии по собственной оригинальной методике. Использование современных ультразвуковых ножниц и аппарата электротермического лигирования тканей «LigaSure» (США) позволяет провести быстро и бескровно мобилизацию кишки в правильном слое, без необходимости применения хирургических клипс и нитей.
При мобилизации правых отделов кишки для более безопасной диссекции тканей (вблизи печеночного изгиба, между фасцией Тольди и Герота) я использую оригинальный комбинированный латерально-медиальный доступ. Этот прием дает возможность безопасно выделить мочеточник и двенадцатиперстную кишку, после чего лигировать крупные сосуды, проходящие на этом участке кишки.
В большинстве случаев на этапе реконструкции я формирую анастомоз, что позволяет сохранить качество жизни пациента на прежнем уровне. При создании межкишечного соустья я использую сшивающие аппараты последнего поколения, их применение позволяет снизить количество таких осложнений после операции, как несостоятельность швов анастомоза или стриктура.
Удаление кишки, клетчатки, лимфоузлов проводится единым блоком. При этом удаляемые ткани предварительно помещаются в специальный пластиковый контейнер, что предупреждает попадание клеток опухоли на здоровые ткани, в противном случае высок риск рецидива. Весь биологический материал, удаленный в ходе операции, отправляется на гистологическое обследование — для верификации диагноза.
При проведении операции важным этапом является профилактика тромбоза и тромбоэмболии, для этого используется компрессионный трикотаж и управляемая интраоперационная прерывистая пневматическая компрессия SCD Response (Tyco Healthcare/Kendall).
Преимущества лапароскопии
В большинстве случаев я провожу операцию методом лапароскопии: все действия выполняются через несколько небольших проколов на передней брюшной стенке. Современное эндоскопическое оборудование, используемое в ходе операции, оснащено минивидеокамерой, что позволяет выполнять все действия точно и максимально бережно. Среди преимуществ лапароскопии также можно выделить:
Короткий период реабилитации позволяет пациентам в ближайшее время после операции приступить к химиотерапии, что важно для предотвращения рецидива. Кроме того, ранняя активизация пациента после лапароскопии рекомендована в целях предупреждения тромбоэмболии.
Прогноз
Продолжительность жизни больных после операции зависит от ряда факторов, основным из которых является своевременное начало лечения. Например, при опухоли 1-2 стадии выживаемость в течение первых пяти лет после лечения превышает 90%. Прогноз при раке ободочной кишки 3 стадии составляет около 30%. Ухудшает выживаемость наличие метастазирования в отдаленные органы, для пациентов с 4 стадией рака ободочной кишки прогноз неблагоприятный, показатель составляет не более 10%.
Впрочем, эти цифры весьма приблизительны. На эффективность лечения влияет тип опухоли, ее степень дифференцировки, а также наличие сопутствующих заболеваний. Кроме того, во многом излечение зависит от адекватности терапии. Существующие сегодня методы лечения, как хирургического, так и химиотерапевтического, позволяют добиться положительных результатов даже в тех случаях, которые еще недавно считались безнадежными. Но для этого обращаться за медицинской помощью следует в клинику, где есть современное оборудование и опытный персонал.
Лечением онкологических пациентов я занимаюсь на протяжении нескольких десятков лет. Я владею четырьмя узкими специализациями, одной из которых является колопроктология. Мною лично проведено более 300 хирургических вмешательств при заболеваниях ободочной кишки. Результаты обобщены в монографии «Малоинвазивная хирургия толстой кишки». Я также регулярно провожу семинары и мастер-классы, посвященные хирургическому лечению заболеваний кишечника, которые посещают специалисты клиник и центров, курсанты постдипломного образования.
Перитонеальный канцероматоз
Перитонеальный канцероматоз
Вам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Национальный центр лечения больных канцероматозом
МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Руководитель Центра к.м.н. Владимир Михайлович Хомяков – 8 495 150 11 22
Введение
Причины возникновения перитонеального канцероматоза
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматоза
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы перитонеального канцероматоза
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза
Перитонельный канцероматоз имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматоза
Длительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению. Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Гипертермическая интраоперационная внутрибрюшная (внутриплевральная) химиотерапия (HITEC).
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)
Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.