Клостридии вызывают острые кишечные инфекции.
Бактерии рода Клостридий вырабатывают наиболее сильные из известных ядов – ботулотоксин, тетаноспазмин и другие.
Клостридии – бактерии в составе постоянной собсвтенной микрофлоры кишечника. Растут строго без доступа воздуха и их очень трудно идентифицировать.
В организме человека клостридии являются стимуляторами Т-регуляторных клеток, которые снижают аллергическую настроенность организма. Один из клостридиальных метаболитов – бутират –защищает нас через интерлейкин 10. к
Кроме того, клостридии учавствуют в обмене липидов, в обмене желчных кислот и их частичном выведении из организма, подавляют рост и развитие в ЖКТ болезнетворных бактерий, расщепляют до молекулярного состояния белки.
В кишечнике новорожденных детей клостридии появляются к 6-7 дню жизни.
У детей на грудном вскармливании уровень клостридий держится в норме.
У детей при раннем введении смешанного или искусственного вскармливании клостридий превышает норму.
Анализ на дисбактериоз
Количество клостридий у взрослых:
Повышенное содержание клостридий часто наблюдается у людей старшего возраста на фоне физиологического снижения бифидобактерий.
Также повышенное содержание мясных продуктов в диете может спровоцировать рост клостридий с превышением естественной нормы.
При дисбактериозах надо регулировать эубактерии, клостридии, бифидо- и лактобактерии.
Лечшими препаратами для коррекции микрофлоры в сторону нормы являются жидкие синбиотики бифидум баг и трилакт. В них запредельное количество живых бактерий плюс жидкая среда в качестве пребиотика.
Живые культуры бифидо- и лактобактерий вместе с частью культуральной среды работают как биокатализаторы, стимулирующие восстановление кишечного гомеостаза в сторону нормы.
Людям старшего возраста необходимо 2 раза в год проводить профилактические курсы бифидум баг+трилакт для восстановления бифидобактерий, латофлоры, клостридий и др. А также регулярно употреблять в пищу кисломолочные продукты.
Трилакт и Бифидум БАГ – это безопасная микробиологическая профилактика и терапия дисбиотических нарушений ЖКТ.
Clostridium (клостридии)
Клостридии (лат. Clostridium) — род грамположительных спороносных бактерий. Клостридии входят в состав нормальной микрофлоры человека. Однако некоторые виды клостридий могут быть причиной заболеваний. Название «клостридии» происходит от греческого κλοςτεδ (веретено), так как при спорообразовании клостридии раздуваются в центре и приобретают форму веретена.
Клостридии — нормальная микрофлора человека
Клостридии — возбудители заболеваний
Большинство клостридий не патогенны, но некоторые виды клостридий могут быть причиной различных болезней человека, часть которых протекает тяжело и может приводить к летальному исходу. В частности, клостридии вида Clostridium botulinum могут быть причиной ботулизма, Clostridium tetani — столбняка, Clostridium perfringens, Clostridium novyi, Clostridium oedematiens и Clostridium septicum — газовой гангрены.

Clostridium perfringens типа А могут вызывать антибиотикоассоциированную диарею или псевдомембранозный колит. Clostridium perfringens типа F может быть причиной некротического энтерита.

Clostridium tetani являются возбудителем столбняка — острого инфекционного заболевания человека и животных, характеризующегося поражением нервной системы и проявляющееся тоническим напряжением скелетной мускулатуры и генерализованными судорогами.
Клостридии могут вызывать заболевания мочеполовых органов человека, в частности, острый простатит.
Приказом Минздравсоцразвития России №1664н от 27 декабря 2011 г. «Об утверждении номенклатуры медицинских услуг» медицинские услуги «A26.02.002 Бактериологическое исследование раневого отделяемого на возбудителей газовой гангрены (Clostridium spp.)» и «A26.19.007 Бактериологическое исследование кала на клостридии (Clostridium spp.)» включены в номенклатуру медицинских услуг, раздел 26.
Антибиотики, активные в отношении клостридий
Антибактериальные средства (из имеющих описание в данном справочнике), активные в отношении клостридий: метронидазол, тинидазол, рифаксимин, тетрациклин, доксициклин, линкомицин.
Виды клостридий, устойчивые к клиндамицину: Clostridium sporogenes и Clostridium tertium.
Клостридии в систематике бактерий
По современной классификации род клостридии входит в семейство Clostridiaceae, порядок Clostridiales, класс Clostridia, тип Firmicutes, Terrabacteria group, царство Бактерии.
К роду клостридии относится более 100 видов: С. aceticum, C. acetireducens, C. acetobutylicum, C. acidisoli, C. aciditolerans, C. aestuarii, C. akagii, C. alcalibutyricum, C. alcaliphilum, C. algidicarnis, C. algifaecis, C. algoriphilum, C. amazonense, C. aminobutyricum, C. aminovorans, C. amylolyticum, C. arbusti, C. argentinense, C. aurantibutyricum, C. autoethanogenum, C. baratii, C. beijerinckii, C. bogorii, C. boliviensis, C. bornimense, C. botulinum, C. bovipellis, C. bowmanii, C. butyricum, C. cadaveris, C. caliptrosporum, C. caminithermale, C. carboxidivorans, C. carnis, C. cavendishii, C. celatum, C. cellulovorans, C. chartatabidum, C. chauvoei, C. chromiireducens, C. cochlearium, C. colicanis, C. collagenovorans, C. corinoforum, C. coskatii, C. crotonatovorans, C. cylindrosporum, C. diolis, C. disporicum, C. drakei, C. elmenteitii, C. estertheticum, C. fallax, C. favososporum, C. felsineum, C. filamentosum, C. formicaceticum, C. frigidicarnis, C. frigoriphilum, C. frigoris, C. fusiformis, C. ganghwense, C. gasigenes, C. grantii, C. guangxiense, C. haemolyticum, C. halophilum, C. homopropionicum, C. huakuii, C. hveragerdense, C. hydrogeniformans, C. hydrolyticum, C. ihumii, C. intestinale, C. isatidis, C. islandicum, C. kluyveri, C. kogasensis, C. lacusfryxellense, C. liquoris, C. ljungdahlii, C. longisporum, C. lundense, C. luticellarii, C. magnum, C. malenominatum, C. massiliodielmoense, C. maximum, C. merdae, C. moniliforme, C. neonatale, C. neuense, C. nitrophenolicum, C. novyi, C. oceanicum, C. oryzae, C. paraputrificum, C. pascui, C. pasteurianum, C. peptidivorans, C. perfringens, C. phoceensis, C. polyendosporum, C. polynesiense, C. proteolyticus, C. psychrophilum, C. punense, C. puniceum, C. putrefaciens, C. quinii, C. ragsdalei, C. roseum, C. saccharobutylicum, C. saccharoperbutylacetonicum, C. sardiniense, C. sartagoforme, C. saudiense, C. scatologenes, C. schirmacherense, C. senegalense, C. septicum, C. sordelli, C. sporogenes, C. subterminale, C. sulfidigenes, C. swellfunianum, C. taeniosporum, C. tagluense, C. tarantellae, C. tepidiprofundi, C. tepidum, C. tertium, C. tetani, C. tetanomorphum, C. thermobutyricum, C. thermopalmarium, C. thermophilus, C. thiosulfatireducens, C. tunisiense, C. tyrobutyricum, C. uliginosum, C. uzonii, C. ventriculi, C. vincentii, C. vulturis, [Butyribacterium] methylotrophicum.
Клостиридии C. sporogenes и другие имеют активные протеолитические ферменты и способны использовать в качестве субстратов белки и пептиды, гидролизуя их до аминокислот и подвергая затем последние сбраживанию. Такие клостридии относят к группе протеолетических клостридий.
Ранее клинически важный вид Clostridium perfringens назывался Clostridium welchii.
Изменения в составе рода Clostridium
В последние годы клостридии были серьёзно реклассифицированы, в частности:
Важнейший клинически вид Clostridium difficile был перенесён во вновь созданный род Clostridioides семейства Peptostreptococcaceae и ему присвоено наименование Clostridioides difficile. В этот же род был перенесён вид Clostridium mangenotii.
Вид Clostridium litorale перемещён в род Peptoclostridium того же семейства Peptostreptococcaceae и переименован в Peptoclostridium litorale.
Вид Clostridium sticklandii перемещён в род Acetoanaerobium семейства Peptostreptococcaceae и переименован в Acetoanaerobium sticklandii.
Вид Clostridium dakarense перемещён в род Romboutsia семейства Peptostreptococcaceae.
Clostridium hiranonis, Clostridium paradoxum, и Clostridium thermoalcaliphilum, их современные наименования: [Clostridium] hiranonis, [Clostridium] paradoxum и [Clostridium] thermoalcaliphilum, перенесены в семейство Peptostreptococcaceae без уточнения рода.
Вид Clostridium histolyticum был перемещён в род Hathewaya семейства Clostridiaceae и ему присвоено наименование Hathewaya histolytica. В этот же род были перенесены виды Clostridium limosum и Clostridium proteolyticum с изменением наименования на Hathewaya limosa и Hathewaya proteolytica, соответственно.
Вид Clostridium ramosum перемещён в род Erysipelatoclostridium, семейство Erysipelotrichaceae, порядок Erysipelotrichales, класс Erysipelotrichia и ему присвоено наименование Erysipelatoclostridium ramosum.
Виды Clostridium aerotolerans, Clostridium aldenense, Clostridium algidixylanolyticum, Clostridium aminophilum, Clostridium amygdalinum, Clostridium asparagiforme, Clostridium bolteae, Clostridium celerecrescens, Clostridium citroniae, Clostridium clostridioforme, Clostridium fimetarium, Clostridium glycyrrhizinilyticum, Clostridium herbivorans, Clostridium hylemonae, Clostridium indolis, Clostridium lavalense, Clostridium methoxybenzovorans, Clostridium polysaccharolyticum, Clostridium populeti, Clostridium saccharolyticum, Clostridium scindens, Clostridium sphenoides, Clostridium symbiosum, Clostridium xylanolyticum были перенесены в род Lachnoclostridium семейства Lachnospiraceae и они в настоящее время именуются [Clostridium] aerotolerans, [Clostridium] aldenense, [Clostridium] algidixylanolyticum, [Clostridium] aminophilum, [Clostridium] amygdalinum, [Clostridium] asparagiforme, [Clostridium] bolteae, [Clostridium] celerecrescens, [Clostridium] citroniae, [Clostridium] clostridioforme, [Clostridium] fimetarium, [Clostridium] glycyrrhizinilyticum, [Clostridium] herbivorans, [Clostridium] hylemonae, [Clostridium] indolis, [Clostridium] lavalense, [Clostridium] methoxybenzovorans, Lachnoclostridium phytofermentans, [Clostridium] polysaccharolyticum, [Clostridium] populeti, [Clostridium] saccharolyticum, [Clostridium] scindens, [Clostridium] sphenoides, [Clostridium] symbiosum, [Clostridium] xylanolyticum, соответственно.
Виды Eubacterium moniliforme и Eubacterium tarantellae перенесены из рода Eubacterium и названы Clostridium moniliforme и Clostridium tarantellae.
Клостридии
СТАЙЛАБ предлагает комплексные тест-системы для анализа клостридий в пищевых продуктах и продовольственном сырье методом ПЦР.
Клостридии – это анаэробные спорообразующие грамположительные бактерии. Они способны жить и размножаться только в отсутствие кислорода. Некоторые из этих бактерий входят в состав нормальной микрофлоры кишечника человека и животных, другие обитают в почве. Клостридии используются для производства спиртов и органических кислот.
Среди патогенных клостридий – возбудители таких заболеваний, как газовая гангрена, столбняк, ботулизм, псевдомембранозные колиты, некротические энтериты. Белковые токсины клостридий – ботулотоксины, тетаноспазмин (тетанотоксин, столбнячный токсин) и ε-токсин относятся к сильнейшим ядам органического происхождения, известным в настоящее время. В пищевых продуктах чаще всего встречаются два представителя клостридий: Clostridium botulinum и Clostridium perfringens.
Clostridium botulinum – это подвижная палочковидная бактерия, обитающая в иле и почве, иногда в организмах рыб. Она не размножается в присутствии кислорода. Однако бескислородная среда консервированных продуктов позволяет Clostridium botulinum размножаться и вырабатывать ботулотоксины. Эти яды разрушаются при кипячении в течение получаса и в щелочной среде (например, в растворе пищевой соды) в течение 1 часа, но проявляют устойчивость к желудочному соку. Наиболее токсичный из ботулотоксинов – ботулотоксин А. Его молекула имеет два связанных между собой домена. После попадания в организм одна часть молекулы превращается в канал в мембране нервной клетки. Вторая часть молекулы отделяется от первой и проникает в клетку по этому каналу, где необратимо препятствует выделению нейромедиатора ацетилхолина. Это приводит к нарушению нервной и нервно-мышечной передаче сигнала и, как следствие, расслаблению мышц. Пострадавшие умирают от остановки дыхания. Скрытый период отравления, во время которого не проявляются никакие его симптомы, зависит от дозы токсина и составляет от нескольких часов до нескольких суток. Отравление ботулотоксином не всегда приводит к смерти, однако противоядия против этого яда не существует. Лечением является симптоматическая и поддерживающая терапия в условиях больницы.
Clostridium botulinum попадает в продукты при нарушении правил их переработки, чаще всего, с землей. Заражены ей могут быть колбасные изделия, консервы из мяса, рыбы, овощей и грибов. Кроме того, иногда эта бактерия встречается в меде. Clostridium botulinum может выжить в пищеварительной системе маленьких детей (до 1 года). В этом случае она становится причиной детского ботулизма. Скрытый период заболевания длится несколько недель, после чего наступает отравление ботулотоксином. У взрослых людей со сниженным иммунитетом, после операций на брюшной полости и с некоторыми другими состояниями также может встречаться такой тип ботулизма.
Ботулизм может возникать не только у людей, но и у животных, зачастую приводя к их гибели. Помимо употребления продуктов, зараженных Clostridium botulinum, отравление ботулотоксином может наступать в результате попадания этого вещества на слизистые оболочки, роговицу глаз, в раны, а также при его вдыхании.
Ботулотоксин А используют в медицине и косметологии в качестве миорелаксанта.
Clostridium perfringens патогенна для человека и животных и является возбудителем пищевых токсикоинфекций, некротических энтеритов, а также газовой гангрены. Эти бактерии обитают в почве и воде, в том числе, в сточных водах. Они способны выживать в кишечнике человека и животных, и их присутствие не всегда приводит к заболеваниям. Clostridium perfringens типа А, в отличие от других бактерий этого вида, относительно устойчива к воздействию кислорода.
Clostridium perfringens выделяет множество ядов с некротическим и гемолитическим (вызывает разрушение клеток крови) действием. Наиболее токсичным из них является выделяемый сероварами B и D ε-токсин (эпсилон-токсин), образующий в клетках каналы, по которым из них выходят ионы калия. Это приводит к отеку различных органов, в том числе, мозга и нарушению их работы. Clostridium perfringens серовара A вызывают относительно легкие пищевые токсикоинфекции.
Clostridium perfringens нередко встречается в сыром мясе животных и птицы и консервах из него. С загрязненной водой эта бактерия может попадать в овощи и фрукты.
В Российской Федерации и странах Таможенного Союза содержание клостридий в пищевых продуктах регламентировано Техническим Регламентом Таможенного Союза ТР ТС 021/2011 «О безопасности пищевой продукции», ТР ТС 034/2013 «О безопасности мяса и мясной продукции» и другими законодательными документами. С актуальной информацией можно ознакомиться на сайте compact24.com
Микробиологические методы анализа клостридий и других анаэробов довольно трудоемки: в присутствии кислорода эти организмы не размножаются, потому необходимо создать им бескислородные условия. Для этого используют различные подходы: культивирование в жидких средах в специальных высоких пробирках или посев внутрь столбика агара, замена воздуха в пробирке углекислым газом, добавка в среды веществ, поглощающих кислород, запаивание пробирок, культивирование под вазелиновым маслом и др. После выделения культуры микроорганизма необходимо определить его биологическими методами, оценив биохимические свойства бактерий или иным методом. Определение ДНК с помощью ПЦР является самым точным способом определения микроорганизма.
Клостридия клостридии волк: С. difficile vs С. scindens
Клостридия клостридии волк: С. difficile vs С. scindens
Автор
Редактор
Тело человека населено триллионами микроорганизмов, совокупность которых называют микробиомом. Микробиом выполняет множество важных функций — от синтеза витаминов до расщепления сложных компонентов пищи. «Здоровая» микрофлора постоянно конкурирует за ограниченные питательные ресурсы с патогенными микроорганизмами, тем самым подавляя их рост. Однако из-за приема антибиотиков или других причин нормальный состав микробиома может нарушаться, и тогда патогены получают возможность размножаться неконтролируемо, вызывая болезни. Один из таких патогенов — бактерия Clostridium difficile, возбудитель псевдомембранозного колита. Борьба с С. difficile осложняется ее устойчивостью к большинству известных антибиотиков. Но недавно было показано, что рост С. difficile можно успешно подавлять не лекарствами, а при помощи родственного ему вида — С. scindens. Это открытие послужит основой для создания «умных» лекарств-пробиотиков: эффективных против С. difficile, но безопасных для полезной микрофлоры.
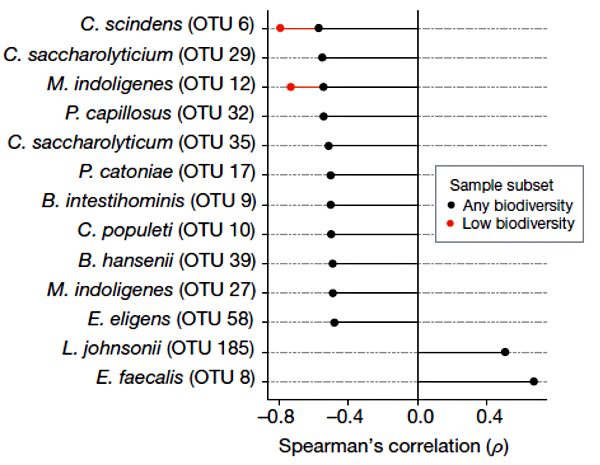
Рисунок 1. Корреляция между присутствием конкретных бактериальных таксонов в микробиоме и устойчивостью к заражению C. difficile [3].
Антибиотики эффективны в борьбе со множеством смертельных заболеваний, но вместе с тем они наносят существенный урон микробиому человека. После курса антибиотиков человек, как правило, более подвержен заражению различными патогенами. Clostridium difficile — грамположительная подвижная бактерия, основной возбудитель острых внутрибольничных кишечных инфекций. За последние 15 лет число смертельных случаев, обусловленных размножением С. difficile, возросло по меньшей мере в 10 раз, особенно среди пожилых и ослабленных людей [1]. Борьба с С. difficile осложняется тем, что при неблагоприятных условиях этот вид образует споры, выдерживающие действие антибиотиков. Такая особенность позволяет бактериям повторно колонизировать кишечник спустя несколько недель и даже месяцев после окончания лечения.
Недавно было показано, что трансплантация микробиомов здоровых доноров вылечивает тяжелые инфекции C. difficile [2]. Однако оставалось неизвестным, какие именно члены микробиома восстанавливают устойчивость организма к инфекции C. difficile и какими механизмами. И вот наконец вышла статья, которая проливает свет на довольно необычный механизм межвидовых взаимодействий в микробиоме [3].
О мышах и людях
C. difficile — не только человеческая беда, но и мышиная. Для начала микробиомы мышей пробовали травить разными антибиотиками и смотрели, как от этого меняется восприимчивость к C. difficile. В целом антибиотики не столько уменьшают суммарное число бактерий в кишечнике, сколько существенно нарушают расстановку сил — соотношение разных таксономических групп. Оказалось, что восприимчивость к C. difficile четко коррелирует с общим снижением видового разнообразия микробима. Удалось выделить горстку из 11 условных видов (операционных таксономических единиц), ассоциированных с устойчивостью к заражению C. difficile (рис. 1). Многие из них оказались тоже клостридиями (кластер Clostridium XIVa). Ученые обратили внимание на один таксон, присутствие которого сильнее всего коррелировало с резистентностью к C. difficile, даже у животных с экстремально низким видовым разнообразием микробиома. Героем оказался Clostridium scindens.
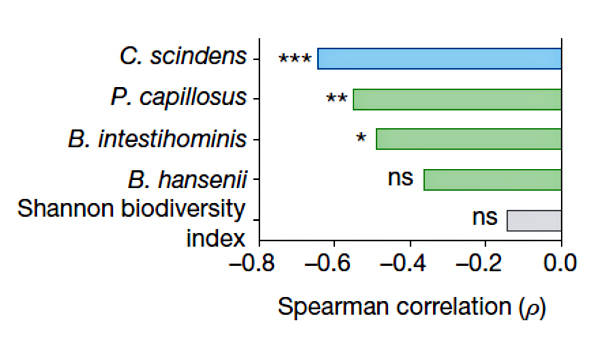
Рисунок 2. Корреляция между приживлением видов-кандидатов в микробиоме и устойчивостью к C. difficile [3].
Но то у мышей. Как же обстоят дела у человека? Для определения видов, связанных с устойчивостью к инфекции C. difficile, исследовали микробиомы пациентов, перенесших аллогеную трансплантацию гемопоэтических стволовых клеток. Большинство из них проходило химиотерапию и/или лучевую терапию одновременно с курсом антибиотиков во время трансплантации. Ослабленный иммунитет и снижение видового разнообразия микробиома делают этих пациентов легкой мишенью для C. difficile. У человека удалось найти два основных вида, с которыми не уживались C. difficile. Наиболее сильным ингибитором оказался C. scindens, как и у мышей. Как будто бы победа?
Для проверки ингибирующего эффекта C. scindens вместе с несколькими другими перспективными бактериями запустили в кишечники животных, недавно принимавших антибиотики (рис. 2). Оказалось, что такая микробная трансплантация существенно облегчила течение инфекции, вызванной C. difficile, а также положительно сказалась на снижении смертности и увеличении массы тела по сравнению с контролем. Наиболее заметную устойчивость к C. difficile обеспечивал, как и ожидалось, C. scindens. Приживление трасплантированных бактерий в микробиоме отслеживали по наличию гена соответствующей 16S рРНК. Устойчивость к C. difficile росла прямо пропорционально обилию C. scindens. То есть улучшение приживаемости C. scindens может повысить защиту против C. difficile. Примечательно, что такая аккуратная замена плохой клостридии на очень похожую, но хорошую, не нарушает существующий в микробиоме баланс (ни качественный, ни количественный). Своеобразная антидотная терапия, только на уровне микробиома. Все это открывает искрящиеся горизонты для разработки безопасных лекарств против C. difficile. Но как именно C. scindens противостоит C. difficile?
Механизм ингибирующего действия
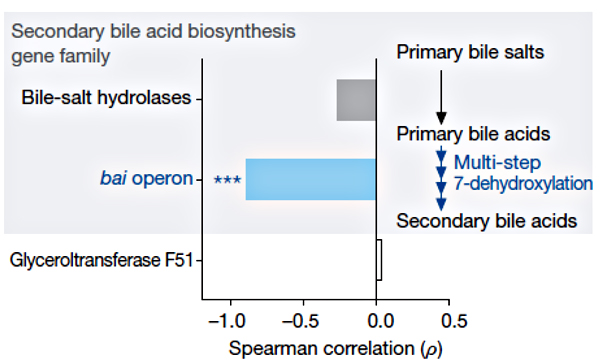
Рисунок 3. Корреляция между устойчивостью к C. difficile и наличием семейств генов, необходимых для синтеза вторичных желчных кислот [3].
Известно, что некоторые вторичные желчные кислоты могут ухудшать рост C. difficile in vitro [4]. У очень большого числа микробиомных бактерий есть ген bsh, кодирующий гидролазу желчных кислот. Однако у редкой бактерии (ужасно малой доли микробиомных организмов) есть все гены, необходимые для осуществления полного пути биосинтеза желчных кислот. Редкой бактерией, конечно же, оказалась C. scindens, обладающая критическим для синтеза вторичных желчных кислот геном 7α-гидроксистероид-дегидрогеназы (рис. 3). Именно на этой уникальной биохимической особенности и зиждется защитный механизм C. scindens против C. difficile. Внедрение C. scindens в микробиом животных, восприимчивых к C. difficile, восстанавливает необходимый уровень и соотношение вторичных желчных кислот: дезоксихолевой (DCA) и литохолевой (LCA). Обе эти кислоты подавляют рост C. difficile пропорционально своей концентрации. Примечательно, что C. scindens повышает количество вторичных желчных кислот до физиологического уровня и препятствует росту C. difficile даже у животных, прошедших курс антибиотикотерапии. Этот механизм консервативен — реализуется как в микробиоме мыши, так и в микробиоме человека.
Терапевтические перспективы
* — О черных делишках кишечных микробов-диверсантов, сокращающих пул желчных кислот и стимулирующих развитие атеросклероза, читайте в статье «Не доверяйте рекламе, или потенциальная связь метаболизма и развития атеросклероза» [6] — Ред.