Клостридиум рамозум что это
Рис.2. Сопоставление распределения ключевых маркеров клостридий C . ramosum с их соотношением в моче ребенка. Приведена общепринятая аббревиатура жирных кислот и альдегидов. Последние отмечены буквой а в конце символа. В профиле липидных компонент стрептококков и метилотрофов сем. Methylomonadaceae альдегиды отсутствуют
Такого рода идентификация клостридий известна в клинической практике:
Allen S.D., Siders J.A., Riddell M.J., Fill J.A. and Wegener W.S. (1995). Cellular
fatty acid analysis in the differentiation of Clostridium species in the clinical
Местообитание и клиническая значимость
Clostridium ramosum – вид бактерий рода Clostridium ; один из возбудителей газовой гангрены. Вызывает газовую гангрену в ассоциации с другими анаэробами. Выделен из фекалий детей и взрослых, из шейки матки. C . ramosum – полиморфные неподвижные грамположительные или грамотрицательные палочки размером 0,5-0,9 х 2-12,8 мкм, образуют круглые, чаще – терминальные споры. Облигатные анаэробы:
Атлас по медицинской микробиологии, вирусологии и иммунологии. Под ред А.А. Воробьева и А.С. Быкова. – М., Медицинское информационное агентство, 2003. – 236 с.: ил.
Brook, I. Bacterial studies of peritoneal cavity and postoperative surgical wound drainage following perforated appendix in children. Annals of Surgery. 1980; 192: 208–12.
С. ramosum обладает близкой к C . perfringens активностью, в том числе также может вызывать газовую гангрену, язвенный и некротизирующий колиты. Они известны как агенты септицемии, нефропатии, бактериемии и менингита.
Известны в рутинной клинической практике выделение и идентификация культурально-биохимическим методом клостридий из вагинального содержимого женщин с хроническими вагинитами и цервицитами в Центре акушерства, гинекологии и перинатологии:
Муравьева В.В., кандидатская диссертация
Г.Р.Байрамова, Гинекология, Том 3/N 2/2001
Franklin R. Cockerill III, John G. Hughes, Emily A. Vetter, Roger A. Mueller, Amy L. Weaver,
Клостридия клостридии волк: С. difficile vs С. scindens
Клостридия клостридии волк: С. difficile vs С. scindens
Автор
Редактор
Тело человека населено триллионами микроорганизмов, совокупность которых называют микробиомом. Микробиом выполняет множество важных функций — от синтеза витаминов до расщепления сложных компонентов пищи. «Здоровая» микрофлора постоянно конкурирует за ограниченные питательные ресурсы с патогенными микроорганизмами, тем самым подавляя их рост. Однако из-за приема антибиотиков или других причин нормальный состав микробиома может нарушаться, и тогда патогены получают возможность размножаться неконтролируемо, вызывая болезни. Один из таких патогенов — бактерия Clostridium difficile, возбудитель псевдомембранозного колита. Борьба с С. difficile осложняется ее устойчивостью к большинству известных антибиотиков. Но недавно было показано, что рост С. difficile можно успешно подавлять не лекарствами, а при помощи родственного ему вида — С. scindens. Это открытие послужит основой для создания «умных» лекарств-пробиотиков: эффективных против С. difficile, но безопасных для полезной микрофлоры.
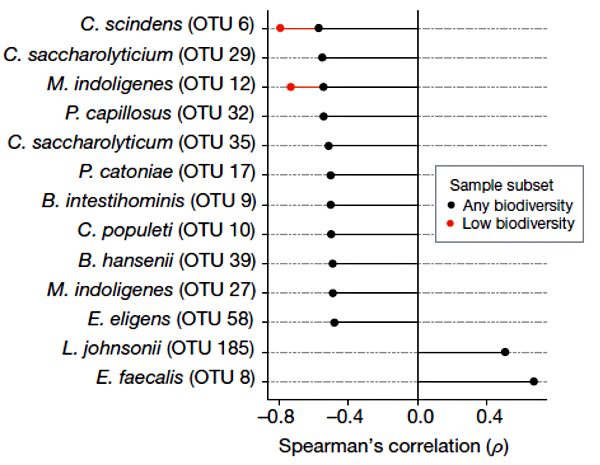
Рисунок 1. Корреляция между присутствием конкретных бактериальных таксонов в микробиоме и устойчивостью к заражению C. difficile [3].
Антибиотики эффективны в борьбе со множеством смертельных заболеваний, но вместе с тем они наносят существенный урон микробиому человека. После курса антибиотиков человек, как правило, более подвержен заражению различными патогенами. Clostridium difficile — грамположительная подвижная бактерия, основной возбудитель острых внутрибольничных кишечных инфекций. За последние 15 лет число смертельных случаев, обусловленных размножением С. difficile, возросло по меньшей мере в 10 раз, особенно среди пожилых и ослабленных людей [1]. Борьба с С. difficile осложняется тем, что при неблагоприятных условиях этот вид образует споры, выдерживающие действие антибиотиков. Такая особенность позволяет бактериям повторно колонизировать кишечник спустя несколько недель и даже месяцев после окончания лечения.
Недавно было показано, что трансплантация микробиомов здоровых доноров вылечивает тяжелые инфекции C. difficile [2]. Однако оставалось неизвестным, какие именно члены микробиома восстанавливают устойчивость организма к инфекции C. difficile и какими механизмами. И вот наконец вышла статья, которая проливает свет на довольно необычный механизм межвидовых взаимодействий в микробиоме [3].
О мышах и людях
C. difficile — не только человеческая беда, но и мышиная. Для начала микробиомы мышей пробовали травить разными антибиотиками и смотрели, как от этого меняется восприимчивость к C. difficile. В целом антибиотики не столько уменьшают суммарное число бактерий в кишечнике, сколько существенно нарушают расстановку сил — соотношение разных таксономических групп. Оказалось, что восприимчивость к C. difficile четко коррелирует с общим снижением видового разнообразия микробима. Удалось выделить горстку из 11 условных видов (операционных таксономических единиц), ассоциированных с устойчивостью к заражению C. difficile (рис. 1). Многие из них оказались тоже клостридиями (кластер Clostridium XIVa). Ученые обратили внимание на один таксон, присутствие которого сильнее всего коррелировало с резистентностью к C. difficile, даже у животных с экстремально низким видовым разнообразием микробиома. Героем оказался Clostridium scindens.
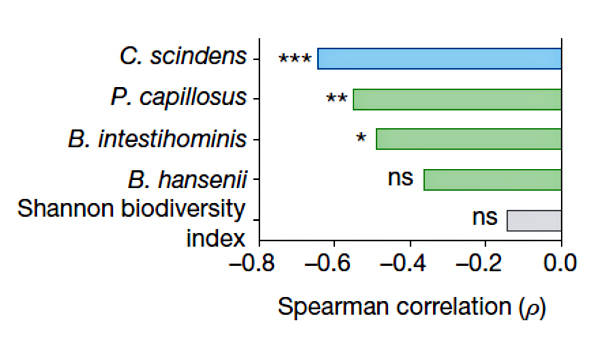
Рисунок 2. Корреляция между приживлением видов-кандидатов в микробиоме и устойчивостью к C. difficile [3].
Но то у мышей. Как же обстоят дела у человека? Для определения видов, связанных с устойчивостью к инфекции C. difficile, исследовали микробиомы пациентов, перенесших аллогеную трансплантацию гемопоэтических стволовых клеток. Большинство из них проходило химиотерапию и/или лучевую терапию одновременно с курсом антибиотиков во время трансплантации. Ослабленный иммунитет и снижение видового разнообразия микробиома делают этих пациентов легкой мишенью для C. difficile. У человека удалось найти два основных вида, с которыми не уживались C. difficile. Наиболее сильным ингибитором оказался C. scindens, как и у мышей. Как будто бы победа?
Для проверки ингибирующего эффекта C. scindens вместе с несколькими другими перспективными бактериями запустили в кишечники животных, недавно принимавших антибиотики (рис. 2). Оказалось, что такая микробная трансплантация существенно облегчила течение инфекции, вызванной C. difficile, а также положительно сказалась на снижении смертности и увеличении массы тела по сравнению с контролем. Наиболее заметную устойчивость к C. difficile обеспечивал, как и ожидалось, C. scindens. Приживление трасплантированных бактерий в микробиоме отслеживали по наличию гена соответствующей 16S рРНК. Устойчивость к C. difficile росла прямо пропорционально обилию C. scindens. То есть улучшение приживаемости C. scindens может повысить защиту против C. difficile. Примечательно, что такая аккуратная замена плохой клостридии на очень похожую, но хорошую, не нарушает существующий в микробиоме баланс (ни качественный, ни количественный). Своеобразная антидотная терапия, только на уровне микробиома. Все это открывает искрящиеся горизонты для разработки безопасных лекарств против C. difficile. Но как именно C. scindens противостоит C. difficile?
Механизм ингибирующего действия
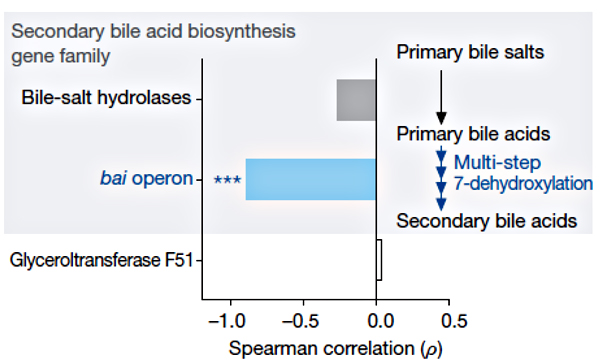
Рисунок 3. Корреляция между устойчивостью к C. difficile и наличием семейств генов, необходимых для синтеза вторичных желчных кислот [3].
Известно, что некоторые вторичные желчные кислоты могут ухудшать рост C. difficile in vitro [4]. У очень большого числа микробиомных бактерий есть ген bsh, кодирующий гидролазу желчных кислот. Однако у редкой бактерии (ужасно малой доли микробиомных организмов) есть все гены, необходимые для осуществления полного пути биосинтеза желчных кислот. Редкой бактерией, конечно же, оказалась C. scindens, обладающая критическим для синтеза вторичных желчных кислот геном 7α-гидроксистероид-дегидрогеназы (рис. 3). Именно на этой уникальной биохимической особенности и зиждется защитный механизм C. scindens против C. difficile. Внедрение C. scindens в микробиом животных, восприимчивых к C. difficile, восстанавливает необходимый уровень и соотношение вторичных желчных кислот: дезоксихолевой (DCA) и литохолевой (LCA). Обе эти кислоты подавляют рост C. difficile пропорционально своей концентрации. Примечательно, что C. scindens повышает количество вторичных желчных кислот до физиологического уровня и препятствует росту C. difficile даже у животных, прошедших курс антибиотикотерапии. Этот механизм консервативен — реализуется как в микробиоме мыши, так и в микробиоме человека.
Терапевтические перспективы
* — О черных делишках кишечных микробов-диверсантов, сокращающих пул желчных кислот и стимулирующих развитие атеросклероза, читайте в статье «Не доверяйте рекламе, или потенциальная связь метаболизма и развития атеросклероза» [6] — Ред.
Клостридии. Всегда рядом, всегда начеку
Ботулизм, столбняк, газовая гангрена… Об этих заболеваниях наслышаны если не все, то очень многие люди. Но если от столбняка существуют вакцины, например АКДС (адсорбированная коклюшно-дифтерийно-столбнячная сыворотка), то от псевдомембранозного колита, некротического энтерита, ботулизма или газовой гангрены таких вакцин нет. А вызываются все эти заболевания бактериями рода Clostridium.
Одним из наиболее распространенных видов клостридий является Clostridium difficile. Ее высевают из почвы, воды (в том числе и морской). Благодаря возможности образовывать эндоспоры (покрываться оболочкой и переживать неблагоприятный период в состоянии своеобразной «спячки») этот вид может длительно, до двух месяцев, сохраняться во внешней среде. Более того, в состоянии эндоспоры клостридия диффициле выдерживает даже кипячение. Чувствительность к антибиотикам у Clostridium difficile от природы очень низкая, поэтому лечение посредством антибиотикотерапии зачастую терпит фиаско.
Clostridium difficile входит в нормофлору (является представителем нормального микробного состава) желудочно-кишечного тракта, обитая преимущественно в толстом кишечнике. Хотя отдельные его представители встречаются и во рту, и в тонком отделе кишечника, и во влагалище у женщин. Чаще всего Clostridium difficile обнаруживается в кишечнике новорожденных (около половины младенцев), а из детей старше 2 лет и взрослых каждый 10 является обладателем этой бактерии.
Clostridium difficile вызывает такие заболевания как псевдомембранозный колит и антибиотикоассоциированные диареи. Патогенные (болезнетворные) свойства этой клостридии обусловлены выделением токсинов А и В, а также белка, угнетающего перистальтику (сократительную функцию) кишечника.
Антибиотикодиссоциированные диареи (сокращенно – ААД) могут вызываться не только клостридией дифициле, а и множеством других микроорганизмов (сальмонеллами, кандидами, клостридией перфрингенс, золотистым стафилококком, клебсиеллой). Этот вид диарей является наиболее частой внутрибольничной инфекцией и связана такая тенденция с тем, что в больницах, во-первых, концентрируется большая масса больных и здоровых людей. А во-вторых, здесь используется множество антибиотиков и дезинфицирующих средств, которые способствуют образованию генераций (поколений) микроорганизмов, устойчивых к антибиотикам. Поэтому в мире ежегодно регистрируется около миллиона случаев ААД. Возникновение антибиотикоассоциированных диарей связано с тем, что антимикробные препараты подавляют как патогенную, так и нормальную микрофлору. Даже однократный прием антибиотиков широкого спектра действия может послужить причиной развития ААД.

Несмотря на это, дети младенческого возраста практически не болеют антибиотикоассоциированными диареями, вызываемыми клостридией диффициле. Связано это с тем, что дети получают с материнским молоком достаточно иммунных факторов, которые могут сдерживать размножение Clostridium difficile. Более того, в младенческом организме нет такого количества сопутствующей условно-патогенной микрофлоры, которая ослабляет иммунитет.
Антибиотикозависимые диареи могут иметь разную симптоматику и течение: от легкой диареи до тяжелейшего псевдомембранозного энтероколита (ПМК). Последний чаще всего вызывается именно клостридией диффициле.
В процессе течения заболевания отмечаются следующие симптомы:
При отсутствии лечения количество смертельных случаев составляет до 30 %.
Характерная особенность болезней, вызванных Clostridium difficile, является то, что около четверти случаев через время повторяются (рецидив заболевания). Причиной этого явления становятся споры клостридий, которые переживают период лечения, либо повторное заражение. Как правило, после лечения больные выздоравливают, или чувствуют себя значительно лучше, но спустя несколько дней (от 3 до 7) развивается рецидив.
Еще одна клостридия, которая может вызывать такие болезни желудочно-кишечного тракта, как пищевые токсикоинфекции и некротический энтерит, — Clostridium perfringens.
Некротический энтерит характеризуется формированием язв и эрозий и деструктивными (разрушающими) изменениями в слизистой оболочке. Первым симптомом заболевания является возникновение участков геморрагического некроза в начальных отделах тощей кишки. Эти участки имеют красный цвет. Наблюдается также сужение просвета кишечника в месте воспаления, за счет отечности стенки. Происходит тромбоз (закупорка) мелких кровеносных сосудов (артериол). У больного отмечаются озноб и лихорадка, рвота и кровавый пенистый понос.
Clostridium perfringens производит ферменты, расщепляющие белки (протеиназа), коллаген (коллагеназа), гиалуроновую кислоту (гиалуронидаза).

Профилактика заболеваний, причиной которых являются клостридии, в первую очередь заключается в соблюдении санитарно-гигиенических норм и правил: мытье и ошпаривание овощей и фруктов; длительная термическая обработка. Но немаловажным является также нормализация микрофлоры и укрепление иммунитета. Причем, как в процессе лечения, так и в процессе предупреждения этих болезней. Ограниченное и строго подконтрольное врачам применение антибиотиков, отказ от самолечения также очень важны для профилактики возникновения АДД и других болезней, связанных с клостридиями.
Клостридиозы у детей
Клостридиозы — острые инфекционные заболевания человека и животных, которые вызваны клостридиями.
Клостридиозы классифицируют по механизму возникновения на травматические и энтеральные. К энтеральным относят: клостридиоз диффициле, клостридиоз перфрингенс, ботулизм. К травматическим относят газовую гангрену и столбняк. Ниже будут рассмотрены клостридиоз диффициле и клостридиоз перфрингенс.
Клостридиоз перфрингенс – острое заболевание инфекционной природы с энтеральным путем заражения, которое проявляется синдромом гастроэнтерита или энтероколита и инфекционным токсикозом, а в более редких случаях и некротическим энтеритом или сепсисом.
Клостридиоз диффициле – острое заболевание инфекционной природы (путь заражения также энтеральный), которое вызывается антибиотикоиндуцированными штаммами клостридий диффициле и проявляется диарейным синдромом с развитием псевдомембранозного колита и инфекционным токсикозом.
Что провоцирует / Причины Клостридиозов у детей:
Человек может заразиться только некоторыми представителями клостридий 2-й и 4-й групп, которые приводят к энтеральным клостридиозам, а также возбудителем столбняка и возбудителями газовой гангрены. Данные бактерии вырабатывают специфические активные экзотоксины.
Клостридии «проживают» в естественной среде в кишечниках животных и человека. Они могут там находиться длительное время и размножаться, но при этом к болезням не приводят. С каловыми массами клостридии попадают во внешнюю среду, в основном в землю. Там они могут «жить» долгий срок в виде спор.
Клостридии перфрингенс длительное время считали возбудителем лишь газовой гангрены. Но в середине прошлого столетия наши связь между данными бактериями и пищевыми токсикоинфекциями.
Клостридии перфрингенс представляю собой короткие полиморфные палочки, которые не имеют жгутиков. Могут образовывать субтерминально расположенные споры. Относятся к строгим анаэробам. Их делят на шесть типов в зависимости от способности производить экзотоксины и ферменты: А, В, С, D, Е, F.
Чаще всего детский кишечный клостридиоз спровоцирован клостридиями перфрингенс типа А, в более редких случаях – типами С и F.
Патогенез (что происходит?) во время Клостридиозов у детей:
Клостридиоз перфрингенс попадает в организме в ЖКТ (желудочно-кишечный тракт) вместе с зараженной едой. Далее они следуют в тонкий кишечник, там размножаются, приводя к развитию воспалительного процесса. Через эпителиальный слой кишечника ребенка они попадают в близлежащие ткани и кровь. Так заболевание переходит в тяжелую септическую форму (но не во всех случаях).
Клостридии перфрингенс продуцируют экзоэнтеротоксины, имеющие цитолитические и некротические свойства, что и определяет основные симптомы, которые проявляются в ходе заболевания.
В кишечнике, многих органах и системах (даже в ЦНС) экзотоксины клостридии перфрингенс приводят к функциональным и структурным изменениям. Может развиться токсикоз и эксикоз. К диарее приводит местный воспалительный процесс в кишечнике ребенка.
Патоморфология клостридиоза перфрингенс. Во время болезни максимальные структурные изменения случаются в тонкой или толстой (реже) кишке. У умерших фиксируют отечность слизистой оболочки кишечника, ее гиперемированность, множественные кровоизлияния, стазы, в более редких случаях и некрозы.
Клостридиоз диффициле начинается лишь во время или по окончанию применения антибиотиков широкого спектра действия, в особенности цефамизина, ампициллина, линкомицина и клиндамицина. Это происходит по причине подавления антибиотиками естественной флоры кишечника, вследствие чего клостридии диффициле могут колонизировать кишечник, размножаясь там и образовывая токсины.
Некоторые антибиотики приводят к энтеротоксинообразованию у бактерий. Помимо этого, нормальная кишечная флора у детей и взрослых производит бета-лактамазу — фермент, разрушающий бета-лактамное кольцо бета-лактамов, чем инактивируется действие антибиотика в кишечнике.
Симптомы Клостридиозов у детей:
Инкубационный период клостридиоза перфрингенс составляет от 6 до 24 часов. Это довольно короткий срок. Болезнь имеет острое начало. Проявляются такие симптомы:
С самого начала клостридиоза перфрингенс стул становится жидкой консистенции, частота дефекации повышается. Стул энтеритный или энтероколитный. Болезнь протекает относительно легко, выздоровление наступает на 3-4 сутки после начала.
Кишечный клостридиоза перфрингенс протекает иногда в тяжелых формах – по типу некротического энтероколита или энтерита. Такой форме болезни подвержены ослабленные дети с длительными дисфункциями желудочно-кишечного тракта; дети, которые пролечили антибиотиками широкого спектра действия; дети с кишечным дисбактериозом. Болезнь начинается по типу острого гастроэнтерита. Появляются боли в животе, частая рвота с наличием крови, стул обильный водянистый или пенистый (дефекация от 15 до 20 раз за сутки). В стуле может наблюдаться примесь крови или слизи. От старших детей поступают жалобы на разбитость и общую слабость, головокружения, боли в животе (могут быть постоянными или схваткообразными). Далее начинается обезвоживание организма ребенка, «падает» артериальное давление. Фиксируют увеличение печени и селезенки, парез кишечника (резкое вздутие живота).
Если болезнь прогрессирует и не вылечена вовремя, может случиться летальный исход вследствие нарушения сердечно-сосудистой деятельности. У ослабленных детей и грудничков инфекция может генерализироваться, развивается сепсис.
Кишечный клостридиоз диффициле в большинстве случаев по симптомам аналогичен псевдомембранозному колиту, в более редких случаях – некротическому энтероколиту или диарейному синдрому. Заболевания псевдомембранозным колитом характерны для грудничков, новорожденных и дошкольников.
Псевдомембранозиый колит появляется, как правило, через неделю-10 дней после начала приема антибиотиков. Болезнь начинается остро – поднимается температура, появляются срыгивания или повторная рвота, боли в животе и диарея. Малыши отказываются от еды, родители могут заметить вздутие живота и снижение массы тела.
Кожа приобретает бледно-серый оттенок, на коже живота часто видна сеть застойных вен. Стул становится жидким, водянистым, наблюдаются примеси слизи и крови (не всегда). В некоторых случаях большая часть стула представляет собой густую белесоватую слизь и обрывки фибринозных наложений. Иногда стул гнойный, с кровянистыми примесями. Для некоторых случаев характерно кишечное кровотечение, что часто приводит к летальному исходу.
Болезнь протекает у новорожденных (в особенности – у недоношенных) тяжело. Наблюдают профузный понос, обезвоживание, расстройство периферического кровообращения или расстройство кровообращения по типу коллапса без диареи.
Если есть изъязвление пораженных участков слизистой оболочки кишечника, могут фиксировать перформацию кишечника и каловый перитонит. При этом состояние ребенка тяжелые, кожа окрашивается в серый оттенок, дыхание поверхностное, резко выражен парез кишечника, наблюдаются гиподинамия и гипорефлексия, заостренность черт лица больного ребенка. Не исключена отечность гениталий. Если лечение не начато вовремя, есть вероятность летального исхода.
Клостридии диффициле, помимо некротических энтероколитов, псевдомембранозных колитов и кишечного сепсиса могут приводить к более легким болезням ЖКТ, которые протекают схоже с энтеритами и энтероколитами, особенностей не имеют.
Диагностика Клостридиозов у детей:
Кишечный клостридиоз перфрингенс диагностируют при помощи эпидемиологических и клинико-лабораторных данных в сумме. Для заболевания характерны острое начало, быстро развитие клинических проявлений – диареи, рвоты, повышения температуры, интоксикации или нейротоксикоза и т. д. Симптомы ярче всего выражены на 1-2 день после начала заболевания. Так же быстро «сходят на нет», как и появляются.
Такие симптомы характерны не только для данного заболевания, потому проводят лабораторную диагностику. Используют экспресс-методы (РНГА и ИФА) для обнаружения в фекалиях больного ребенка энтеротоксина. У выделенных штаммов клостридий определяют энтеротоксигенность.
В крови у больных с кишечным клостридиозом перфрингенс наблюдают умеренный лейкоцитоз и палочко-ядерный сдвиг.
Для диагностики кишечного клостридиоза диффициле необходимы сведения анамнеза о терапии антибиотиками, а также инструментальные и клинические показатели. Проводится комплекс лабораторных исследований для обнаружения в фекалиях больного ребенка специфических токсинов (энтеро- и цитотоксина) и возбудителя.
Селективное выделение клостридии диффициле проводят с помощью циклосерин-цефокситин-фруктозного агара. В последнее время диагностику энтероклостридиоза диффициле проводят с помощью высокочувствительных методов ИФА и РЛА.
Доказать клостридиоз диффициле с помощью только обнаружения возбудителя и его токсинов в кале или другом биоматериале от больного нельзя. Потому что данные микроорганизмы и токсины могут быть и у здорового человека, в основном у недавно рожденных и детей до 6 месяцев.
Лечение Клостридиозов у детей:
Лечебные мероприятия при кишечном клостридиозе перфрингенс аналогичны таковым при других бактериальных диареях. Назначают этиотропную терапию, учитывая чувствительность обнаруженных штаммов клостридий к антибиотикам. Врачи рекомендуют использовать для лечения энтеральные формы антибиотиков, к примеру, азитромицин, амоксиклав, цефалоспорины 3-го поколения и т. д.
Комплексная терапия включает бактерийные препараты, такие как бификол или бифидумбактерин, а также другие препараты для нормализации биоценоза кишечника. Бактерийные препараты служат для прекращения колонизации кишечника клостридиями. При особо тяжелых формах заболевания, если установлен тип возбудителя, для лечения могут применять антитоксическую сыворотку в дозе 5000—10000 АЕ внутримышечно по методу Безредки или энтерально.
Под этиотропной терапией антибиотикоиндуцированного кишечного клостридиоза диффициле подразумевают введение парентеральных аминогликозидов, метронидазола, цефалоспоринов.
После окончания приема антибиотиков следует назначить ребенку прием бактерийных препаратов (к примеру, линекса, бифидумбактерина, лактобактерина и пр). Это поможет нормализовать биоценоз в кишечнике.
Лечат клостридий диффициле также ферментными препаратами, например, фесталом, креоном и т. д., витаминами (в особенности – группой В). Необходима симптоматическая и патогенетическая терапия. Если есть соответствующие показания, применяют инфузионную терапию, чтобы нормализовать баланс жидкости в организме ребенка, провести дезинтоксикацию и парентеральное питание. Применяют антигистаминные препараты, а при тяжелых формах кортикостероиды и специфические антитоксические сыворотки.
Профилактика Клостридиозов у детей:
Самые важные профилактические меры заключаются в:
— строгом соблюдении санитарно-гигиенических норм приготовления, хранения и сбыта пищевых продуктов;
— активном выявлении носителей клостридий среди работников пищеблоков и детских учреждений;
— своевременной изоляции и лечении зараженных клостридиями детей и взрослых;
— санитарно-просветительной работе среди населения о правильном уходе за детьми и их кормлении;
— кратновременном хранении продуктов и термической обработке.
Профилактические меры при кишечном клостридиозе диффициле должны быть направлены, прежде всего, на предупреждение антибиотикоиндуцированности как важнейшего фактора заболевания этим клостридиозом.
Не следует использовать как профилактическое или лечебное средство антибактериальные лекарства широкого спектра действия длительными курсами.
Чтобы избежать колонизации кишечника клостридиями, необходимо вовремя лечить кишечный дисбактериоз и проводить его профилактику. В стационарах, особенно в отделениях для новорожденных, следует обеспечивать необходимый санитарно-гигиенический режим, правильную дезинфекцию инструментария, посуды, белья и т. д.
Обработка предметов проводится с помощью хлориндиоксида или его аналогов, имеющих бактерицидные и спороцидные свойства, влияющие на клостридий.