Коактивация мышц что это
«Установка» части тела путем сокращения мышц агонистов и антагонистов на противоположных сторонах сустава. Коактивация мышц агонистов и антагонистов. Практически все движения тела связаны с одновременным сокращением мышц агонистов и антагонистов на противоположных сторонах суставов, что называют коактивацией мышц агонистов и антагонистов. Коактивация контролируется двигательными центрами головного и спинного мозга.
Положение каждой части тела, например руки или ноги, определяется относительными степенями сокращения групп мышц агонистов и антагонистов. Предположим, что рука или нога должны находиться в среднем положении. Для этого мышцы агонисты и антагонисты возбуждаются примерно в одинаковой степени. Вспомните, что мышцы при удлинении сокращаются с большей силой, чем при укорочении: мышца развивает максимальную силу сокращения при ее полной функциональной длине и не развивает почти никакой силы при длине, равной половине исходной. Следовательно, удлиненная мышца на одной стороне сустава может сокращаться с гораздо большей силой, чем более короткая мышца на противоположной стороне.
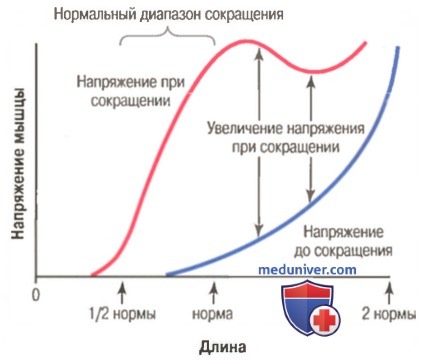
По мере того, как рука или нога движутся в направлении своего среднего положения, сила сокращения более длинной мышцы уменьшается, тогда как сила сокращения более короткой мышцы возрастает до тех пор, пока обе силы не станут равны друг другу. В этот момент движение руки или ноги останавливается. Таким образом, путем изменения степени активации мышц агонистов и антагонистов нервная система управляет положением руки или ноги.
Реконструкция мышцы для приведения ее в соответствие с функцией
Все мышцы тела постоянно реконструируются, приспосабливаясь к предназначенной им функции. Изменяются их диаметр, длина, развиваемая сила, снабжение сосудами и даже типы мышечных волокон (в небольшой степени). Этот процесс реконструкции часто осуществляется довольно быстро — в течение нескольких недель. Эксперименты на животных показали, что в некоторых мелких, активных мышцах сократительные белки могут замещаться в течение такого небольшого периода как 2 нед.
Гипертрофия и атрофия мышц. Увеличение общей массы мышцы называют мышечной гипертрофией, а уменьшение — мышечной атрофией.
Мышечная гипертрофия практически всегда является результатом увеличения количества актиновых и миозиновых нитей в каждом мышечном волокне, что ведет к их укрупнению. Это называют простой гипертрофией волокон. Степень гипертрофии значительно возрастает, если во время сокращения мышца нагружена. Для развития значительной гипертрофии достаточно лишь нескольких сильных сокращений в день в течение 6-10 нед.
Механизм, с помощью которого сильное сокращение ведет к гипертрофии, не ясен. Известно, однако, что при развитии гипертрофии резко ускоряется синтез мышечных сократительных белков. Это способствует постепенному увеличению числа актиновых и миозиновых нитей в миофибриллах, количество которых часто возрастает до 50%. Отмечено также, что некоторые миофибриллы в гипертрофированной мышце сами расщепляются с формированием новых миофибрилл, но важность этого процесса при обычной мышечной гипертрофии еще неизвестна.
Наряду с увеличением размера миофибрилл также усиливаются ферментные энергообразующие системы. Это особенно выражено у ферментов для гликолиза, который обеспечивает быструю доставку энергии во время мощного кратковременного сокращения мышцы.
Если в течение многих недель мышца не используется, скорость распада сократительных белков в ее волокнах становится выше скорости их восстановления. В результате развивается мышечная атрофия.
Приспособление длины мышцы. Когда мышцы растягиваются за пределы их нормальной длины, развивается другой тип гипертрофии. Это ведет к добавлению новых саркомеров на концах мышечных волокон, где они прикрепляются к сухожилиям. Известно, что во вновь развивающейся мышце новые саркомеры могут добавляться очень быстро — до нескольких саркомеров в минуту, что характеризует возможную скорость развития этого типа гипертрофии. Напротив, если мышца постоянно остается короче нормальной длины, саркомеры на концах мышечных волокон могут фактически исчезнуть. С помощью этих процессов мышцы постоянно реконструируются, чтобы иметь соответствующую длину для надлежащего мышечного сокращения.
Гиперплазия мышечных волокон. Когда мышца развивает чрезмерную силу сокращения (в редких случаях), кроме гипертрофии волокон возрастает и их абсолютное число. Это увеличение числа волокон называют гиперплазией. Во время этого процесса происходит линейное расщепление предварительно увеличенных волокон.
Коактивация мышц что это
Около 40% массы тела человека составляют скелегные мышцы, и, вероятно, 10% приходится на долю гладких мышц и мышцы сердца. Некоторые из основных принципов сокращения являются общими для разных типов мышц.
На рисунке показана схема организации скелетной мышцы. Все скелетные мышцы содержат множество волокон диаметром от 10 до 80 мкм. На рисунке также показано, что каждое из этих волокон состоит из последовательно соединенных более мелких элементов.
В большинстве скелетных мышц каждое волокно вытянуто во всю длину мышцы и, за исключением примерно 2%, обычно иннервируется лишь одним нервным окончанием вблизи середины волокна.
Сарколемма. Сарколеммой называют клеточную мембрану мышечного волокна. Она состоит из собственно мембраны клетки, называемой плазматической мембраной, и наружного покрытия из тонкого слоя полисахаридного материала, который содержит множество тонких коллагеновых нитей. На концах мышечного волокна этот поверхностный слой сарколеммы сливается с сухожильными волокнами. Сухожильные волокна, в свою очередь, собираются в пучки и формируют мышечные сухожилия, вплетающиеся в кости.
Миофибриллы. Нити актина и миозина. Каждое мышечное волокно содержит от нескольких сотен до нескольких тысяч миофибрилл, которые представлены на поперечном срезе в виде небольших светлых точек. Каждая миофибрилла собрана примерно из 1500 смежных нитей миозина и 3000 нитей актина, представляющих собой большие полимеризованные белковые молекулы, ответственные за мышечное сокращение. Они видны в продольном сечении на электронной микрофотографии. Толстые нити на схемах — миозиновые, тонкие — актиновые.
Обратите внимание, что на рисунке актиновые и миозиновые нити частично перекрываются, в связи с чем миофибриллы имеют чередующиеся светлые и темные полоски. Светлые полоски содержат только актиновые нити, их называют I-полосками, поскольку они изотропны в поляризованном свете. Темные полоски содержат миозиновые нити, а также концы актиновых нитей, которые частично накладываются на миозиновые нити. Эти полоски называют А-полосками, поскольку они анизотропны в поляризованном свете. На рисунке видны также маленькие выступы по сторонам миозиновых нитей. Это так называемые поперечные мостики. Их взаимодействие с актиновыми нитями лежит в основе сокращения мыщц.
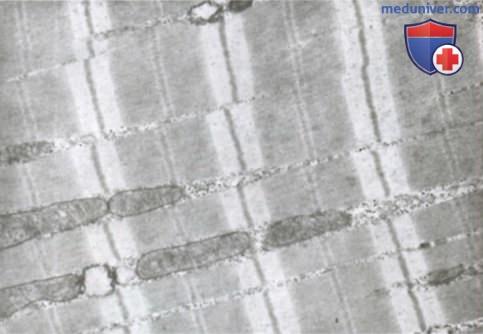
На рисунке показано также, что концы актиновых нитей прикреплены к так называемому Z-диску (Z-мембране). Отсюда актиновые нити распространяются в обе стороны, проходя между миозиновыми нитями. Z-диск, состоящий из нитевидных белков, отличающихся от актиновых и миозиновых нитей, проходит в поперечном направлении через миофибриллу, а также через все мышечное волокно, переходя от одной миофибриллы к другой, скрепляя их между собой. В связи с этим целое мышечное волокно, как и отдельные миофибриллы, имеет светлые и темные полоски. Эти полоски придают скелетным и сердечной мышцам характерный полосатый вид.
Часть миофибриллы (или целого мышечного волокна), расположенную между двумя последовательными Z-дисками, называют саркомером. В сокращенном мышечном волокне длина саркомера равна примерно 2 мкм. При этой длине актиновые нити полностью перекрывают миозиновые, и кончики актиновых нитей начинают перекрывать друг друга. Мы увидим далее, что при этой длине мышца способна генерировать максимальную силу сокращения.
Что удерживает актиновые и миозиновые нити на месте? Удерживать актиновые и миозиновые нити рядом довольно трудно. Это обеспечивается с помощью большого числа нитевидных молекул белка, называемого тайтином. Каждая молекула тайтина имеет молекулярную массу около 3000000, что делает ее одной из самых крупных белковых молекул в организме. Кроме того, поскольку молекула тайтина волокнистая, она очень упруга. Упругие молекулы тайтина образуют каркас, удерживающий актиновые и миозиновые нити в положении, обеспечивающем нормальную работу сократительного аппарата саркомера. Это позволяет полагать, что сама молекула тайтина действует как матрица для начального формирования участков сократительных нитей саркомера, особенно миозиновых нитей.
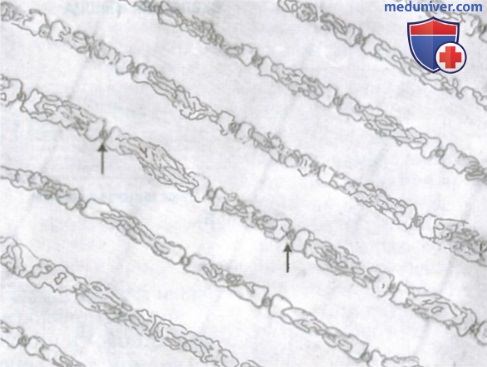
Саркоплазма. В каждом мышечном волокне многочисленные миофибриллы расположены рядом, бок о бок. Пространство между ними заполнено внутриклеточной жидкостью, называемой саркоплазмой и содержащей большое количество калия, магния и фосфатов, а также множество ферментов. Кроме того, имеется огромное число митохондрий, расположенных параллельно миофибриллам. Они снабжают сокращающиеся миофибриллы большим количеством энергии в форме аденозинтрифосфата, синтезируемого митохондриями.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Коактивация мышц что это
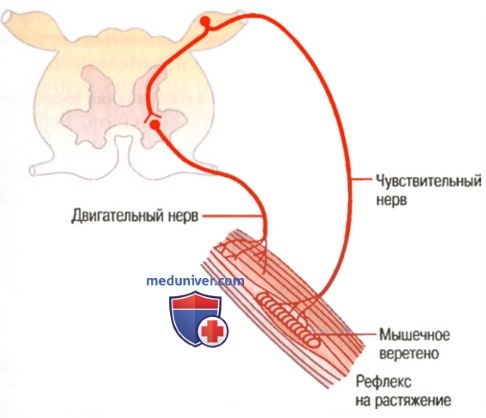
а) Роль мышечных веретен в произвольной двигательной активности. Важность гамма-эфферентной системы подчеркивает тот факт, что 31% всех двигательных нервных волокон к мышцам представлены тонкими эфферентными волокнами типа Аγ, а не толстыми двигательными волокнами типа Аα. Каждый раз, когда сигналы передаются от двигательной коры или от любой другой области головного мозга к альфа-мотонейронам, в большинстве случаев одновременно стимулируются гамма-мотонейроны, что называют коактивацией альфа- и гамма-мотонейронов.
Это ведет к одновременному сокращению экстрафузальных волокон скелетных мышц и интрафузальных волокон мышечных веретен.
Сокращение интрафузальных мышечных волокон одновременно с сокращением крупных мышечных волокон скелетных мышц имеет двойное значение. Во-первых, это удерживает длину рецепторной части мышечного веретена от изменений во время сокращения всей мышцы. Следовательно, коактивация сдерживает противодействие рефлекса с мышечных веретен мышечному сокращению. Во-вторых, это сохраняет соответствующую функцию демпфирования мышечного веретена, независимо от любых изменений длины мышцы.
Например, если бы мышечное веретено не сокращалось и не расслаблялось вместе с крупными мышечными волокнами, рецепторная часть веретена была бы то слишком свободна, то перерастянута, что не соответствует оптимальным условиям для функции веретена.
б) Области головного мозга, регулирующие гамма-эфферентную систему. Гамма-эфферентная система возбуждается непосредственно сигналами из бульборетикулярной облегчающей области ствола мозга и опосредованно — импульсами, передаваемыми в бульборетикулярную область от:
(2) базальных ганглиев;
(3) коры большого мозга.
О точных механизмах контроля гамма-эфферентной системы известно мало. Однако поскольку бульборетикулярная облегчающая область прежде всего связана с сокращениями антигравитационных мышц (а эти мышцы имеют очень высокую плотность мышечных веретен), считают, что особое значение гамма-эфферентный механизм имеет для демпфирования (сглаживания) движений разных частей тела во время ходьбы и бега.
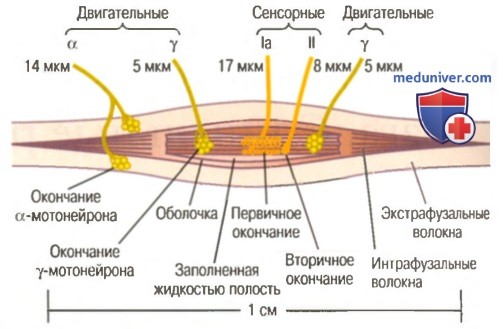
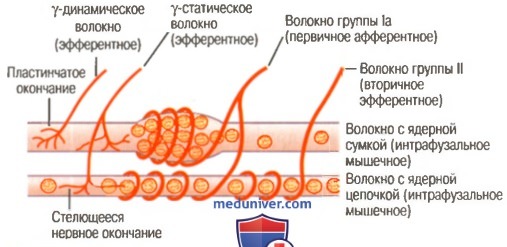
в) Система мышечных веретен стабилизирует положение тела во время напряженной деятельности. Одной из наиболее важных функций системы мышечных веретен является стабилизация положения тела во время напряженной мышечной деятельности. Для этого бульборетикулярная облегчающая область и связанные с ней области мозгового ствола передают возбуждающие сигналы через гамма-нервные волокна к интрафузальным мышечным волокнам.
Это укорачивает концы веретен и растягивает их центральные рецепторные области, усиливая сенсорный сигнал. Однако если веретена одновременно активируются в скелетных мышцах, расположенных по обе стороны каждого сустава, рефлекторное возбуждение этих мышц также возрастает, обеспечивая в окружении сустава сильное напряжение мышц, противодействующих друг другу. В результате положение сустава становится очень устойчивым, и любой силе, которая пытается его нарушить, противодействуют чрезвычайно чувствительные рефлексы на растяжение, действующие с обеих сторон сустава.
Каждый раз, когда человек должен выполнять мышечную работу, которая требует тонкой и точной регулировки положения тела, возбуждение соответствующих мышечных веретен сигналами из бульборетикулярной облегчающей области ствола мозга стабилизирует положение основных суставов. Это очень помогает выполнению дополнительных тонких произвольных движений (пальцами или другими частями тела), необходимых для сложных двигательных манипуляций.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Коактивация мышц что это
АТФ как источник энергии для сокращения. Химические явления при движении головок миозина. При сокращении мышцы выполняется работа и расходуется энергия. Во время процесса сокращения много молекул АТФ расщепляются с формированием АДФ. Чем больше работа, производимая мышцей, тем больше расщепляется АТФ. Это называют эффектом Фена. При этом, как полагают, происходят следующие явления.
1. До начала сокращения головки поперечных мостиков связываются с АТФ. АТФ-азная активность головки миозина немедленно расщепляет АТФ, но продукты расщепления (АДФ и фосфатный ион) остаются связанными с головкой. В этом состоянии конформация головки такова, что она располагается перпендикулярно нити актина, но еще не прикрепляется к ней.
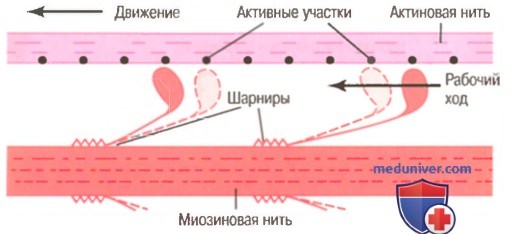
2. Когда тропонин-тропомиозиновый комплекс связывается с ионами кальция, активные участки нити актина открываются, и миозиновые головки соединяются с ними.
3. Связь между головкой поперечного мостика и активным участком на нити актина вызывает конформационное изменение в головке, заставляющее ее наклониться к плечу поперечного мостика. Это обеспечивает рабочий ход для протягивания актиновой нити. Рабочий ход активируется энергией, сохраненной в головке, как во «взведенной» пружине, в виде ее конформационного изменения, происходящего ранее во время расщепления молекулы АТФ.
4. Наклон головки поперечного мостика позволяет освободить АДФ и фосфатный ион, предварительно соединенные с головкой. К месту, от которого выделилась АДФ, прикрепляется новая молекула АТФ, что ведет к отсоединению головки от актина.
5. После отсоединения головки от актина новая молекула АТФ расщепляется, начиная следующий цикл, ведущий к новому рабочему ходу. Это значит, что энергия снова «взводит» головку в перпендикулярное положение, из которого она готова начать новый цикл рабочего хода.
6. Когда «взведенная» головка (с запасом энергии, извлеченной из расщепленной АТФ) связывается с новым активным участком на нити актина, она «разряжается», обеспечивая новый рабочий ход. Таким образом, процесс повторяется снова и снова до тех пор, пока нити актина не притянут Z-диску вплотную к концам миозиновых нитей или пока нагрузка на мышцу не станет слишком большой для осуществления дальнейшей тяги.
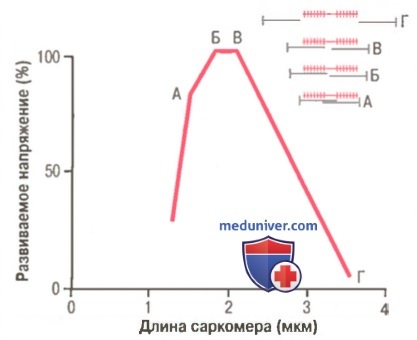
Видно, что максимальная сила сокращения развивается при длине саркомера 2,0-2,2 мкм.
Вверху справа показано относительное расположение актиновых и миозиновых нитей при разной длине саркомера, соответственно точкам от А до Г.
На рисунке демонстрируется влияние длины саркомера и степени перекрытия миозиновых и актиновых нитей на активное напряжение, развиваемое сокращающимся мышечным волокном. Справа черными линиями показаны разные степени перекрытия миозиновых и актиновых нитей при разной длине саркомера. В точке Г на кривой актиновая нить по всей длине оттянута от конца миозиновой нити, и перекрытие между актином и миозином отсутствует. В этом случае напряжение, развиваемое активированной мышцей, равно нулю. Затем по мере укорочения саркомера нить актина начинает перекрывать миозиновую нить, и напряжение постепенно увеличивается до тех пор, пока длина саркомера не уменьшится примерно до 2,2 мкм.
В этом случае актиновая нить перекрывает все поперечные мостики миозиновой нити, но еще не достигает ее центра. При дальнейшем укорочении саркомер сохраняет максимальное на пряжение до тех пор, пока длина саркомера не уменьшится до 2 мкм, что соответствует точке Б на кривой. В этом случае концы двух актиновых нитей начинают перекрывать друг друга в дополнение к перекрытию миозиновых нитей. По мере уменьшения длины саркомера от 2 мкм вплоть до 1,65 мкм, как в точке А, сила сокращения быстро уменьшается. В этой точке два Z-диска саркомера примыкают к концам миозиновых нитей. Если осуществляется сокращение с целью еще большего укорочения саркомера, концы миозиновых нитей изгибаются, и, как видно на рисунке, сила сокращения приближается к нулю, однако вся мышца теперь сжата до своей минимальной длины.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Коактивация мышц что это
Выделяют несколько последовательных этапов запуска и осуществления мышечного сокращения.
1. Потенциал действия распространяется вдоль двигательного нервного волокна до его окончаний на мышечных волокнах.
2. Каждое нервное окончание секретирует небольшое количество нейромедиатора ацетилхолина.
3. Ацетилхолин действует на ограниченную область мембраны мышечного волокна, открывая многочисленные управляемые ацетилхолином каналы, проходящие сквозь белковые молекулы, встроенные в мембрану.
4. Открытие управляемых ацетилхолином каналов позволяет большому количеству ионов натрия диффундировать внутрь мышечного волокна, что ведет к возникновению на мембране потенциала действия.
5. Потенциал действия проводится вдоль мембраны мышечного волокна так же, как и по мембране нервного волокна.
6. Потенциал действия деполяризует мышечную мембрану, и большая часть возникающего при этом электричества течет через центр мышечного волокна. Это ведет к выделению из саркоплазматического ретикулума большого количества ионов кальция, которые в нем хранятся.
7. Ионы кальция инициируют силы сцепления между актиновыми и миозиновыми нитями, вызывающие скольжение их относительно друг друга, что и составляет основу процесса сокращения мыщц.
8. Спустя долю секунды с помощью кальциевого насоса в мембране саркоплазматического ретикулума ионы кальция закачиваются обратно и сохраняются в ретикулуме до прихода нового потенциала действия. Удаление ионов кальция от миофибрилл ведет к прекращению мышечного сокращения.
Далее мы обсудим молекулярные механизмы этого процесса.
Молекулярные механизмы мышечного сокращения
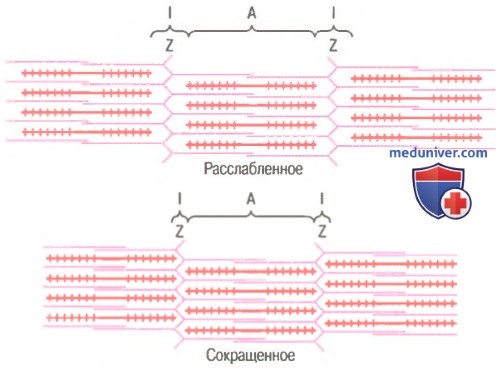
Механизм скольжения нитей для мышечного сокращения. На рисунке показан основной механизм мышечного сокращения. Показано расслабленное состояние саркомера (вверху) и сокращенное состояние (внизу). В расслабленном состоянии концы актиновых нитей, отходящие от двух последовательных Z-дисков, лишь незначительно перекрываются. Наоборот, в сокращенном состоянии актиновые нити втягиваются внутрь между миозиновыми так сильно, что их концы максимально перекрывают друг друга. При этом Z-диски притягиваются актиновыми нитями к концам миозиновых. Таким образом, мышечное сокращение осуществляется путем механизма скольжения нитей.
Что заставляет нити актина скользить внутрь среди нитей миозина? Это связано с действием сил, генерируемых при взаимодействии поперечных мостиков, исходящих от нитей миозина, с нитями актина. В условиях покоя эти силы не проявляются, однако распространение потенциала действия вдоль мышечного волокна приводит к выделению из саркоплазматическо-го ретикулума большого количества ионов кальция, которые быстро окружают миофи-бриллы. В свою очередь, ионы кальция активируют силы взаимодействия между нитями актина и миозина, в результате начинается сокращение. Для осуществления процесса сокращения необходима энергия. Ее источником являются высокоэнергетические связи молекулы АТФ, которая разрушается до АДФ с высвобождением энергии. В следующих разделах мы приведем известные детали молекулярных процессов сокращения.
Молекулярные особенности сократительных нитей
Миозиновая нить. Она состоит из множества молекул миозина, молекулярная масса каждой составляет около 480000. На рисунке показана отдельная молекула; и также — объединение многих молекул миозина в миозиновую нить, а также взаимодействие одной стороны этой нити с концами двух актиновых нитей.
В состав молекулы миозина входят 6 полипептидных цепей: 2 тяжелые цепи с молекулярной массой около 200000 каждая и 4 легкие цепи с молекулярной массой около 20000 каждая. Две тяжелые цепи спирально закручиваются вокруг друг друга, формируя двойную спираль, которую называют миозиновым хвостом. С одного конца обе цепи изгибаются в противоположных направлениях, формируя глобулярную полипептидную структуру, называемую миозиновой головкой. Таким образом, на одном конце двойной спирали молекулы миозина образуются 2 свободные головки; 4 легкие цепи также включены в состав миозиновой головки (по 2 в каждой). Они помогают регулировать функцию головки во время мышечного сокращения.
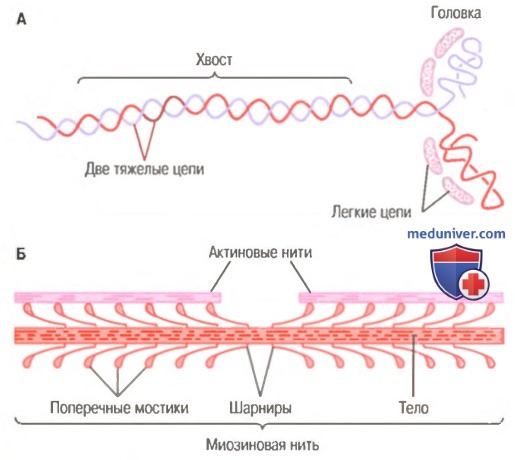
Б. Объединение многих молекул миозина в одну миозиновую нить.
Показаны также тысячи миозиновых поперечных мостиков и взаимодействие их головок с прилежащими актиновыми нитями.
Миозиновая нить состоит из 200 или более отдельных молекул миозина. Видно, что хвосты молекул миозина объединяются, формируя тело нити, а многочисленные головки молекул выдаются наружу по сторонам тела. Кроме того, наряду с головкой в сторону выступает часть хвоста каждой миозиновой молекулы, образуя плечОу которое выдвигает головку наружу от тела, как показано на рисунке. Выступающие плечи и головки вместе называют поперечными мостиками. Каждый поперечный мостик может сгибаться в двух точках, называемых шарнирами. Один из них расположен в месте, где плечо отходит от тела миозиновой нити, а другой — где головка крепится к плечу. Движение плеча позволяет головке или выдвигаться далеко наружу от тела миозиновой нити, или приближаться к телу. В свою очередь, повороты головки участвуют в процессе сокращения, что обсуждается в следующих разделах.
Общая длина каждой миозиновой нити остается постоянной и равна почти 1,6 мкм. В самом центре миозиновой нити на протяжении 0,2 мкм поперечных мостиков нет, поскольку снабженные шарнирами плечи отходят в стороны от центра.
Сама миозиновая нить сплетена таким образом, что каждая последующая пара поперечных мостиков смещена в продольном направлении относительно предыдущей на 120°, что обеспечивает распределение поперечных мостиков во всех направлениях вокруг нити.
АТФ-азная активность миозиновой головки. Есть и другая особенность миозиновой головки, необходимая для мышечного сокращения: миозиновая головка функционирует как фермент АТФ-аза. Как объясняется далее, это свойство позволяет головке расщеплять АТФ и использовать энергию расщепления высокоэнергетической связи для процесса сокращения.
Актиновая нить. Актиновая нить состоит из трех белковых компонентов: актина, тропомиозина и тропонина.
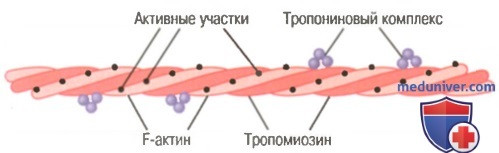
К одному концу каждой молекулы тропомиозина прикреплен тропониновый комплекс, который запускает сокращение.
Основой актиновой нити являются две цепи белковой молекулы F-актина. Обе цепи закручиваются в спираль так же, как и молекула миозина.
Каждая цепь двойной спирали F-актина состоит из полимеризованных молекул G-актина с молекулярной массой около 42000. К каждой молекуле G-актина прикреплена 1 молекула АДФ. Полагают, что эти молекулы АДФ являются активными участками на актиновых нитях, с которыми взаимодействуют поперечные мостики миозиновых нитей, обеспечивая мышечное сокращение. Активные участки на обеих цепях F-актина двойной спирали расположены со смещением таким образом, что вдоль всей поверхности актиновой нити встречается один активный участок примерно через каждые 2,7 нм.
Длина каждой актиновой нити — около 1 мкм. Основания актиновых нитей прочно встроены в Z-диски; концы этих нитей выступают в обоих направлениях, располагаясь в пространствах между миозиновыми молекулами.
Молекулы тропомиозина. Актиновая нить также содержит другой белок — тропомиозин. Каждая молекула тропомиозина имеет молекулярную массу 70000 и длину 40 нм. Эти молекулы спирально оплетают спираль из F-актина. В состоянии покоя молекулы тропомиозина располагаются поверх активных участков актиновых нитей, препятствуя их взаимодействию с миозиновыми нитями, лежащему в основе сокращения.
Тропонин и его роль в мышечном сокращении. По ходу молекул тропомиозина к ним периодически прикреплены другие белковые молекулы, называемые тропонином. Они представляют собой комплексы трех слабосвязанных белковых субъединиц, каждая из которых играет специфическую роль в регуляции мышечного сокращения. Одна из субъединиц (тропонин I) имеет высокое сродство к актину, другая (тропонин Т) — к тропомиозину, третья (тропонин С) — к ионам кальция. Считают, что этот комплекс прикрепляет тропомиозин к актину. Высокое сродство тропонина к ионам кальция, как полагают, инициирует процесс сокращения, о чем говорится в следующей статье.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»



