Спонтанный пневмоторакс
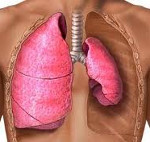
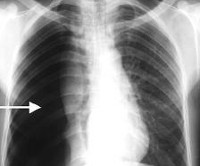
Спонтанный пневмоторакс – это патологическое состояние, характеризующееся внезапным нарушением целостности висцеральной плевры и поступлением воздуха из легочной ткани в плевральную полость. Развитие спонтанного пневмоторакса сопровождается остро возникающей болью в грудной клетке, одышкой, тахикардией, бледностью кожных покровов, акроцианозом, подкожной эмфиземой, стремлением пациента принять вынужденное положение. С целью первичной диагностики спонтанного пневмоторакса проводится рентгенография легких и диагностическая плевральная пункция; для установления причин заболевания требуется углубленное обследование (КТ, МРТ, торакоскопия). Лечение спонтанного пневмоторакса включает дренирование плевральной полости с активной или пассивной эвакуацией воздуха, видеоторакоскопические или открытые вмешательства (плевродез, удаление булл, резекцию легкого, пульмонэктомию и др.)
МКБ-10
Общие сведения
Под спонтанным пневмотораксом в клинической пульмонологии понимают идиопатический, самопроизвольный пневмоторакс, не связанный с травмой или ятрогенными лечебно-диагностическими вмешательствами. Спонтанный пневмоторакс статистически чаще развивается у мужчин и преобладает среди лиц трудоспособного возраста (20-40 лет), что предопределяет не только медицинскую, но и социальную значимость проблемы.
Если при травматическом и ятрогенном пневмотораксе четко прослеживается причинно-следственная связь между заболеванием и внешним воздействием (травмой грудной клетки, пункцией плевральной полости, катетеризацией центральных вен, торакоцентезом, биопсией плевры, баротравмой и др.), то в случае спонтанного пневмоторакса такая обусловленность отсутствует. Поэтому выбор адекватной диагностической и лечебной тактики является предметом повышенного внимания пульмонологов, торакальных хирургов, фтизиатров.
Причины
Первичный спонтанный пневмоторакс развивается у лиц, не имеющих клинически диагностированной патологии легких. Однако при проведении диагностической видеоторакоскопии или торакотомии у данного контингента больных в 75-100% случаев выявляются субплеврально расположенные эмфизематозные буллы. Отмечена взаимосвязь между частотой спонтанного пневмоторакса и конституциональным типом пациентов: заболевание чаще возникает у худых высоких молодых людей. Курение увеличивает риски развития спонтанного пневмоторакса до 20 раз.
Вторичный спонтанный пневмоторакс может развиваться на фоне широкого круга патологий:
К относительно редким формам спонтанного пневмоторакса относят менструальный и неонатальный пневмоторакс. Менструальный пневмоторакс этиологически связан с грудным эндометриозом и развивается у молодых женщин в первые двое суток от начала менструации. Вероятность рецидива менструального пневмоторакса, даже на фоне консервативной терапии эндометриоза, составляет около 50%, поэтому сразу после установления диагноза с целью предотвращения повторных эпизодов спонтанного пневмоторакса может выполняться плевродез.
Неонатальный пневмоторакс – спонтанный пневмоторакс новорожденных встречается у 1-2% детей, в 2 раза чаще у мальчиков. Патология может быть связана с проблемами расправления легкого, респираторным дистресс-синдромом, разрывом ткани легкого при проведении ИВЛ, пороками развития легких (кистами, буллами).
Патогенез
Степень выраженности структурных изменений зависит от времени, прошедшего с момента возникновения спонтанного пневмоторакса, наличия исходных патологических нарушений в легком и висцеральной плевре, динамики воспалительного процесса в плевральной полости.
При спонтанном пневмотораксе имеет место патологическое легочно-плевральное сообщение, обусловливающее попадание и скопление воздуха в плевральной полости; частичный или полный коллапс легкого; смещение и флотация средостения.
Воспалительная реакция развивается в полости плевры через 4-6 часов после эпизода спонтанного пневмоторакса. Она характеризуется гиперемией, инъекцией сосудов плевры, образованием незначительного количества серозного экссудата. В течение 2-5 суток нарастает отечность плевры, особенно на участках ее контакта с проникшим воздухом, увеличивается количество выпота, происходит выпадение фибрина на поверхность плевры.
Прогрессирование воспалительного процесса сопровождается разрастанием грануляций, фиброзной трансформацией выпавшего фибрина. Спавшееся легкое фиксируется в поджатом состоянии и становится неспособным к расправлению. В случае присоединения гемоторакса или инфекции со временем развивается эмпиема плевры; возможно образование бронхоплеврального свища, поддерживающего течение хронической эмпиемы плевры.
Классификация
По этиологическому принципу различают первичный и вторичный спонтанный пневмоторакс. О первичном спонтанном пневмотораксе говорят при отсутствии данных за клинически значимую легочную патологию. Возникновение вторичного спонтанного пневмоторакса происходит на фоне сопутствующих легочных заболеваний.
В зависимости от степени коллабирования легкого выделяют:
По степени компенсации дыхательных и гемодинамических расстройств, сопровождающих спонтанный пневмоторакс, определены три фазы патологических изменений: фаза стойкой компенсации, фаза неустойчивой компенсации и фаза декомпенсации (недостаточной компенсации).
Симптомы спонтанного пневмоторакса
По характеру клинической симптоматики различают типичный вариант спонтанного пневмоторакса и латентный (стертый) вариант. Типичная клиника спонтанного пневмоторакса может сопровождаться умеренными или бурными проявлениями.
В большинстве случаев первичный спонтанный пневмоторакс развивается внезапно, среди полного здоровья. Уже в первые минуты заболевания отмечаются острые колющие или сжимающие боли в соответствующей половине груди, остро возникшая одышка. Выраженность боли варьирует от слабо интенсивной до очень сильной. Усиление болей происходит при попытке глубокого вдоха, кашле. Болевые ощущения распространяются на шею, плечо, руку, область живота или поясницы.
В течение 24 часов болевой синдром уменьшается или полностью исчезает, даже в том случае, если спонтанный пневмоторакс не разрешается. Ощущения дыхательного дискомфорта и нехватки воздуха возникают только при физической нагрузке.
При бурных клинических проявлениях спонтанного пневмоторакса болевой приступ и одышка выражены крайне резко. Могут возникать кратковременные обморочные состояния, бледность кожи, акроцианоз, тахикардия, чувство страха и тревоги. Пациенты щадят себя: ограничивают движения, принимают положение полусидя или лежа на больном боку. Нередко развивается и прогрессирующе нарастает подкожная эмфизема, крепитация в области шеи, верхних конечностей, туловища. У пациентов с вторичным спонтанным пневмотораксом, виду ограниченности резервов сердечно-сосудистой системы, заболевание протекает тяжелее.
Осложнения
К осложненным вариантам течения спонтанного пневмоторакса относится развитие напряженного пневмоторакса, гемоторакса, реактивного плеврита, одномоментного двустороннего коллапса легких. Скопление и длительное нахождение инфицированной мокроты в коллабированном легком приводит к развитию вторичных бронхоэктазов, повторных эпизодов аспирационной пневмонии в здоровом легком, абсцессов. Осложнения спонтанного пневмоторакса развиваются в 4-5% случаев, однако они могут представлять угрозу для жизни пациентов.
Диагностика
Спонтанный пневмоторакс латентного или стертого течения необходимо дифференцировать от гигантской бронхолегочной кисты и диафрагмальной грыжи. В последнем случае дифдиагностике помогает рентгенография пищевода.
Лечение спонтанного пневмоторакса
Лечебные стандарты требуют как можно более ранней эвакуации скопившегося в полости плевры воздуха и достижения расправления легкого. Общепринятым стандартом является переход от диагностической тактики к лечебной. Таким образом, получение в процессе торакоцентеза воздуха является показанием к дренированию плевральной полости. Плевральный дренаж устанавливается во II межреберье по среднеключичной линии, после чего присоединяется к активной аспирации.
Улучшение проходимости бронхов и эвакуация вязкой мокроты облегчают задачу расправления легкого. С этой целью проводятся лечебные бронхоскопии (бронхоальвеолярный лаваж, трахеальная аспирация), ингаляции с муколитиками и бронхолитиками, дыхательная гимнастика, оксигенотерапия.
Если в течение 4-5 суток не наступает расправления легкого, переходят к хирургической тактике. Она может заключаться в торакоскопической диатермокоагуляции булл и спаек, ликвидации бронхоплевральных свищей, осуществлении химического плевродеза. При рецидивирующем спонтанном пневмотораксе, в зависимости от его причин и также состояния легочной ткани, может быть показана атипичная краевая резекция легкого, лобэктомия или даже пневмонэктомия.
Прогноз
При первичном спонтанном пневмотораксе прогноз благоприятный. Обычно удается достичь расправления легкого минимально инвазивными способами. При вторичном спонтанном пневмотораксе рецидивы заболевания развиваются у 20-50% пациентов, что диктует необходимость устранения первопричины и избрания более активной лечебной тактики. Пациенты, перенесшие спонтанный пневмоторакс, должны находиться под наблюдением торакального хирурга или пульмонолога.
Коллаборация: что это значит простыми словами (ТОП-7 примеров из моды, спорта и бизнеса)
Слово «коллаборация» стремительно ворвалось в современную русскую речь и начало звучать даже в разговорах подростков. Причем еще совсем недавно, в 2010 году в «Историческом словаре галлицизмов русского языка» указывается, что коллаборация – это сотрудничество, с пометкой «устаревшее».
И вдруг со слова стряхнули пыль времен и вернули его в активный лексикон. Что же послужило поводом для такого возрождения? Что называли коллаборацией раньше и какое значение вкладывают сегодня в это понятие? В нашей статье ответим на эти вопросы и рассмотрим примеры удачных коллабораций в разных областях деятельности.
Немного этимологии
Кто-то ошибочно предполагает, что коллаборация – это сокращенное словосочетание «коллектив лабораторий», т.к. в научном мире взаимодействие между учеными из разных учреждений и государств давно и широко распространено. Но это просто совпадение.
Коллаборация – слово, пришедшее из французского языка, в дословном переводе это работа с (кем-то), или сотрудничество.
Но до недавних пор оно имело скорее негативный смысл. Так называли предательское сотрудничество с врагом. Явление получило распространение в 40-е годы XX века, когда французское правительство Виши содействовало немецким оккупантам.
Французское слово в переводе на английский collaboration также употребляется в значениях:
В современном русском языке коллаборация – это совместная деятельность людей или организаций, которая направлена на достижение определенных взаимовыгодных результатов.
Синонимом слова можно назвать сотрудничество.
В мире коллаборации начали завоевывать популярность в начале двухтысячных в модной индустрии. Уже несколько лет наблюдается настоящий бум этого явления, которое из мира моды распространяется в другие области.
Арт-коллаборации
История коллабораций в мире моды начинается еще в 30-е годы XX века, только тогда у этого явления не было названия.
Дизайнер одежды Эльза Скиапарелли, дружившая с Сальвадором Дали, создала провокационное платье с лобстером, взяв за основу рисунка скульптуру знаменитого художника.
Выгода от такого взаимодействия была очевидна для обоих – Скиапарелли вместе с Дали привлекли внимание к себе. Сегодня такие совместные работы художников и дизайнеров или модных брендов называют арт-коллаборациями.
Корпорации привлекают известных современных, а в некоторых случаях и старинных, художников, деятелей искусства для дизайна своих изделий или для организации нетривиальных, ярких презентаций.
Мода давно претендовала на более высокий статус, стремилась стать частью высокой культуры.
Попытки соединить моду и искусство предпринимались многократно, но на новый уровень вышли в 2001 году, когда бренд Louis Vuitton создал совместную коллекцию сумок с художником-граффитистом Стивеном Спраузом.
Коллаборации с другими художниками – теперь визитная карточка бренда.
Это явление стало очень популярным и вышло за пределы мира моды.
Арт-коллаборациями славятся такие гиганты как BMW, Samsung и др.
Например, автомобильный бренд Cadillac на первом этаже своего нью-йоркского офиса создал открытое арт-пространство, где проводятся выставки, программы с участием модных дизайнеров и т.п.
Успешность такого взаимодействия бизнеса и арт-сообщества зависит от ряда факторов:
Коллаборации брендов
Первый случай сотрудничества универмага одежды с топовым дизайнером произошел еще в 1983 году в США.
Американский модельер Рой Халстон выпустил серию вещей для обычных магазинов. Но в то время ни покупатели, принявшие прохладно коллекцию, ни представители торговли, решившие, что это дискредитация высокой моды, не оценили эксперимента.
Должно было пройти целых 20 лет, прежде чем все стороны созрели для положительной оценки коллабораций.
Кооперация брендов, обслуживающих совершенно разную аудиторию, получило массовое распространение в 2004 году с первой коллаборации H&M с Карлом Лагерфельдом.
Коллекцию, созданную великим модельером для общедоступного магазина одежды, раскупили за два часа.
С тех пор участие люксовых брендов в создании капсульных коллекций для масс-маркета стало настоящим бумом в мире моды. Покупатели ждут начала продаж, на лету расхватывают все вещи линейки, позже перепродают их тем, кому ничего не досталось.
Капсульная коллекция – небольшая линейка одежды и аксессуаров, в которой все вещи хорошо сочетаются друг с другом.
Такой тандем оказался взаимовыгодным для представителей разных полюсов фэшн-индустрии.
Потребители массовой моды получили возможность прикоснуться к миру Haute Couture, магазины одежды для простых смертных увеличили продажи, а знаменитые модные дома, взявшие курс на демократизацию моды, смогли продавать свои коллекции немыслимыми для них тиражами и создавать громкий информационный повод в СМИ.
Например, дизайнер Верджил Абло, основатель марки Off-White, за очень короткую историю существования своего бренда благодаря революционным коллаборациям с известнейшими компаниями типа Nike совершил настоящий прорыв. Его марка одежды по популярности превзошла известнейшие модные дома.
Это общая тенденция. Неизвестные или же, наоборот, признанные дизайнеры кооперируются для создания ограниченных коллекций с гигантами не только модной индустрии, но и, например, спортивной (Adidas) или мебельной (IKEA) отрасли.
Совместная работа по формуле «бренд+бренд» сейчас на пике популярности, причем, взаимодействуют не только компании, занимающие разные ценовые или даже отраслевые ниши, но и конкуренты, находящиеся в одном сегменте.
Такие тандемы обогащают мир моды уникальными вещами, комбинируя свои достижения, совмещая разные идеи и стили.
Например, бренд высокотехнологичной одежды Стон Айленд (Stone Island) организовывал коллаборации со спортивной маркой Адидас, создав кроссовки, с дизайнерским бюро Zanotta, сделав кресло-мешок, напоминающий их куртку.
Бренд для скейтеров Supreme сам инициировал кооперацию с Stone Island для выпуска лимитированной серии спортивных костюмов.
Апофеоз происходящего бума коллабораций пришелся на коллекцию весна-лето 2017 грузинского дизайнера Демны Гвасалия.
Она полностью была составлена из вещей других брендов, которые модельер немного видоизменил. Теперь такой формат нельзя назвать плагиатом, т.к. изначально было объявлено о том, что это коллаборации.
Сотрудничество брендов со знаменитостями
Тренд создания коллабораций с селебрити разного уровня известности тоже стал набирать популярность в начале XXI века.
Слава очень хорошо продается, звезды притягивают внимание к маркам, использующим их имя в создании коллекций. Сейчас уже никого не удивляют актрисы-парфюмеры, певицы-дизайнеры одежды или спортсмены, создающие свою линейку обуви.
Иногда такие коллаборации оказываются настолько продуктивными, что перерастают из разовых акций в долгосрочное сотрудничество.
Некоторые звезды так поднимают продажи маркам, с которыми взаимодействуют, что за них начинается нешуточная борьба среди именитых брендов. Например, певица Рианна создает удивительно удачные коллаборации с модными домами и косметическими марками, принося своим партнерам внушительные прибыли. Ее талант, креативность и армия фанатов способствуют такой успешности.
Часто от звезд требуется не столько сотрудничество и прямое участие в создании коллекций, сколько простое продвижение марки – важно только звучное имя на лейбле и реклама с известным персонажем. Сама знаменитость в реальности может вообще не иметь отношения к созданию продукта, который представляется как совместное творчество.
Тренд на совместную работу в разных областях деятельности
Бум коллабораций в фэшн-сообществе не остался незамеченным и в других сферах деятельности.
Наука
В мире ученых подобные взаимополезные проекты давно осуществляются между исследовательскими группами различных организаций и государств.
Часто это обусловлено наличием узких специалистов и оборудования в одном месте и ученых, которым необходимы их исследования, в другом.
Так возникают международные или межвузовские коллаборации, результатом которых становятся научные открытия.
Это взаимодействие людей науки настолько ценно, что на подобные совместные проекты выдаются общие гранты, и даже в условиях политических разногласий научные международные коллаборации стараются не трогать.
Искусство
В мире искусства коллаборации также давно и прочно занимают свою нишу.
Совместное творчество музыкантов, театральных деятелей, художников – эти проекты хорошо принимает публика, они становятся очень популярными.
Например, удачный музыкальный дуэт может вытащить из небытия старых подзабытых исполнителей или их творчество.
Коллаборации музыкантов призваны расширить аудиторию слушателей. Совместные выступления на концертах, туры, написание и исполнение общей композиции и другие способы взаимодействия помогают молодым музыкантам стать более узнаваемыми и известными.
Бизнес
Мода на коллаборации не прошла мимо бизнеса, этот метод активно внедряется в систему управления. Такое решение получило название Collab, и это совершенно иная система управления, нежели та иерархическая, к которой мы все привыкли.
В этой системе важен обмен информацией, взаимодействие. Вместо монолитных должностей у каждого появляется своя роль, которая трансформируется по ходу работы над задачей.
Помимо системы управления коллаборации возникают и во внешних связях бизнеса.
На этом поле вчерашние конкуренты, объединившись, могут разработать стратегию успешного сотрудничества. Конечно, такие объединения требуют детального анализа, не всегда они приносят ожидаемую пользу для компаний.
Коллаборации блогеров
Говоря о коллаборациях, невозможно пройти мимо блогеров разных мастей – в Инстаграмме, на YouTube и других площадках.
Задача каждого блогера – увеличить количество подписчиков, ради этого они готовы на различные ухищрения. В плане борьбы за аудиторию блогер блогеру враг, но ситуацию можно кардинально изменить, объединившись со своим конкурентом. В случае удачной «хайповой» коллаборации оба участника смогут заполучить часть подписчиков друг друга.
Например, в сети сейчас очень популярны совместные вайны Насти Ивлеевой и Иды Галич. Хотя их блоги раскручены и сами по себе, девушки все-таки создали коллаборацию и повысили свою известность. Публика ждет их совместные ролики, обсуждает, с удовольствием комментирует.
ТОП-7 примеров из моды, спорта и бизнеса
Удачных, громких коллабораций за последние годы создано немало. Назовем семерку одних из самых знаковых в разных сферах деятельности, хотя лучшие из лучших выделить невозможно в этом многообразии.
Сосудистые аномалии легочного круга кровообращения как причина кровохарканья у женщины с бронхиальной астмой
Рассмотрены причины развития легочных кровохарканий и кровотечений у больных бронхиальной астмой. Описаны легочные артериовенозные мальформации — клиническая картина, методы диагностики, подходы к лечению. Приведен клинический случай.
The reasons of pulmonary blood spitting and bleeding in patients with bronchial asthma were considered. Pulmonary arteriovenous malformations were described— clinical representation, diagnostic methods, approaches to treatment. A clinical case was given.
Кровохарканье и легочное кровотечение — респираторные симптомы, которые могут приводить к развитию грозных осложнений, таких как массивная кровопотеря, аспирационная пневмония и асфиксия пациента выделяющейся кровью. В клинической практике для разграничения этих понятий чаще всего используют количество выделившейся крови. Так, под кровохарканьем понимают откашливание из дыхательных путей отдельных прожилок крови или небольшой примеси в мокроте ярко-красного цвета. Легочное кровотечение определяют как более массивное выделение крови в чистом виде из дыхательных путей или в виде обильной примеси к мокроте (в объеме более 100 мл или 200 мл крови).
Причиной развития легочных кровохарканий и кровотечений может быть один или сочетание нескольких факторов, к которым относятся врожденная или приобретенная патология легких, сердечно-сосудистой системы, пищевода, болезни системы крови, системные заболевания, реже инфекционные и паразитарные. Нередко предрасполагающими моментами служат травма грудной клетки, резкое повышение внутригрудного давления, психоэмоциональное напряжение, нарушение целостности сосудистой стенки, применение антикоагулянтов и некоторые другие факторы.
В связи с тем что легочные кровотечения более опасны для пациента, а также учитывая сообщения описываемой нами больной о том, что при впервые возникшем кровохарканьи у нее выделилось более 200 мл кровяных сгустков, мы в статье особое внимание уделим ангиодисплазии как наиболее частой причине легочных кровотечений в настоящее время.
Структура нозологий, вызывающих легочные кровотечения, за последние десятилетия претерпела существенные изменения. Если в середине прошлого столетия большинство легочных кровотечений наблюдалось у больных деструктивными формами туберкулеза, абсцессом, гангреной и распадающимся раком легкого, то в настоящее время легочные кровотечения чаще происходят из сосудов большого круга кровообращения при хронических воспалительных заболеваниях легких.
Среди относительно нечасто встречающихся причин легочного кровотечения или кровохарканья являются пороки развития сосудов легких или ангиодисплазии, при которых могут возникать патологические соустья или открываться ранее закрытые межсосудистые шунты как в системе малого или большого кругов кровообращения, так и между двумя системами кровообращения. Менее неблагоприятной сосудистой аномалией служит шунтирование артериальной оксигенированной крови из бронхиальных артерий в легочные вены, более неблагоприятной и клинически более значимой является ангиодисплазия со сбросом венозной неоксигенированной крови в большой круг кровообращения, минуя легочную капиллярную сеть. В доступной литературе среди сосудистых заболеваний легких, приводящих к легочным кровотечениям, наибольшее внимание в настоящее время уделяется легочным артериовенозным мальформациям (ЛАВМ), чему способствует развитие и внедрение в практику различных рентгенэндоваскулярных хирургических методов лечения в противовес радикальным инвазивным вмешательствам.
ЛАВМ ранее была описана в литературе под множеством названий: доброкачественная кавернозная гемангиома легких, легочный артериовенозный ангиоматоз, гамартоматозная гемангиома легких, артериовенозная аневризма легких, артериовенозная фистула легких и другие.
Первое описание ЛАВМ у 12-летнего ребенка было дано T. Churton в 1987 г. [1]. Начиная с 1980-х гг. в литературе периодически стали публиковаться работы об успешном лечении ЛАВМ при помощи малоинвазивных рентгенэндоваскулярных методов (эмболизации) [2, 3]. В настоящее время продолжается сравнение эффективности и безопасности радикальных хирургических и малоинвазивных методов лечения ЛАВМ.
Четкие статистические данные о частоте встречаемости ЛАВМ отсутствуют, однако распространенность заболевания не превышает 2–3 случая на 100 тыс. населения. Встречаемость ЛАВМ у мужчин и женщин приблизительно одинакова. Довольно часто ЛАВМ ассоциируют с множественными геморрагическими телеангиэктазиями, наиболее известными как синдром Рандю–Ослера–Вебера: до 90% пациентов с ЛАВМ диагностируют также этот синдром [4]. Согласно статистическим данным чаще встречаются односторонние ЛАВМ. До 70% больных имеют поражения в нижних долях легких. Размер ЛАВМ колеблется в среднем от 1 до 5 см, но в ряде случаев может достигать 10 см в диаметре.
Что касается ангиодисплазий легкого, то они представляют собой патологические сообщения между артериальной и венозной системами легкого посредством прямых соустий, сети шунтов (микрофистул) или различного рода гемангиом, которые могут располагаться как в глубине легочной ткани, так и субплеврально. Величина артериовенозного сброса может колебаться от 20% до 80% от объема циркулирующей крови, что определяет степень выраженности клинических проявлений заболевания. Единичные образования менее 2 см в диаметре не сопровождаются какой-либо симптоматикой. Клинические симптомы отмечаются при множественных ангиодисплазиях или размере ЛАВМ свыше 2 см.
Классическая картина ЛАВМ включает жалобы на одышку, кровохарканье или легочные кровотечения, реже встречаются цереброваскулярные нарушения и транзиторные ишемические атаки. Превалирующее большинство пациентов предъявляет жалобы на одышку, интенсивность которой зависит от степени гипоксемии. Выраженность одышки может возрастать при переходе от горизонтального положения к вертикальному, что происходит вследствие увеличения кровотока в нижних отделах легких, где чаще локализуется ЛАВМ, и усугубления шунтирования неоксигенированной крови. При осмотре больных с ангиодисплазиями обращают на себя внимание такие проявления хронической гипоксемии, как диффузный цианоз кожных покровов, изменения формы ногтей, приобретающих вид «часовых стекол», и изменения пальцев рук и ног в виде «барабанных палочек». Одним из постоянных компенсаторных изменений крови в ответ на артериовенозное шунтирование является эритроцитоз или полицитемия и повышение уровня гемоглобина.
Достоверная диагностика ЛАВМ возможна уже при рентгенологическом исследовании органов грудной клетки. Для данной ангиодисплазии характерно усиление сосудистого рисунка в прикорневых зонах, а также обнаружение патологической тени, локализующейся главным образом в периферических отделах нижних долей легких. Характерным признаком является связь дополнительной тени с корнем легкого, что делает ее похожей на комету. Однако далеко не всегда обзорная рентгенограмма может выявить ЛАВМ. С большей точностью определить количество и анатомические характеристики аномалий легочных сосудов позволяет спиральная компьютерная томография высокого разрешения с внутривенным контрастным усилением.
Наиболее точными и информативными методами исследования при ангиодисплазии легких являются контрастные исследования: ангиопульмонография и бронхиальная артериография, позволяющие не только определить число, размер и диаметр артерий, вовлеченных в процесс, но и напрямую измерить давление и исследовать газовый состав крови того или иного кругов кровообращения. Избежать инвазивных методов исследования, особенно при невозможности их проведения, может позволить тест с микропузырьками (bubble-test) — одна из простых и доступных методик контрастной эхокардиографии, использующейся в современной кардиологии для оценки право-левых сбросов крови при пороках сердца, однако по информативности сильно уступающая инвазивным исследованиям [5]. Несмотря на этот метод диагностики, неоспоримым считается тот факт, что все пациенты с ЛАВМ должны быть прооперированы — либо радикально, либо малоинвазивно. Обе лечебные тактики позволяют ликвидировать межсосудистые шунты и предовтратить развитие грозных осложнений. Отказ больного от оперативного лечения сопряжен с высоким риском летального исхода и ведет к быстрому прогрессированию заболевания с развитием тяжелых тромбоэмболических осложнений или легочных кровотечений.
К радикальному методу лечения сосудистых аномалий легких относят открытую операцию в объеме пульмонэктомии или резекции легкого в пределах анатомических границ поражения. Менее инвазивными способами лечения ангиодисплазий легких служат рентгенэндоваскулярные методы лечения. В доступной литературе продолжается обсуждение преимуществ той или иной оперативной тактики.
До середины прошлого века только хирургическое лечение данной патологии рассматривалось как единственная эффективная и безопасная тактика ведения больного при ограниченных формах ангиодисплазий, в частности ЛАВМ. Открытая операция показана пациентам с большими центрально расположенными сосудистыми образованиями, с короткими приводящими артериями, с субплеврально расположенными образованиями, которые могут разорваться, а также при продолжающемся массивном легочном кровотечении. Вероятность рецидива при инвазивном лечении не превышает 2% [6].
В последние три десятилетия достойной альтернативой открытой операции у больных с ЛАВМ, межсосудистыми шунтами и фистулами становится рентгеноэндоваскулярная окклюзия легочных артериальных сосудов, вовлеченных в патологический процесс. Этот метод менее инвазивный, при необходимости его можно использовать повторно. Для ангиографической окклюзии сосудистой аномалии в качестве эмболизирующего материала используют различного типа материал: съемные баллончики (впервые в 1977 г. описал W. Porstmann), металлические спирали С. Gianturco (впервые использованы в 1975 г.), ивалон (поливинил) и другие. Убедительных преимуществ использования баллона или спиралей для окклюзии сосудов не отмечено ни одним из авторов. Выбор определяется диаметром и числом артерий, которые предстоит окклюзировать.
После лечения все пациенты подлежат динамическому наблюдению в течение ближайших нескольких лет в связи с возможным рецидивированием легочных ангиодисплазий, особенно при сохраняющихся патогенетических факторах. По сравнению с открытой операцией после рентгеноэндоваскулярной окклюзии сосудистой аномалии риск рецидива, к сожалению, выше, в связи с чем наряду с ежегодной рентгенографией органов грудной клетки и пульсоксиметрией требуется также динамический контроль картины компьютерной томографии. В то же время пациенты с ЛАВМ, прошедшие резекцию легкого, не требуют столь сложного послеоперационного наблюдения.
Ниже приводим клиническое наблюдение, в котором отражена сложность дифференциальной диагностики легочного кровотечения/кровохарканья и возможности рентгеноэндоваскулярных методов лечения ангиодисплазии легких.
Пациентка И., 56 лет, поступила в терапевтическое отделение ФТК УКБ № 1 Первого МГМУ им. И. М. Сеченова 07.09.2015.
При поступлении предъявляла жалобы на кашель с отделением небольшого количества мокроты слизистого характера, свистящее дыхание, одышку при умеренной физической нагрузке, общую слабость, потливость.
Из анамнеза жизни известно, что пациентка родилась в 1949 г. в Москве, росла и развивалась соответственно возрасту, получила среднее специальное образование по профессии «парикмахер». Однако, работая парикмахером, при частом контакте с красками для волос, лаками начинали беспокоить заложенность носа, приступообразный кашель, в связи с чем сменила вид деятельности и в настоящее время работает кассиром в театре. Из семейного анамнеза известно, что отец умер в 56 от рака гортани, мать — в 85 лет (о заболеваниях информации нет), сестра, дети — практически здоровы. Пациентка эпизодически курит, выкуривая до 3 сигарет в день (индекс курящего человека менее 5 пачек/лет), алкоголем не злоупотребляет. Из перенесенных заболеваний отмечает острый калькулезный холецистит, панкреатит, осложнившийся панкреонекрозом в 1983 г., гипертоническая болезнь с 1982 г., с максимальными подъемами уровня артериального давления до 180/100 мм рт. ст. без приема регулярной гипотензивной терапии. Гипотиреоз на протяжении 10 лет, медикаментозно компенсированный (L-тироксин 75 мкг). В 1982, 1994 гг. проведено кесарево сечение. В аллергологическом анамнезе обращает на себя внимание возникновение заложенности носа и приступообразного кашля при контакте со средствами бытовой химии и парфюмерии. При приеме антибиотиков пенициллинового ряда возникает крапивница.
Из анамнеза заболевания известно, что с детского возраста отмечает частые простудные заболевания (до 3–4 раз в год), страдает вазомоторным ринитом. Приступообразный кашель также беспокоит пациентку с детского возраста. За медицинской помощью не обращалась. С апреля текущего года появилось свистящее дыхание и одышка. 18.04.2015 г. в предутренние часы возник приступ кашля, сопровождавшийся кровохарканьем, откашливанием сгустков крови вишневого цвета, со слов больной до 200 мл. Была госпитализирована в ГКБ по месту жительства, где при обследовании на компьютерной томографии органов грудной клетки от 22.04.2015 в нижней доле левого легкого (сегменты S9–10) были выявлены сливающиеся фокусы уплотнения легочной ткани по типу «матового стекла» и единичные, более плотные перибронхиальные очаги, что было расценено как картина поствоспалительных изменений в нижней доле левого легкого, предположительно аспирационного генеза. По данным бронхоскопии выявлена локальная кровоточивость в верхнедолевом бронхе справа. Во время нахождения на стационарном лечении возникали еще два эпизода кровохарканья, купированные, как и предыдущие, внутривенным введением эпсилонаминокапроновой кислоты и приемом Дицинона. Причины кровохарканья установлены не были. В повторных анализах мокроты микобактерии туберкулеза отсутствовали. Вместе с тем по выписке домой пациентке было рекомендовано амбулаторно посетить фтизиатра, однако больная к фтизиатру не обратилась, и тщательное обследование для исключения туберкулеза как причины кровохарканья было проведено во время следующей госпитализации в ГКБ в июле 2015 г. Повторный эпизод кровохарканья возник 05.05.2015 г., купированный больной самостоятельно приемом Дицинона, эпсилонаминокапроновой кислоты и не потребовавший госпитализации.
26 июля 2015 г. в предутренние часы очередной приступ кровохарканья не удалось купировать самостоятельно, была повторно госпитализирована в ГКБ по месту жительства. По данным мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки от 10.08.2015 г. в S3 и S9 справа обызвествленный очаг до 2 мм в диаметре, немногочисленные очаги линейного и очагового фиброза в обоих легких, перибронхиальные зоны уплотнения по типу «матового стекла», сливающиеся друг с другом в базальных сегментах нижней доли левого легкого. При бронхоскопии грубых органических изменений в бронхиальном дереве не выявлено. Отмечалась лишь повышенная контактная кровоточивость слизистой верхнедолевых бронхов на фоне кашля. При сцинтиграфии легких нарушение перфузии и вентиляции легких, с преобладанием вентиляционных нарушений. Больная была тщательно обследована у фтизиатра с проведением диагностических проб, данных за туберкулез не получено. Вновь состояние с учетом данных МСКТ органов грудной клетки было расценено как поствоспалительные изменения в легких, предположительно аспирационного генеза. Повторная терапия эпсилонаминокапроновой кислотой, Дициноном оказалась успешной. Кровохарканье не рецидивировало. Причина кровохарканья по-прежнему оставалась неуточненной. В сентябре 2015 г. кашель, одышка и свистящее дыхание усилились, и пациентка, опасаясь повторения кровохарканья, обратилась в поликлиническое отделение Первой университетской клинической больницы Первого МГМУ им. И. М. Сеченова и была госпитализирована в Факультетскую терапевтическую клинику.
В биохимическом анализе крови: общий белок 74,8 г/л, альбумин 44,5 г/л, альфа2-глобулины — 6,2%, креатинин 0,7 мг/дл, глюкоза 5,0 ммоль/л, железо 17,5 мкмоль/л, K + 4,7 мэкв/л, Na + 140 мэкв/л, АЛТ 21 ед/л, АСТ 19 ед/л, ГГТ 74 ед/л.
В общем анализе мочи и кала без особенностей. Реакция кала на скрытую кровь отрицательная.
Общий анализ мокроты: характер — слизистый, лейкоциты 10–15 в поле зрения, эритроциты единичные в препарате, макрофаги — много, эпителий плоский — немного, эпителий цилиндрический — немного, спирали Куршмана — 1 в препарате, эозинофилы сплошь покрывают поля зрения.
При микробиологическом исследованим мокроты выявлена условно-патогенная флора (Haemophilus parahaemolyticus, Streptococcus sanguinis, Streptococcus oralis, Candida albicans) в диагностически незначимом титре.
На ЭКГ ритм синусовый, правильный, ЧСС 62 уд. в мин. ЭОС отклонена влево, PR 190 мсек, QRS 90 мсек, QT 394 мсек, QTc 402 мсек. Начальные признаки гипертрофии левого желудочка.
Функция внешнего дыхания (ФВД): исходно ЖЕЛ 3,00 л (117%), ОФВ1 2,73 л (114%), ОФВ1/ЖЕЛ 79%, МОС25 78%, МОС50 91%, МОС75 54%. После Беротека: ЖЕЛ 4,29 л (145%), ОФВ1 3,31 л (138%), ОФВ1/ЖЕЛ 77%, МОС25 94%, МОС50 104%, МОС75 69%.
Заключение. Нарушение вентиляции легких по обструктивному типу. Обструктивные нарушения легкой степени тяжести. Снижение скорости воздушного потока в дистальном отделе. ЖЕЛ в пределах возрастной нормы. Положительная проба с Беротеком 400 мкг (КБД 11%, +260 мл).
ФВД: исходно ЖЕЛ 3,44 л (100%), ОФВ1 2,34 л (97%), ОФВ1/ЖЕЛ 78%, МОС25 69%, МОС50 74%, МОС75 63%. После Атровента: ЖЕЛ 3,89 л (103%), ОФВ1 3,26 л (102%), ОФВ1/ЖЕЛ 83%, МОС25 92%, МОС50 81%, МОС75 78%. Заключение: нарушений вентиляции легких не выявлено. ЖЕЛ в пределах возрастной нормы. Положительная проба с Атровентом (КБД 21%, +580 мл). Таким образом, при ФВД получены данные, свидетельствующие об обратимой бронхиальной обструкции, преимущественно на уровне мелких бронхов.
С учетом жалоб пациентки на кашель с отхождением мокроты, свистящее дыхание, одышку при умеренной физической нагрузке, данных анамнеза (заложенность носа и приступообразный кашель на средства бытовой химии), данных осмотра (сухие хрипы над всей поверхностью легких), а также результатов клинико-лабораторного обследования (эозинофилы в мокроте, обратимая бронхиальная обструкция по данным ФВД с медикаментозными пробами) больной впервые был поставлен диагноз «бронхиальная астма, инфекционно-аллергическая, легкого течения» и начата терапия Онбрезом Бризхалер 150 мкг 1 вдох утром, Пульмикортом Турбухалер 200 мкг 1 вдох утром. По поводу артериальной гипертонии проводилась терапия Амлодипином 5 мг по 1 таблетке 1 раз в день с дальнейшим увеличением до 1 таблетки 2 раза в день, Индапамидом ретард 1,5 мг по 1 таблетке утром. Продолжает принимать L-тироксин 75 мкг по 1 таблетке утром. Самочувствие больной оставалось удовлетворительным, жалобы не беспокоили больную. Однако, ввиду того, что главной причиной обращения пациентки в клинику послужили эпизоды кровохарканья в анамнезе, больной был проведен тщательный поиск их причины.
С учетом того, что причины легочного кровохарканья чрезвычайно разнообразны, мы сразу анамнестически исключили существования заболеваний, сопровождающихся развитием легочных васкулитов, служащих источником кровохарканья (васкулит Вегенера, болезнь Гудпасчера и т. д.), так как у больной отсутствовали клинические проявления этих заболеваний, не было признаков активности процесса (нормальные значения СОЭ, альфа2-глобулинов, нет гематурии и т. д.).
Не выявлены изменения в свертывающей системе крови, которые также могли быть причиной кровохарканья: АЧТВ 0,93, ПТИ по Квику 119%, фибриноген 3,17 г/л, тромбиновое время 18,6 сек, FM-тест менее 40 мг/л, Д-димер 0,25 мкг/мл, ИТТ 0,98, АРТТ LA 0,94, SLA 0,99, агр. Т. АДФ 50%, агр. Т-коллаген 48%, ТЭГ (Р) 5`20« мин, ТЭГ (К) 1`40« мин, ТЭГ (МА) 55 мм, агр. Т. Ристомицин 70% — все показатели коагулограммы в пределах нормальных значений.
Осмотр ЛОР-врача исключил источник кровохарканья в верхних отделах дыхательных путей. Отмечено лишь незначительное усиление сосудистого рисунка, слизь обнаружена в передних отделах полости носа с обеих сторон, что может быть результатом вазомоторного ринита. Выявлено небольшое S-образное искривление перегородки носа, больше вправо.
Источник кровохарканья в верхних отделах желудочно-кишечного тракта также не обнаружен: при эзофагогастродуоденоскопии отмечалась лишь недостаточность кардии, поверхностный очаговый гиперпластический гастрит.
После тщательного анализа анамнеза заболевания и результатов повторных бронхоскопий, выполненных накануне в ГКБ по месту жительства, результатов лабораторно-инструментального обследования, выполненного в клинике, исключившего основные причины кровохарканья (воспалительные, инфекционно-грибковые, врожденные аномалии, пороки сердца, ТЭЛА, болезнь Рандю–Ослера, легочные васкулиты, патологию в свертывающей системе крови и т. д.), было высказано предположение о наличии у пациентки артериовенозных анастомозов в системе сосудов легочного круга кровообращения или ЛАВМ. Эту же идею поддержал и торакальный хирург, профессор В. Д. Паршин.
Больная 22 сентября 2015 г. была переведена в отделение торакальной хирургии Факультетской хирургической клиники Первого МГМУ им. И. М. Сеченова для проведения бронхиальной артериографии, где артериография и была проведена 23.09.2015 г. При артериографии бронхиальных артерий выявлены аневризматические изменения в области сосудов нижней доли правого легкого и выраженные артериовенозные анастомозы в области нижней доли левого легкого (рис. 1), что потребовало в дальнейшем проведения эндоваскулярной эмболизации этих артерий. 25 сентября 2015 г. проведена эндоваскулярная суперселективная эмболизация бронхиальных артерий (рис. 2). Послеоперационный период протекал гладко, без особенностей. 6 октября 2015 г. больная была выписана из клиники под амбулаторное наблюдение. В настоящее время больная чувствует себя хорошо, работает, эпизодов кровохарканья не наблюдается. Продолжает получать противоастматическую, антигипертензивную терапию, L-тироксин.
Литература
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва







_575.jpg)



