Материалы конгрессов и конференций
IV РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
НОВЫЕ ПОДХОДЫ К КОМБИНИРОВАННОМУ ЛЕЧЕНИЮ ОНКОЛОГИЧЕСКИХ БОЛЬНЫХ: РОЛЬ ЛУЧЕВОЙ ТЕРАПИИ, ЕЁ ДОСТИЖЕНИЯ, НЕУДАЧИ И ПЕРСПЕКТИВЫ.
Г.В. Голдобенко
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
В последние несколько десятилетий прогрессивное развитие клинической онкологии связано со становлением мультимодальной терапии, у истоков которой стояла комбинация лучевого и хирургического методов лечения.
Причём ионизирующие излучения использовались в основном у больных с неоперабельными опухолями с целью уменьшения их до размеров, при которых было бы возможно выполнение радикальной операции. К настоящему времени предоперационная лучевая терапия находит своё применение и при лечении пациентов с операбельными новообразованиями. Многочисленные клинические исследования показали, что неудачи оперативного лечения, к которым, прежде всего, можно отнести развитие местных рецидивов обусловлено рядом причин: нерадикальное удаление первичного очага из-за микроинфильтрации злокачественными клетками пограничных тканей, диссеминация опухолевых клеток по операционной ране, кровеносным и лимфатическим сосудам во время оперативного вмешательства. Для предупреждения этих неблагоприятных процессов было начато использование ионизирующих излучений с целью повышения абластики оперативных вмешательств. Их повреждающее действие ведёт к изменению биологического потенциала опухоли из-за гибели радиочувствительных, наиболее злокачественных клеточных популяций, которые обычно локализуются по периферии новообразования и в зонах их микроскопического распространения и, что особенно важно, из-за разрушения клоногенных пролиферирующих клеток снижаются имплантационные способности клеток.
Многолетний опыт применения комбинированного лечения показывает, что благоприятные изменения в полной мере реализуются только после подведения опухолевой дозы, которая была бы достаточна для разрушения опухоли с максимальным сохранением репарационных способностей нормальных тканей, принимающих участие в заживлении послеоперационных ран. Этому требованию, особенно в отношении сохранения нормальных тканей, в определенной мере отвечает доза, лежащая в пределах 40 Гр, подведённых конвенциальным режимом фракционирования. Однако, как показывает современный анализ неудач комбинированной терапии, она недостаточна в определенных клинических ситуациях.
Злокачественное новообразование: причины появления, виды и стадии развития
Существует более двухсот разновидностей онкологических заболеваний, которые могут развиваться в любой области человеческого организма. Болезнь провоцируется неконтролируемым появлением атипичных мутировавших клеток, что со временем вызывает нарушение работы отдельных органов и систем организма, а также ухудшает общее самочувствие человека.
Проявление симптомов зависит от того, где расположено злокачественное новообразование и какова стадия его развития. Основными симптомами становятся: общая слабость, ухудшение аппетита, резкая потеря веса, субфебрильная температура, чрезмерная потливость, озноб.
Лечение и шансы на полное выздоровление зависят от стадии злокачественных новообразований, их вида и реакции на различные препараты. Чтобы предотвратить появление онкологии или быстро ее обнаружить, важно знать причины болезни и первые симптомы. Если есть подозрения на злокачественное новообразование, рекомендуется обратиться за консультацией опытного врача-онколога. Наилучшую помощь оказывают в иностранных клиниках.
В Турции пациентам обеспечивается максимально эффективное лечение, быструю и точную диагностику, демократичные цены на услуги.
Причины злокачественных новообразований
Ученые определили ряд причин злокачественных новообразований, способных спровоцировать развитие рака. Для удобства их принято разделять на две большие группы: эндогенные и экзогенные.
Рассмотрим подробнее каждую из них.
Эндогенные причины злокачественных новообразований:
Экзогенные причины злокачественных новообразований:
Виды злокачественных новообразований
Злокачественное образование по строению в первую очередь зависит от тканей, в которых оно сформировалось. По этому признаку различают следующие виды злокачественных новообразований:
По принципу деления злокачественных клеток выделяют гистологические, клинические и морфологические виды опухолей.
По сложности строения бывают простые (образование из одного типа ткани) или сложные виды злокачественных новообразований. Также рак различают по органу или системе, в которых он сформировался: костей, кишечника, яичников, кожи, желудка, молочных желез, предстательной железы, шейки матки, легких и т.п.
Виды злокачественных новообразований по строению клеток, на основе которых они развиваются:
Стадии злокачественных новообразований
По степени агрессивности болезни и ее распространению по организму, различают 4 стадии злокачественных новообразований.
Рассмотрим признаки каждой из них:
Стадии злокачественных новообразований определяются после тщательного обследования и консультации врача-онколога.
Лечение онкологических заболеваний
С развитием науки клинические онкологи все больше узнают о процессах формирования злокачественных новообразований. Понимание клеточных, молекулярных и генных механизмов дает возможность разрабатывать новые средства борьбы с опухолями. Несмотря на то, что сражение идет с переменным успехом, врачам удается отвоевать больше жизней, чем раньше.
Классическая триада лечения онкологии (хирургия, лучевая и химиотерапия) пополняются новыми, направленными на опухоль и более щадящими для организма, методами. К традиционным способам терапии формируются обновленные подходы.
Лечение онкологии в зависимости от стадии заболевания

Всего выделяют пять стадий развития онкозаболеваний. В зависимости от того, на какой стадии выявлено заболевание и начато лечение, составляется план лечебных мероприятий, а также определяется прогноз.
Чем в более ранней стадии начато лечение онкологии, тем выше шансы на полное выздоровление и тем менее агрессивной и масштабной будет терапия.
0 стадия — опухоли любой локализации. Границы очага не выходят за границу эпителиального слоя клеток, из которых произошла опухоль. Такой рак при своевременном адекватном лечении можно полностью вылечить.
I стадия — рак распространяется в границах органа. Если такую опухоль вовремя выявить и удалить, то прогноз в целом благоприятный.
II стадия — практически все опухоли на этой стадии в границах органа, но с большим проникновением вглубь или больших размеров. Здесь уже прогноз зависит от вида опухоли и ее расположения.
III стадия — опухоль и дальше прогрессирует, дает метастазы в регионарные лимфоузлы, но отдаленных метастазов, как правило, еще нет. Это может дать надежду на продление жизни. Но общий прогноз зависит от целого ряда факторов: типа опухоли, ее анатомических особенностей, нарушений функции соседних органов, сопутствующих заболеваний и общего состояния пациента.
IV стадия — распространенная. Первичные очаги большого размера, часто прорастающие в соседние органы, нарушение кровоснабжения, поражение регионарных и отдаленных лимфоузлов, общая интоксикация. Для облегчения состояния проводится паллиативное и симптоматическое лечение.
В Онкологическом центре «СМ-Клиника» разработаны скрининговые программы для выявления рака на ранних доклинических стадиях. Достаточно уделять своему здоровью всего несколько часов в год, чтобы убедиться, что вашей жизни ничто не угрожает, или начать лечение онкологии как можно раньше.
Лечение рака с помощью оперативного вмешательства: от радикальных операций к органосохраняющим
Хирургические вмешательства по-прежнему остаются стандартом лечения рака с вполне удовлетворительными результатами. В этой области онкологи достигли большого мастерства.
Операции при лечении опухолевых заболеваний могут быть:
Последние достижения хирургической (в т.ч. роботизированной) техники позволяют расширить количество органосохраняющих операций, число вмешательств, которые выполняются в один этап, уменьшить послеоперационные осложнения и сократить реабилитационный период.
Кроме того, в настоящее время до 54,3% увеличилось число случаев лечения рака, когда хирургический способ использовался как самостоятельный. Особенно эффективен он при раке почки, меланоме кожи, раке щитовидной железы.
В комбинации с другими методами в РФ оперативное лечение опухолей проводится в 85% случаев. Это говорит о том, что хирургия лидирует в лечении злокачественных новообразований. Намного чаще стали использоваться эндоскопические, в том числе лапароскопические методы, которые меньше травмируют ткани, окружающие опухоль, и дают возможность сохранить орган. Конечно, специалисты, в первую очередь, оценивают индивидуальную клиническую ситуацию, стадию, распространенность и тип рака, состояние пациента. И только потом коллегиально (на онкоконсилиуме) принимают решение в пользу открытой операции или эндоскопического вмешательства.
Также доказано, что результат лечения при меланоме кожи мало зависит от того, насколько широко иссекли ткани в районе опухоли, то есть достаточно отступить всего на 1–2 см (а не до 15 см, как было принято ранее).
Изменилось отношение и к лечению рака молочной железы — от радикальной мастэктомии (полного удаления вместе с группой лимфоузлов) до органосохраняющей операции и одномоментной пластики.
Используются инструменты (например, электронож), которые помогают более строго следовать таким принципам хирургического лечения, как
Современные технологии позволяют расширить число показаний к оперативному лечению с сохранением органа и сделать более радикальными операции при локальных или метастатических злокачественных опухолях, которые раньше невозможно было прооперировать. Все это стало возможным, когда в крупных центрах, таких как Онкологический центр «СМ-Клиника», стали создаваться целые бригады специалистов (хирургов, химиотерапевтов, радиологов), которые занимаются комплексным лечением одного пациента.
Хотите мы вам перезвоним?
Лучевая терапия в лечении онкологии
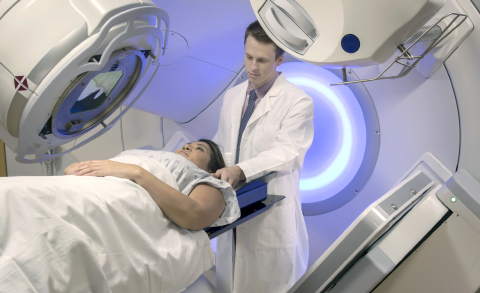
Для лучевой терапии используют ионизирующее излучение. Оно может отличаться по механизму биологического действия, проникающей способности и распределению энергии. В клинической практике чаще других применяют фотонное излучение, к которому относится:
Также используется корпускулярное излучение (от ядерных частиц). Виды: бета-излучение, позитронное излучение, альфа-частицы.
Основные источники ионизирующего излучения — это естественные и искусственные радионуклиды (радиоактивные вещества) и специальные аппараты — ускорители, генераторы нейтронов, рентгеновские аппараты.
Возможно дистанционное, контактное и внутреннее облучение, при котором радионуклиды вводятся внутривенно или через рот.
При дистанционной лучевой терапии источник излучения (в основном фотонного) удален от опухоли на 80–100 см. При контактном облучении, которое называется брахитерапия, источник находится на близком расстоянии, до 30 см, от опухолевого очага или в непосредственном контакте. Это более щадящий вид терапии. Основные виды контактного облучения: внутриполостное, внутритканевое, аппликационное (на поверхности тела).
Под действием ионизирующего излучения образуются свободные радикалы, которые повреждают клетки, также нарушается воспроизведение ДНК и деление клеток, что приводит к уничтожению опухоли. При этом есть мгновенное действие и отсроченное.
В сочетании с хирургическими методами лечения рака применяется:
Для того чтобы общая реакция организма на лучевую терапию была менее выраженной, современные методики дополняются способами визуализации опухоли, в том числе 3D, а также фиксирующими приспособлениями. Это помогает наиболее точно воздействовать на опухоль.
Лучевая терапия хорошо сочетается и с лекарственными методами лечения онкологии.
Химиотерапия
Химиотерапевтические методы лечения рака (и монотерапия, и комбинированное применение средств) связаны с действием лекарственных препаратов на опухолевые клетки в определенных фазах их развития.
В зависимости от места химиотерапии в лечении опухолевого заболевания выделяют:
При полихимиотерапии подбираются препараты с различным механизмом действия.
Возможна цитостатическая терапия, когда препарат замедляет развитие опухоли и цитотоксическая, если раковые клетки уничтожаются.
В зависимости от того, на каком этапе и каким образом химиопрепарат действует на клетку, его относят к той или иной группе:
Гормонотерапия при лечении онкологии
Одним из направлений химиотерапии является терапия гормонами, которую еще называют эндокринотерапия. Дело в том, что отдельные опухоли растут из-за гормональной стимуляции, поэтому удалив источник гормонов, можно остановить развитие злокачественного процесса. При этом такого воздействия можно добиться хирургическим путем (удаление органа, в котором синтезируются гормоны), с помощью лучевой терапии и введением лекарственных препаратов (гормонов и антигормонов).
Главная цель введения гормонов — это блокировка патологических сигналов.
Иммунотерапия
Один из самых прогрессивных методов лечения онкозаболеваний, который позволяет действовать на раковые клетки высокоспецифическими механизмами. Применяется в комбинации с другими способами терапии.
Иммунотерапия дает возможность организму сформировать иммунный ответ на опухоль, проявить цитотоксическое действие, а также повысить иммунную защиту.
Применяются следующие группы препаратов:
Таргетная терапия
Это новый метод лечения онкологии и метастазов. Он призван действовать только на определенные мишени. Это могут быть рецепторы гормонов, гены, ферменты. Также происходит повреждение структур, которые питают опухоль, или выключение внутриклеточных обменных процессов за счет нарушений в цепочке биохимических реакций.
В настоящее время применяется для лечения устойчивых к терапии видов рака, может значительно повысить эффект от лечения в сочетании с химиотерапией. С препаратами для таргетной терапии возможно лечение даже запущенных стадий.
Доказана эффективность для лечения рака молочной железы, рака легкого, меланомы и других.
Лечение онкологических заболеваний можно пройти в Онкоцентре «СМ-Клиника»
В Онкологическом центре «СМ-Клиника» есть все возможности для комплексного лечения опухолевых заболеваний различных видов и локализаций. Над планом лечения каждого пациента работает целая команда специалистов из различных областей.
Под контролем онкологов проходит не только терапия опухоли, но и лечение сопутствующих заболеваний, профилактика и уменьшение побочных эффектов, а также полный курс реабилитационных мероприятий.
Отдаленные эффекты комбинированного лечения злокачественных опухолей с интраоперационной лучевой терапией:
поздние осложнения, метахронные новообразования
ФГБУ МРНЦ, Обнинск, Россия
Цель: изучить отдаленные эффекты комбинированного лечения с интраоперационной лучевой терапией (ИОЛТ) и оценить возможный вклад ИОЛТ в их развитие.
Материал и методы. 232 больным раком желудка (78 больных), толстой кишки (74), молочной железы (61) и почки (19) проведено комбинированное лечение с ИОЛТ. 174 пациента прослежены более 3 лет и 142 – более 5 лет. Методики лечения существенно различались в зависимости от локализации, размеров, морфологии и стадии опухоли. У большинства больных применяли различные методики неоадъювантной и/или адъювантной терапии. Отдаленные результаты лечения больных, получивших ИОЛТ, сравнивали с больными, леченными по сходной схеме без ИОЛТ в рамках рандомизированных исследований.
Результаты. Поздними считали осложнения, развившиеся через 3 и более мес. после лечения. Различные патологические состояния в эти сроки имели место более чем у половины больных. Однако часть из них не связаны с лечением: воспалительные заболевания, прогрессирование опухоли и т.д., которые зачастую выглядели как токсические проявления. В целом, количество и структура поздних осложнений лечения были сравнимы в группах больных с и без ИОЛТ. Поздние (более 5 лет после лечения) рецидивы были выявлены только у 3 больных, у всех были отдаленные метастазы, диагностированные через 77-86 мес. после лечения. Метахронные первичные опухоли были выявлены у 4 (5%) больных раком желудка, леченных с ИОЛТ, и у 2 (4%) больных в контрольной хирургической группе. У всех были опухоли различных отделов желудочно-кишечного тракта и поджелудочной железы. Еще более часто полинеоплазии развивались у больных раком толстой кишки – у 9 (12%). Интервал времени до диагностики второй опухоли варьировал от 2 до 16 лет, медиана составила 6 лет. У больных раком молочной железы и почки метахронные опухоли зарегистрированы не были. Ни одна опухоль не локализовалась в поле ИОЛТ, за исключением рака поджелудочной железы через 10 лет после лечения рака желудка.
Заключение. Различные патологические состояния после комбинированного лечения злокачественных новообразований развиваются достаточно часто, однако не все они связаны с проведенным лечением. В связи с применением многокомпонентных лечебных схем вычленить вклад ИОЛТ представляется весьма сложным. Для предотвращения развития поздних осложнений исключительно важно тщательное соблюдение техники ИОЛТ, как и всех других компонентов лечения. Суммарная очаговая доза не должна превышать пределов толерантности нормальных тканей. Поздние рецидивы достаточно редки, а частота развития метахронных новообразований высока, особенно у больных раком толстой кишки. В отдаленном после лечения периоде появление вторых опухолей представляется наиболее серьезной проблемой, особенно в случае ранних стадий.
Ключевые слова: интраоперационная лучевая терапия, поздние осложнения, метахронные новообразования.
Интраоперационная лучевая терапия (ИОЛТ) – высокотехнологичный метод лечения злокачественных новообразований. Он заключается в подведении во время оперативного вмешательства высокой дозы электронного излучения непосредственно к опухоли или зоне наиболее вероятного развития рецидива. При этом становится возможным прецизионное облучение «мишени», в т.ч. в случае глубоко расположенных опухолей, а также защита окружающих органов и тканей, что дает возможность значительно увеличить очаговую дозу и уменьшить риск развития лучевых осложнений. Оптимальным видом излучения, позволяющим реализовать преимущества ИОЛТ, является высокоэнергетическое электронное излучение. Физические характеристики электронного излучения – быстрое падение дозы на глубине и гомогенное распределение в тканях – позволяют резко снизить по сравнению с фотонным или гамма-излучением интегральную дозу, уменьшив тем самым облучение окружающих опухоль здоровых тканей и органов.
В последние годы интерес к ИОЛТ существенно возрос, что в первую очередь связано с внедрением в клиническую практику специализированных мобильных ускорителей электронов. В ведущих европейских и американских клиниках было продемонстрировано очевидное преимущество мобильных ускорителей электронов в связи с их компактностью, мобильностью, минимальными требованиями к дополнительной радиационной защите, точностью подведения аппликатора к мишени и относительно низкой стоимостью.
В отличие от практически единодушного мнения об отсутствии негативного влияния ИОЛТ на течение раннего послеоперационного периода, поздние эффекты воздействия высоких однократных доз электронного излучения в должной степени не изучены и оцениваются неоднозначно [1, 4, 5, 7]. Оценка поздних осложнений и потенциального канцерогенного эффекта является одной из важнейших задач любого исследования, включающего использование новых комбинированных методов лечения с адъювантной терапией.
В 1993-2008 гг. в МРНЦ проходили масштабные клинические исследования безопасности и эффективности ИОЛТ у больных злокачественными новообразованиями основных локализаций [4]. Непосредственные результаты, показатели выживаемости были ранее представлены в многочисленных публикациях сотрудников МРНЦ. Целью настоящей работы явилась оценка отдаленных эффектов комбинированного лечения, а также попытка выявить специфический вклад ИОЛТ в развитие поздних осложнений и метахронных опухолей.
Для проведения ИОЛТ использовали электронное излучение ускорительного комплекса «Микpотpон М». Процедура ИОЛТ включала выполнение следующих этапов: 1) ревизия, удаление первичной опухоли, лимфодиссекция; 2) установка аппликатора, ограничивающего поле облучения, выбор дозы и энергии электронного излучения; 3) транспортирование больного, укладка в каньоне ускорителя с формированием необходимой конфигурации поля облучения; 4) ИОЛТ, дистанционный визуальный и ЭКГ-контроль; 5) транспортировка больного в операционную, пластический этап операции. Объектом ИОЛТ было «ложе» опухоли и зона pегионаpного лимфогенного метастазирования. Использовали круглые и прямоугольные поля от 6 до 10 см. Однократные дозы варьировали от 10 до 20 Гp, энергия пучка электронов – от 8 до 12 МэВ. Согласно протоколам исследования, больные регулярно проходили контрольное обследование в амбулаторных условиях, а также в стационаре МРНЦ.
К поздним мы относили все осложнения, развившиеся у больных через 3 и более мес. после лечения. Для определения метахронных опухолей использовали критерии S. Warren, O. Gates [16]: 1) злокачественный характер каждой опухоли должен быть подтвержден морфологически; 2) опухоли должны быть расположены раздельно; 3) должна быть исключена возможность того, что вторая опухоль является метастазом первой. Метахронными считали опухоли, выявленные более чем через 6 мес. после диагностики первой опухоли.
Методики лечения, число больных, в т.ч. наблюдаемых более 3 и 5 лет после завершения лечения, представлены в таблице 1. Всего комбинированное лечение с ИОЛТ получили 232 больных; сроки наблюдения за 174 больными превышают 3 года, а за 142 больными – 5 лет.
Таблица 1. Методики лечения, сроки наблюдения за больными.
| Локализация опухоли | Группы | Методика лечения | Число больных | ||
|---|---|---|---|---|---|
| Всего | Наблюдаются | ||||
| более 3 лет | более 5 лет | ||||
| Рак желудка* | – | Предоперационная лучевая терапия 20-25 Гр/5 дней + операция + ИОЛТ 20 Гр | 78 | 44 | 32 |
| Рак ободочной кишки* | «Фиксированные» отделы | Предоперационная лучевая терапия 18 Гр/3 дня + операция + ИОЛТ 20 Гр | 33 | 59 | 53 |
| «Мобильные» отделы | Операция + ИОЛТ 20 Гр | 41 | |||
| Рак молочной железы** | 1-2АВ стадии (Т1-2N0-1M0), размер опухоли до 3 см, без метастазов в подмышечных лимфатических узлах | Операция (радикальная резекция молочной железы) + ИОЛТ 10 Гр + послеоперационная лучевая терапия 46-50 Гр / 5 нед. (на зоны регионарного лимфооттока) и 40 Гр/4 недели на ткань молочной железы | 22 | 60 | 51 |
| 2-3А стадии (Т1-3N1-2M0), размер опухоли более 2 см, метастазы в подмышечных лимфатических узлах | Предоперационная лучевая терапия 12 Гр/2 дня + операция (радикальная мастэктомия) + ИОЛТ 10 Гр + послеоперационная лучевая терапия 46-50 Гр / 5 нед. (на зоны регионарного лимфооттока) | 39 | |||
| Рак почки | – | Операция (нефрэктомия) + ИОЛТ 20 Гр | 19 | 11 | 6 |
* При наличии показаний больным было рекомендовано проведение адъювантной химиотерапии по месту жительства.
** Всем больным проводили химиотерапию по схеме CMF; 1 цикл в неоадъювантном и 4-7 циклов в адъювантном режиме.
Рак желудка. Комбинированное лечение с ИОЛТ было проведено 78 больным, в т.ч. 42 – в рамках рандомизированного исследования (контрольную группу составил 41 больной, получивший хирургическое лечение). В отдаленные после лечения сроки изучали функциональное и структурное состояние поджелудочной железы, печени, почек, поскольку эти органы находились в зоне воздействия всех компонентов комбинированного лечения (табл. 2, 3). Функциональное состояние печени, о котором судили на основании биохимических тестов (АЛТ, АСТ, щелочная фосфатаза, билирубин, общий белок, холестерин), у больных обеих групп не претерпевало существенных изменений в течение 1 года после лечения. Увеличение отдельных показателей у ряда больных было связано либо с клинической манифестацией метастатического поражения печени, либо с воспалительными заболеваниями панкреато-билиарной системы (холецистит, панкреатит и др.). Содержание холестерина в сыворотке крови, как показатель липидного обмена, у всех больных находилось в пределах нормальных значений. Нами также не отмечено влияния метода лечения на функцию почек. Как следует из представленных в таблице 2 данных, как экзокринная, так и эндокринная функция поджелудочной железы в сроки до 1 года после окончания лечения не различались у больных обеих групп.
Таблица 2. Показатели биохимического анализа крови у больных раком желудка в отдаленные сроки после комбинированного (1 группа) и хирургического лечения (2 группа).
| Показатели (норма) | Группы больных | Срок исследования | |||
|---|---|---|---|---|---|
| 3 мес. | 6 мес. | 9 мес. | 12 мес. | ||
| АЛТ* (0-45) | 1 | 24 (1) | 24 (1) | 20 (0) | 28 (1) |
| 2 | 15 (0) | 20 (0) | 26 (1) | 14 (0) | |
| АСТ* (0-45) | 1 | 21 (0) | 24 (0) | 21 (0) | 27 (2) |
| 2 | 20 (0) | 22 (0) | 28 (1) | 19 (0) | |
| Щелочная фосфатаза* (80-270) | 1 | 211 (2) | 227 (2) | 287 (2) | 287 (3) |
| 2 | 175 (1) | 193 (0) | 160 (0) | 186 (0) | |
| Общий билирубин* (2-20) | 1 | 11 (0) | 15 (1) | 11 (0) | 13 (2) |
| 2 | 15 (2) | 17 (2) | 21 (3) | 13 (1) | |
| Холестерин** (3,4-7,2) | 1 | 4,8 (0) | 4,7 (1) | 4,2 (0) | 4,6 (2) |
| 2. | 4,7 (0) | 4,4 (1) | 4,0 (0) | 4,6 (2) | |
| Белок** (60-80) | 1 | 68 (0) | 67 (3) | 70 (0) | 67 (3) |
| 2 | 67 (1) | 63 (1) | 72 (0) | 69 (0) | |
| Амилаза* (0-96) | 1 | 33 (0) | 33 (0) | 39 (0) | 38 (0) |
| 2 | 48 (0) | 39 (0) | 72 (1) | 50 (0) | |
| Глюкоза* (3,9-5,8) | 1 | 5,2 (3) | 5,3 (2) | 4,6 (0) | 4,8 (1) |
| 2 | 4,5 (0) | 5,0 (0) | 4,5 (0) | 5,0 (1) | |
| Мочевина* (3,3-6,7) | 1 | 4,3 (0) | 4,9 (1) | 4,0 (0) | 5,2 (1) |
| 2 | 5,0 (1) | 5,3 (2) | 5,2 (0) | 5,2 (1) | |
| Креатинин* (45-100) | 1 | 62 (0) | 65 (0) | 54 (0) | 68 (3) |
| 2 | 68 (2) | 75 (1) | 77 (1) | 67 (2) | |
* В скобках указано число больных, у которых данный показатель превышал нормальные цифры.
** В скобках указано число больных, у которых данный показатель был ниже нормальных цифр.
Таблица 3. Структурные и функциональные изменения поджелудочной железы и почек в отдаленные сроки
у больных раком желудка после комбинированного (1 группа) и хирургического (2 группа) лечения.
| Структурные и функциональные изменения | 1 группа n = 29 | 2 группа n = 26 | ||
|---|---|---|---|---|
| абс. | % | абс. | % | |
| Атрофия и фиброз паренхимы поджелудочной железы | 16 | 55 | 18 | 62 |
| Хронический панкреатит | 4 | 14 | 5 | 17 |
| Сахарный диабет | 1 | 3 | 1 | 3 |
| Хронический пиелонефрит | 2 | 7 | 4 | 14 |
| Киста правой почки | 1 | 3 | 2 | 7 |
| Конкременты левой почки | 1 | 3 | – | – |
| Аплазия левой почки | 1 | 3 | – | – |
В сроки от 5 до 10 лет после лечения были обследованы 58 больных, леченных в рамках рандомизированного исследования, по 29 из каждой группы. При анализе учитывали клиническую картину, лабораторные показатели, а также структурные изменения органов. Основными методами диагностики были: физикальное обследование, СКТ, УЗИ, радионуклидные исследования, биохимический и общий анализы крови, анализ мочи. Как следует из представленных в таблице 3 данных, при сравнении первой и второй групп была выявлена сходная картина как функциональных нарушений (хронический панкреатит, сахарный диабет), так и структурных изменений в поджелудочной железе. Последние у всех больных проявлялись явлениями атрофии и фиброза паренхимы. Интересными представляются результаты анализа функционального состояния почек. Число больных хроническим пиелонефритом во второй группе было в два раза больше, чем в первой. В то же время у одного больного первой группы была отмечена аплазия левой почки, которая, вероятнее всего, явилась конечным результатом хронического пиелонефрита. Исход хронического пиелонефрита во вторичное сморщивание почки, по-видимому, может быть связан с применением комбинированного лечения на фоне скрытого хронического заболевания, но этот вопрос нуждается в дальнейшем изучении. Частота фиброзных изменений левой почки, которая частично попадает в поле предоперационной лучевой терапии, была одинаковой в обеих группах.
Рак ободочной кишки. Комбинированное лечение с ИОЛТ было проведено 74 больным. У одного больного через три года после комбинированного лечения рака правой половины толстой кишки с ИОЛТ в дозе 20 Гр развилась стриктура правого мочеточника. Попытки стентирования, а также пластики мочеточника успеха не имели, и в последующем больному была выполнена нефрэктомия. Больной наблюдается более 10 лет без признаков рецидива. Несмотря на то, что у всех больных выделяли мочеточники, брали их на держалки и выводили из поля облучения, развитие этого осложнения мы связываем с ИОЛТ, поскольку подобные осложнения описаны и другими авторами [7]. У остальных больных при сроках наблюдения до 15 лет каких-либо поздних осложнений, которые можно было бы связать с лучевым компонентом лечения, выявлено не было.
Рак молочной железы. ИОЛТ была применена у 61 больной раком молочный железы, которые были разделены на две подгруппы в зависимости от стадии опухоли. Лечение было комплексным и включало наряду с радикальной операцией и ИОЛТ дистанционную лучевую терапию на ложе опухоли и зоны регионарного лимфооттока, послеоперационную химиотерапию. Как следует из представленных в таблице 4 данных, различий в частоте и характере поздних осложнений лечения по сравнению с группами исторического контроля, которые получили аналогичное лечение без ИОЛТ, не было.
Таблица 4. Поздние осложнения лечения у больных раком молочной железы.
| Характер осложнений | Радикальная резекция молочной железы + ИОЛТ, n = 22 абс. (%) | Радикальная резекция молочной железы без ИОЛТ, n=24 абс. (%) | Радикальная мастэктомия + ИОЛТ, n=39 абс. (%) | Радикальная мастэктомия без ИОЛТ, n=35 абс. (%) |
|---|---|---|---|---|
| Фиброз мягких тканей | 3 (13,6) | 4 (16,7) | 2 (5,1) | 3 (8,6) |
| Фиброз легкого | 1 (4,5) | – | 1 (2,6) | 2 (5,7) |
| Отек верхней конечности 1 ст. | 1 (4,5) | 2 (8,3) | 6 (15,4) | 7 (20,0) |
| Отек верхней конечности 2 ст. | 1 (4,5) | 1 (4,2) | 5 (12,8) | 5 (14,3) |
| Брахиаплексит | – | – | 1 (2,6) | 3 (8,6) |
| Тугоподвижность плечевого сустава | – | – | 2 (5,1) | 3 (8,6) |
Рак почки. Показания для проведения ИОЛТ были следующие: размеры опухоли более 7 см и/или признаки инвазии паранефральной клетчатки. В исследование было включено 19 больных (9 мужчин, 10 женщин). Из них у 17 пациентов диагноз был установлен впервые, у 2 имел место местный рецидив рака после хирургического лечения. В этой группе больных данных о развитии каких-либо поздних осложнений не получено.
Метахронные злокачественные опухоли
Метахронные злокачественные опухоли (табл. 5) были выявлены у 4 из 78 (5,1%) больных раком желудка, получивших комбинированное лечение с ИОЛТ. В контрольной хирургической группе в рамках рандомизированного исследования (41 больной) метахронные опухоли были диагностированы у двух больных (4,9%). Спектр вторых опухолей и частота их развития в группах сравнения не различались. В группе больных раком ободочной кишки вторые опухоли были диагностированы у 9 (12%) больных. В целом у больных раком желудка все вторые опухоли локализовались в различных отделах желудочно-кишечного тракта и поджелудочной железе. У больных раком ободочной кишки спектр вторых опухолей был шире, преимущественных локализаций не наблюдали. Метахронные опухоли выявляли в сроки от 2 до 16 лет, медиана составила 6 лет. Ни одна из вторых опухолей, за исключением рака поджелудочной железы, выявленного через 10 лет после лечения рака желудка, не находилась в поле ИОЛТ.
Таблица 5. Метахронные злокачественные опухоли.
| Первичная опухоль, метод лечения, число больных | Количество метахронных опухолей (%) | Локализация метахронной опухоли (интервал до диагностики, годы) |
|---|---|---|
| Рак желудка (+ИОЛТ), n = 78 | 4 (5) | Ободочная кишка – 2 (4 и 11 лет) Пищевод (5 лет) Поджелудочная железа (10 лет) |
| Рак желудка (контрольная группа, хирургическое лечение), n = 41 | 2 (4) | Поджелудочная железа (5 лет) Пищевод (16 лет) |
| Рак ободочной кишки (+ИОЛТ), n = 74 | 9 (12) | Яичники – 2 (3 и 6 лет) Предстательная железа – 2 (12 и 13 лет) Тело матки (2 года) Вульва (2 года) Поджелудочная железа (5 лет) Желудок (9 лет) Носоглотка (10 лет) |
У больных раком молочной железы и почки метахронных злокачественных опухолей выявлено не было.
В связи с применением высоких однократных доз ионизирующего излучения, имеющих радиобиологические особенности, можно было ожидать, что ИОЛТ обладает специфическим профилем токсичности, особенно поздней. Вместе с тем следует помнить, что ИОЛТ всегда является одним из компонентов комбинированного воздействия. Поэтому поздние осложнения со стороны нормальных тканей у больных, которым проведено многокомпонентное лечение, следует интерпретировать как результат воздействия многофакторных механизмов повреждения на молекулярном, клеточном и тканевом уровнях. Не следует забывать, что под маской поздних осложнений лечения могут протекать различные воспалительные и дегенеративные процессы, а также прогрессирование первичной и/или метахронных опухолей.
В конце 80-х – начале 90-х годов 20 века был опубликован ряд работ, посвященных изучению поздних осложнений в нормальных тканях в эксперименте. F. Ahmadu-Suka и соавт. [6] сообщили о результатах исследования толерантности поджелудочной железы к различным дозам ИОЛТ в сочетании с фракционированным облучением. Комплекс воздействия включал: резекцию желудка по Бильрот-2; ИОЛТ в дозах 17,5-40 Гр; послеоперационное облучение в дозе 50 Гр по 2 Гр за фракцию. Лабораторные исследования проводили до операции и регулярно повторяли в течение 5 мес. С помощью разработанных критериев количественной оценки гистологических изменений авторами была выявлена статистически достоверная зависимость между дозой ИОЛТ и степенью повреждения поджелудочной железы. Содержание нормальных ацинарных клеток в контрольной группе (85%) было достоверно выше, чем в группе облученных собак (22-32%; р<0,01). В то же время повреждение островковых клеток отсутствовало; ни у одного животного не было клинических и лабораторных признаков сахарного диабета.
H. Heijmans и соавт. [11] представили результаты изучения функции поджелудочной железы при использовании ИОЛТ в дозах 25-35 Гр. В поле ИОЛТ включали всю поджелудочную железу. У одной собаки, получившей ИОЛТ в дозе 30 Гр, через 8 мес. на аутопсии был обнаружен стеноз общего желчного протока с развитием вторичного цирроза печени. В целом при сроках наблюдения до 1 года ни у одного из животных не было отмечено признаков панкреатита, диабета или экзокринной недостаточности поджелудочной железы. Однако при использовании ИОЛТ в дозе 35 Гр отмечалось снижение уровня инсулина в крови. Авторами был сделан вывод о безопасности подведения к поджелудочной железе дозы 25 Гр. В то же время предполагалось, что использование больших доз может привести к недостаточности эндокринной функции органа в отдаленные сроки.
В ранних сообщениях ряда авторов есть указания на поздние осложнения у больных, которым проводили ИОЛТ по поводу рака желудка. Так, Y.Y. Jiang и соавт. [13] наблюдали изменения проксимальных отделов тощей кишки у 5 из 100 больных после ИОЛТ в дозе 30-40 Гр. Основными симптомами были выраженные боли в эпигастрии и рвота. На операции начальный сегмент тонкой кишки сразу за связкой Трейца имел вид «свинцовой трубки», кишечная стенка была утолщена, просвет резко сужен. Авторы расценили это осложнение как следствие попадания тонкой кишки в поле ИОЛТ и рекомендовали экранировать эту зону свинцовой пластиной. T. Inamoto и соавт. [12] сообщили о развитии у 3 из 57 больных раком желудка в поздние сроки осложнений, вероятно связанных с ИОЛТ: у одного была язва культи желудка, у двух – стриктура общего желчного протока. F.A. Calvo и соавт. [10] сообщили о развитии у 9(19%) больных, получивших ИОЛТ в дозе 15 Гр и послеоперационную лучевую терапию в дозе 46 Гр, тяжелых энтеритов, потребовавших у двух оперативного лечения в связи со стенозом просвета и перфорацией стенки кишки. С другой стороны, W.F. Sindelar и соавт. [15] отметили развитие энтеритов у 6 (24%) больных, потребовавших у двух выполнения повторных операций после проведения только послеоперационной лучевой терапии в дозе 50 Гр. Таким образом, наиболее вероятной представляется связь этого осложнения с послеоперационным облучением.
В нашем исследовании у больных раком желудка ни одно из вышеперечисленных осложнений не наблюдалось, системные исследования функции и структуры поджелудочной железы, а также ряда других органов и тканей не показали роста числа осложнений и наличия каких-либо специфических осложнений по сравнению с хирургическим лечением. На рисунке 1 представлены данные МРТ, из которых видно отсутствие изменений нормальных тканей в зоне комбинированного воздействия (поджелудочная железа, мягкие ткани забрюшинного пространства, магистральные сосуды, позвонки) у больного через 10 лет после лечения.
Рис. 1. МРТ больного Т., выполненная через 10 лет после комбинированного лечения рака желудка
(предоперационная лучевая терапия 25 Гр, гастрэктомия, ИОЛТ 20 Гр) на уровне пред- и интраоперационного
лучевого воздействия во фронтальной (а) и сагиттальной (б) плоскостях.
А.А. Завьялов и соавт. [8] подвели итоги 15-летнего опыта применения ИОЛТ в Томском НИИ онкологии. Авторы не выявили увеличения числа поздних лучевых повреждений при применении ИОЛТ по сравнению с традиционными методами лечения у больных злокачественными новообразованиями носа и околоносовых пазух, местно-распространенными формами рака щитовидной железы, раком желудка, шейки и тела матки. В то же время у 12 из 50 (24%) больных с опухолями опорно-двигательного аппарата было отмечено развитие поздних лучевых повреждений в сроки от 6 до 24 мес. при курсовой СОД 77-82 Гр (128-137 ед. ВДФ). Фиброз мягких тканей наблюдали у 8 больных, патологический перелом – у 2, неврит – у 2. Таким образом, при комбинированном лечении больных саркомами мягких тканей с применением ИОЛТ и дистанционной лучевой терапии было отмечено повышение частоты лучевых повреждений нормальных тканей, которое авторы связывали как с увеличением площади облучения при дистанционной гамма-терапии, так и с использованием суммарной дозы в очаге-мишени 77-82 Гр по изоэффекту. Комбинированное лечение по поводу сарком длинных трубчатых костей с ИОЛТ 20 Гр было проведено 52 больным, в т.ч. 16 в сочетании с дистанционной фракционированной лучевой терапией (СОД 20-44 Гр); средняя величина курсовой дозы смешанного облучения составила 85 изоГр. В отдаленном послеоперационном периоде у 2 из 16 больных, получивших смешанное облучение, наблюдались лучевые повреждения тканей – постлучевой неврит и патологический перелом кости. Авторы отметили, что ключевым моментом при планировании лечения является правильный выбор как дозы ИОЛТ, так и дистанционной фракционированной лучевой терапии, с учетом изозффективности их воздействия на нормальные ткани. По мнению авторов, величина суммарной курсовой дозы смешанного облучения не должна превышать 60-65 изоГр (100-125 усл. ед. ВДФ) в мишени.
I. Azinovic и соавт. [4] изучили поздние эффекты комбинированного лечения с ИОЛТ у 195 больных с опухолями различных локализаций, проживших более 5 лет после лечения (медиана наблюдения составила 94 мес.). Большинство больных получили лечение по поводу сарком костей и мягких тканей (36%), опухолей желудочно-кишечного тракта (24%) и мочеполовой системы (14%). Авторы разделили больных в зависимости от интенсивности лечения на 3 группы: операция + ИОЛТ (9%); операция + ИОЛТ + дистанционная фракционированная лучевая терапия ± химиосенсибилизация (46%); операция + ИОЛТ + дистанционная фракционированная лучевая терапия ± адъювантная химиотерапия/химиолучевая терапия (45%). В целом отсутствие поздних осложнений или минимальные их проявления имели место у 50% больных, осложнения 2 степени – у 27% и 3-4 степени – у 23%. Частота и степень тяжести осложнений достоверно повышались с увеличением интенсивности лечения (р<0,001). Наиболее часто тяжелые поздние осложнения были отмечены у больных саркомами костей (28 из 46 больных; 60%), намного реже – у больных раком легкого (0%) и желудочно-кишечного тракта (4%). Самым частым ИОЛТ-специфичным видом поздних осложнений авторы считают периферическую нейропатию (12%). Авторы заключили, что частота и степень тяжести поздних осложнений со стороны нормальных тканей весьма значительны, однако вклад ИОЛТ в поздние тканевые повреждения в клинических условиях, за исключением периферической нейропатии, до настоящего времени неясен и требует дальнейшего изучения.
Е.М. Слонимская и соавт. [14] оценили эффективность органосохраняющего лечения 218 больных раком молочной железы с применением интраоперационной (10 Гр) и послеоперационной дистанционной фракционированной (СОД 45-48 Гр) лучевой терапии. Авторы оценили у 93% больных косметический эффект как «отличный» и «хороший», у 7% – как «удовлетворительный».
Полученные нами данные также подтверждают относительную безопасность проведения комбинированного лечения с ИОЛТ в дозе 10-20 Гр больным с опухолями желудочно-кишечного тракта, молочной железы, почки.
Таким образом, тяжелые поздние осложнения в основном отмечаются у больных, получавших сочетанную интра- и послеоперационную лучевую терапию, химиотерапию. Развитие их, очевидно, связано с превышением толерантности нормальных тканей в зоне лучевого воздействия. Следует отметить, что по результатам экспериментальных исследований на крупных лабораторных животных использованный уровень доз был расценен как безопасный. Тем не менее, полученные нами данные показали отсутствие роста числа и тяжести поздних осложнений лечения при применении ИОЛТ. Полученные результаты мы связываем с применением оригинальных технических средств, соблюдением методики и техники выполнения всех компонентов комбинированного лечения, применением доз лучевого воздействия, не превышающих толерантность здоровых тканей.
По данным популяционных исследований, число больных с полинеоплазиями постоянно увеличивается и становится одной из наиболее серьезных проблем современной онкологии. С другой стороны, эта тема в мировой и особенно отечественной литературе освещена крайне скудно, в т.ч. и в отношении ИОЛТ. Механизмы развития вторых опухолей могут существенно различаться: генетические нарушения, канцерогенный эффект внешней среды, индукция проводимым лечением и т.д. Для отнесения второй опухоли к радиоиндуцированной B.E. Powers и соавт. [14] предложили следующие критерии: опухоль должна локализоваться в пределах поля облучения, необходимо ее морфологическое подтверждение и достаточно длительный латентный период от лечения до ее появления, а также низкая вероятность ее спонтанного образования.
Подводя итоги серии экспериментальных исследований в Национальном институте рака США, M. Barnes и соавт. [9] сообщили о развитии 9 опухолей в пределах поля ИОЛТ у 8 (23%) животных. Две из них представляли собой доброкачественные опухоли периферических нервов, 7 – злокачественные опухоли из костной, хрящевой и мышечной тканей. Опухоли обнаруживали через 24-58 мес. (в среднем – 40 мес.) после ИОЛТ в дозах 25-35 Гр. Из сообщения неясно, получали животные только ИОЛТ или в сочетании с фракционированным облучением. B.E. Powers и соавт. [14] сообщили о развитии в поле ИОЛТ опухолей поясничного отдела позвоночника, имевших строение низкодифференцированной остеогенной саркомы, у 8 из 67 (12%) собак через 4-5 лет после воздействия. Только в одном случае было отмечено развитие опухоли после ИОЛТ в дозе 47,5 Гр; остальные 7 опухолей развились в группе из 27 животных, получивших комбинацию ИОЛТ с фракционированным облучением. Причем только в одном случае опухоль была выявлена при использовании ИОЛТ в дозе 25 Гр, остальные – 32,5-47,5 Гр. Ни у одного животного контрольной группы, получивших только фракционированное облучение, опухолей обнаружено не было.
Клинических исследований, посвященных развитию полинеоплазий после ИОЛТ, в мировой литературе крайне мало. I. Azinovic и соавт. [7] сообщили о развитии метахронных злокачественных новообразований у 8 (4%) из 195 больных, получивших комбинированное лечение с ИОЛТ, в сроки 15-85 мес. (медиана – 56,5 мес.). Ни одна из вторых опухолей не была в поле ИОЛТ, три находились на границе с полем дистанционной фракционированной лучевой терапии.
M.H. Aziz и соавт. [8] проанализировали риск развития индуцированных метахронных опухолей у больных раком молочной железы при применении ИОЛТ низкоэнергетическим рентгеновским излучением (50 кВ, 20 Гр) с помощью аппарата «Intrabeam» по сравнению с другими методиками лучевой терапии – ускоренным парциальным облучением (СОД 34 Гр / РОД 3,4 Гр / 2 раза в день в течение 5 дней) и традиционным фракционированным облучением (СОД 50 Гр / 2 Гр за фракцию). Авторы оценили соотношение средней и максимальной очаговых доз, а также объемов облучения в критических органах, к которым были отнесены пораженная молочная железа, вторая молочная железа, оба легких, сердце и позвоночник. Авторы показали, что риск развития метахронной радиоиндуцированной опухоли достоверно ниже в случае применения ИОЛТ по сравнению с другими методиками лучевой терапии.
Таким образом, высокая частота развития метахронных опухолей в поле ИОЛТ, преимущественно сарком, в экспериментальных исследованиях не нашла подтверждения в клинике. До настоящего времени в клинических публикациях нет ни одного достоверного сообщения об индуцированной опухоли в поле ИОЛТ. Более того, результаты M.H. Aziz и соавт. [8] в отношении рака молочной железы позволяют предположить уменьшение риска развития вторых опухолей при применении ИОЛТ вместо фракционированного облучения. Показанные в данной работе достаточно высокие цифры развития вторых опухолей у больных с опухолями желудочно-кишечного тракта лишь отражают современную глобальную тенденцию к постоянному росту частоты полинеоплазий [2].
Значительный собственный клинический опыт и анализ мировой литературы позволяет нам заключить, что включение ИОЛТ в состав комбинированного лечения злокачественных новообразований основных локализаций не приводит к росту числа и тяжести поздних осложнений. Для достижения подобных результатов необходимо строгое соблюдение методических и технических подходов как к ИОЛТ, так и к остальным компонентам лечения. Суммарная доза при сочетанном облучении не должна превышать толерантность нормальных тканей. Единственным ИОЛТ-специфичным осложнением является периферическая нейропатия, профилактике и лечению которой следует уделить серьезное внимание. Не получены также достоверные данные об индуцирующем влиянии ИОЛТ на развитие метахронных опухолей у человека. Тем не менее, нам хотелось бы подчеркнуть, что частота развития полинеоплазий, независимо от метода лечения, имеет постоянную тенденцию к росту. Клиническое значение вторых опухолей исключительно велико, особенно в случае ранних стадий и благоприятного прогноза при лечении первой опухоли.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.




