Компактизация хромосом
Вы будете перенаправлены на Автор24
Компактизация ДНК – это процесс «укладки» ДНК внутри хромосом.
Хромосомы – это ядерные структуры, которые содержат в себе наследственную информацию.
Система компактизации хромосом
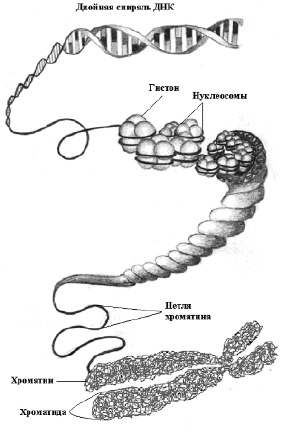
Хромосомы состоят из двух плачей, которые соединяются хроматидой. Суммарная длина ДНК внутри клеток человека составляет приблизительно 2 метра. Диаметр ядра клетки составляет приблизительно 7 мкм. При учете того факта, что каждая хромосома представлена отдельной молекулой ДНК, то компактизация ДНК составляет более шести тысяч раз. Подобная укладка происходит в несколько уровней:
Готовые работы на аналогичную тему
Средний размер таких розеток достигает 100 – 150 нм. Розетки фибрилл хроматина называются хромомерами. Каждый такой хромомер состоит из нескольких нуклеосом или петель, которые связываются в одном центре. Хромомеры связываются друг с другом и некоторыми участками нуклеосомного хроматина. Это обеспечивает так называемую структурную компактизацию хроматина и организует функциональные хромосомные единицы, а именно репликоны и гены, транскрибируемые в пределах хроматина.
Более плотная компактизация ДНК на хроматидном и хромосомном уровне достигается за счет дальнейшей компактизации хромомеров и наблюдается в делящихся клетках с плотными хромосомами. Такая компактизация хромосом становится видна даже при использовании светового микроскопа в виде отдельных образований. Если клетка не делится, то хромосомы деспирализуются и между ними не видно границ. Диффузный материал таких хромосом называется хроматином.
Разновидности компактизации хромосом
Электронная микрофотография растительной клетки показывает темные и плотные участки гетерохроматина и светлые части эухроматина. Эухроматин активизируется при транскрипции, гетерохроматин составляет своего рода молчащие участки ДНК. Также выделяют теломеры и центромеры или структурные элементы хромосом, в которых не существует генов. Центромеры и теломеры входят в состав облигатного (обязательного) гетерохроматина. Факультативный гетерохроматин образуется в клетке без обязательной основы.
Резюмируя сказанное, можно выделить несколько уровней компактизации хромосом:
Таким образом, сохраняя преемственность в ряду поколений, хроматин меняет собственную организацию. В интерфазе он выделяется в виде глыбок, которые рассеяны в нуклеоплазме ядра. Если клетка переходит в митоз, в частности в метафазе, то хроматин приобретает вид интенсивно окрашенных телец – хромосом. Эти формы существования расцениваются как два полярных варианта структурной организации хроматина.
Они связываются в митотическом цикле своеобразными взаимными переходами. В пользу подобного мнения свидетельствуют эмпирические данные, полученные в результате применения метода электронной микроскопии. В основе метафазной и интерфазной структуры лежит элементарная нитчатая структура белка.
Неодинаковая степень компактизации хромосом имеет колоссальное функциональное значение. Различают конститутивный (структурный) и факультативный гетерохроматин. Скорее всего, его роль заключается в поддержании общей структуры ядра и прикреплении хроматина к ядерной оболочке, а также регуляции активности некоторых клеточных структур.
Совокупность всех хромосом называется кариотипом, который включает в себя все молекулы ДНК, содержащие сведения о всем многообразии признаков организма. Изменение числа хромосом в кариотипе человека может привести к различным заболеваниям. Наиболее частым хромосомным заболеванием у человека является синдром Дауна.
Научная электронная библиотека
Юров И. Ю., Ворсанова С. Г., Воинова В. Ю., Чурносов М. И., Юров Ю. Б.,
3.1. Геном человека и структурная организация хромосом
Как уже сказано выше, данные о структуре, размерах и количестве митотических хромосом в клеточном ядре определяются как кариотип. Морфологическое строение хромосом на всех уровнях организации (молекулярном, микроскопическом и субмикроскопическом) определяется упаковкой нитей ДНК, организующих хромосому. На микроскопическом уровне нити ДНК формируют спирализованные хромонемы митотических хромосом. Упаковка хромонем по длине хромосом неравномерна. В них закономерно дифференцируются участки с резко выраженной и резко сниженной степенью спирализации хромонем. Последние формируют хромосомные перетяжки. Важным элементом структуры хромосом является первичная перетяжка, в участке которой расположена центромера. Она делит хромосому на два плеча – короткое (р) и длинное (q).
Структура хромосом претерпевает значительные изменения в ходе клеточного деления (клеточного цикла) и, следовательно, не является постоянной. Хромосомы интерфазных ядер (интерфазные хромосомы) в отличие от метафазных хромосом (см раздел, посвященный делению клетки) представляют собой более расправленные и диффузные клеточные структуры. Интерфазные хромосомы содержат одну хроматиду, в составе которой имеется одна двуспиральная молекула ДНК, в то время как метафазные хромосомы образованы двумя хроматидами и двумя молекулами ДНК. Хромосома, как функционирующая клеточная органелла, должна содержать минимум три типа последовательностей ДНК, формирующих её структурные компоненты: центромеру, теломеры и участок начала репликации ДНК.
Индивидуальные хромосомы содержат одну протяжённую двуспиральную молекулу ДНК диаметром 2 нм, которая претерпевает несколько уровней упаковки, формируя хроматин или ДНК-белковый комплекс (дезоксирибонуклеопротеид – ДНП). Элементарной дискретной единицей упаковки хроматина является нуклеосома. Каждая нуклеосома имеет вид глобулы и состоит из четырех пар гистоновых белков Н2А, Н2В, Н3 и Н4, содержащих по 102–135 аминокислотных остатков. Вокруг гистоновой глобулы диаметром 10 нм (октамера) располагается молекула двуспиральной ДНК длиной 146 пн (или 68 нм), образуя виток в 1,75 оборота. Соседние нуклеосомы соединяются так называемой «спейсерной» ДНК длиной около 20 нм, образуя структуры в виде «бус на нитке». На следующем этапе компактизации 10-нанометровые нуклеосомы образуют фибриллы хроматина диаметром 30 нм (в каждом витке примерно 6 нуклеосом), которые образуют большие петли. На стадии метафазы степень компактизации достигает 1 на 10000 от первоначальной длины хромосомной ДНК. Петли 30-нанометровых фибрилл хроматина содержат 20–100 тысяч пн. ДНК на каждой петле прикрепляется к осевой структуре хромосомы (рис. 4). Осевые компоненты метафазной хромосомы состоят из негистоновых белков.
Рис. 4. Организация ДНК
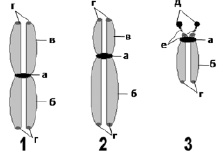
Как уже отмечалось, одним из структурных элементов хромосомы является центромера – место присоединения кинетохоров (макромолекулярных структур на белковой основе, участвующих в процессе расхождения хромосом при митотическом делении клетки), и слипания сестринских хроматид. Они также регулируют присоединение хромосом к веретену деления и направляют движение хромосом в ходе мейотического и митотического деления клетки. Хромосомы без центромеры (ацентрические фрагменты) не могут присоединяться к нитям веретена деления и теряются в ходе клеточного деления. У человека центромеры содержат особые типы повторяющихся ДНК, а также специфические «центромерные» белки, обеспечивающие сегрегацию хромосом в ходе митотического и мейотического деления клеток. В зависимости от положения центромеры в хромосоме, как уже сказано выше, она может быть метацентрической, субметацентрической и акроцентрической. В акроцентрических хромосомах довольно часто на коротких плечах видны небольшого размера хроматические тельца, так называемые спутники, и спутничные нити (рис. 5). Они содержат ядрышковый организатор – значимую структуру генома человека. Плечи некоторых хромосом человека содержат вторичные перетяжки.
Рис. 5. Схематическое изображение метафазных хромосом:
1 – метацентрическая хромосома; 2 – субметацентрическая хромосома; 3 – акроцентрическая хромосома. Видны: а – центромеры; б – длинные плечи (q); в – короткие плечи (p); г – теломерные участки; д – спутники; е – спутничные нити
Другими структурными элементами хромосом являются теломеры. Это специализированные структуры, содержащие особые типы ДНК и белки, которые образуют концевые участки хромосом. Теломеры выполняют несколько функций:
1) поддержание структурной целостности хромосомы;
2) обеспечение полной репликации концевых участков хромосомы;
3) поддержание организации хромосом в интерфазном ядре.
Теломеры хромосом человека представляют собой повторы нуклеотидной последовательности ТТАГГГ, общий размер которой варьирует от 3 до 20 тысяч пн. Стабильность теломер поддерживается с помощью фермента теломеразы, нарушение функциональной активности которой приводит к нарушению структуры хромосом и, как следствие, к клеточной гибели. Укорочение последовательностей теломер, которому противодействует теломераза, связано с процессами старения и малигнизации.
ДНК хромосом реплицируется в ходе периода синтеза ДНК клеточного цикла. Каждая хромосома содержит множество элементарных единиц репликации – репликонов, представляющих собой участки автономной репликации. Каждый репликон имеет одну точку инициации репликации, с которой начинается двунаправленный синтез ДНК (см предыдущий раздел, посвященный синтезу ДНК). Размеры репликонов могут различаться друг от друга. Репликоны у человека могут иметь большие размеры, достигая более чем 1 млн пн.
Гистоны и протамины в сперматозоидах
ОЦЕНКА УПАКОВКИ ХРОМАТИНА СПЕРМАТОЗОИДОВ
В последнее десятилетие многими исследованиями установлен факт снижения фертильности, эффективности методов ВРТ и повышения риска врожденных уродств при увеличении уровня повреждений хроматина сперматозоидов.
Термином «повреждение ДНК сперматозоидов» обозначают многие дефекты структуры хроматина, в том числе нарушения соотношения между белками гистонами и протаминами в сперматозоидах. Такие нарушения называют дефектами протаминации.
По R.Sharma, A.Agarwal // Сперматозоид хроматина: биологическое и клиническое применение при мужском бесплодии и вспомогательной репродукции / A.Zini, A.Agarwal (Ed.), 2011, Springer: 31.
Считают, что протаминация делает хроматин сперматозоидов в десятки раз более компактным, и одновременно, защищает спермальные ДНК от возможных повреждений при движении по мужскому, а затем женскому репродуктивному тракту.
После завершения упаковки хроматина на завершающих стадиях сперматогенеза большая часть ДНК ассоциирована с протаминами, только 5-15% остается связанной с гистонами. Предполагают, что эти участки после оплодотворения первыми становятся местами транскрипции и нужны для активации всего мужского генома. Но из-за того, что в этих участках ДНК остаются незащищенными протаминами, они особенно чувствительны к действию повреждающих факторов. Генотоксикантами являются – радиация, электромагнитное излучение, некоторые химические вещества (диоксид, пестициды, формальдегиды и др.).
Отмечают наличие прямой корреляции между повышенным содержанием сперматозоидов с фрагментацией ДНК в зрелых сперматозоидах и содержанием сперматозоидов с аномальной упаковкой хроматина.
Предполагают, что уменьшение доли протаминов делает хроматин более чувствительным к повреждающим воздействиям.
Дефектные сперматозоиды, содержащие неправильно упакованную ДНК, сохраняют способность к оплодотворению.
Дефицит протаминов и увеличение доли гистонов ведет к преждевременной конденсации хроматина, что является причиной сбоев в оплодотворении и развитии эмбриона.
Не до конца ясно, как взаимосвязаны аномалии хроматина с показателями стандартной спермограммы: концентрацией, подвижностью, морфологией сперматозоидов. Предполагают, что апоптоз, признаком которого является фрагментация ДНК, как связанная, так и несвязанная нарушением протоминации, служит конечным результатом различных патологических состояний и системой деградации, контролирующей сперматогенез.
Поскольку это может иметь несколько причин, оценка нарушений конденсации (упаковки) хроматина особенно рекомендуются для:
пар с историей выкидышей;
пар с необъяснимым бесплодием более 6 месяцев;
мужчин с вредными факторами образа жизни (курение, ионизирующее излучение, токсические вещества, перегревание, несбалансированное питание и др.);
мужчин с историей рака и химиотерапией;
плохом качестве эмбриона во время повторных циклов донорства яйцеклеток;
мужском идиопатическом бесплодии.
Для обнаружения нарушений упаковки хроматина в сперматозоидах используют специальные методы: окраска хромомицином А3 позволяет оценить количество протаминов, анилиновым синим – гистонов.
Рекомендуют оценивать количество сперматозоидов с низкой компактизацией хроматина по преобладанию в клетках гистонов. Принято считать, что таких сперматозоидов не должно быть больше 30%; при этом индекс нарушения, зависящий от шкальной интенсивности окраски (G0+G1+G2x2) должен быть меньше 40.
Оригинальные фото из нашей лаборатории:
синие клетки различной интенсивности окраски имеют повышенное содержание гистонов,
Последние годы для нормализации структуры хроматина сперматозоидов достаточно эффективно используются современные клеточные технологии, в т.ч. связанные с применением МСК и клеток Сертоли.
Доктор мед. наук, профессор В.А.Божедомов
Несколько цитат о значении нарушений протаминации сперматозоидов:
«…Уникальный процесс уплотнения хроматина в сперматозоиде имеет важные последствия как для развития скрининговых тестов мужского бесплодия, так и для понимания характеристик хроматина спермы, которые могут повлиять на результаты вспомогательных репродуктивных технологий. »
Palermo GD et al. Perspectives on the assessment of human sperm chromatin integrity. Fertil Steril. 2014 Dec; 102(6):1508-17.
«…В некоторых случаях неудавшееся оплодотворение после ИКСИ также ассоциировалось с дефицитом протаминов спермы и преждевременной хромосомной конденсацией…»
Tosti E, Ménézo Y. Gamete activation: basic knowledge and clinical applications.
Hum Reprod Update. 2016; 22(4): 420-39.
«…Этот тип повреждения может возникнуть у эмбрионов с нормальным комплементом хромосом и, возможно, объяснить, почему некоторые эмбрионы с нормальными кариотипами не способны обеспечить беременность у пациентов с необъяснимыми выкидышами. В целом, чем больше степень повреждения ДНК передается эмбриону отцовским геномом, тем раньше этот ущерб будет проявляться во время развития эмбриона…»
Bareh Gihan M. еt al.// Fertility and Sterility, 2016, 105 (2): 15-282
«…Дефектные сперматозоиды, содержащие поврежденную ДНК, сохраняют способность к оплодотворению. Однако с такими повреждениями ДНК связаны некоторые фенотипы бесплодия, например, необъяснимое и идиопатическое бесплодие, повторяющиеся неудачные ВМИ и ЭКО, и привычные выкидыши. …»
Sperm chromatin: biological and clinical application in male infertility and assisted reproduction / A.Zini, A.Agarwal (Ed.), 2011, Springer, 512.
«…Два объяснения есть для взаимосвязи ненормальной экспрессии протаминов и незавершенным сперматогенезом: (1) ненормальная экспрессия протаминов индуцирует системные повреждения сперматогенеза возможно посредством влияния на транскрипцию или (2) регулятор трансляции протаминов действует как «контрольная точка» в регуляции сперматогенеза и аномальная экспрессия протаминов ведет к индукции апоптотических процессов и системному ухудшению качества спермы…»
Carell DT et al.// Hum Reprod Update. 2007; 13: 313-27.
Организовать геном: запутанная история гипотез и экспериментов
Организовать геном: запутанная история гипотез и экспериментов
Всем известно, что огромные геномы организмов остаются организованными. Но как это получается?
Автор
Редакторы
Молекула ДНК очень длинная, но в клетке находится в очень компактном, «сложенном» состоянии. Как геному удается оставаться организованным и какова его трехмерная структура? О том, как ученые распутывают этот Гордиев узел с помощью новой модели петлевой организации генома, помогает ли альпинизм науке и о самом большом вопросе в биологии генома сегодня — вы узнаете в этой статье. Причем из первых рук: комментарии предоставили Илья Флямер, исследователь из Эдинбургского университета, специализирующийся на пространственной организации генома, и Леонид Мирный, биофизик из Массачусетского технологического университета и один из авторов рассматриваемой модели loop extrusion.
Геном в клетке находится в сильно уплотненном состоянии — это, пожалуй, озвучивается во всех книгах по биологии. Но ведь для этого надо сложить в клеточное ядро 2 метра человеческой ДНК без потери биологической функции [1]! В этом задействованы специальные белки, играющие важную роль в структурировании интерфазных и митотических хромосом и поддерживающие конформацию хроматина на протяжении всего клеточного цикла. Как же тогда выглядит трехмерная структура хромосомы? Как нужные гены остаются активными при такой компактизации? Честно говоря, при попытке ответить на эти вопросы воображение рисует несколько миллионов километров запутанной колючей проволоки.
Однако варианты ответов появились сразу у двух исследовательских групп [2]. Одну из них представляет биофизик Леонид Мирный, заведующий лабораторией MIT [3], а другую — Эрез Либерман Айден (Erez Lieberman Aiden), генетик из Медицинского колледжа Бейлора в Хьюстоне, Техас [4] (рис. 1). Модель назвали loop extrusion — иногда на русский язык ее переводят как «модель растущей петли» или «модель выпетливания», но общепризнанного названия пока нет.
Рисунок 1. Great minds think alike — новые гипотезы петлеобразования хроматина представлены параллельно двумя группами: Леонида Мирного из MIT (слева) и Эреза Либермана Айдена из Медицинского колледжа Бейлора в Хьюстоне (справа).
Несмотря на это, остается ответить еще на многие вопросы, в том числе подтвердить или опровергнуть роль специфических белков, названных авторами моделей. Ким Насмит (Kim Nasmyth), генетик из Оксфордского университета, известный своими работами по разделению хромосом при делении клетки, и один из героев этой статьи, cчитает это «самым большим вопросом в биологии генома на сегодня». Но, если модели окажутся верными, то, по словам знаменитого британского генетика, «это абсолютная революция в энзимологии ДНК». Помимо практического применения, они могли бы предсказать многие процессы, которые пока не удалось увидеть в эксперименте.
Ниже мы погрузимся в историю изучения пространственной структуры ДНК, во все ее взлеты, падения и петли, и вернемся к главному героя рассказа: модели loop extrusion.
Трехмерная модель генома: от азов до последних публикаций
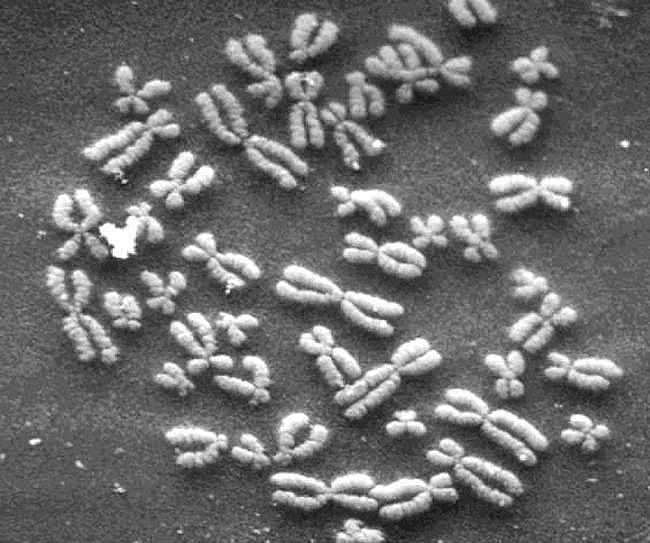
Компактизация ДНК необходима всем организмам для структурирования и передачи своего генома посредством клеточного деления [5]. Например, у эукариот хроматин образует однородные структуры — хромосомы (рис. 2). Их последующее разделение между двумя клетками должно быть очень выверенным, иначе геном дочерних клеток необратимо пострадает. (Повторить клеточный цикл и стадии митоза и мейоза помогут видео — далее рассказывается про структуру ДНК в таких стадиях клеточного цикла, как метафаза и интерфаза)
Рисунок 2. Электронная микрофотография четко различимых компактных метафазных хромосом, состоящих из двух хроматид (увеличение 2800×).
У эукариот первый уровень уплотнения геномной ДНК — так называемые «бусины на нити», когда ДНК обертывается вокруг комплекса из восьми молекул гистонов с образованием нуклеосом — структурных единиц хроматина. Уже на этом уровне доступность ДНК для ядерных белков и вовлечение в клеточные процессы снижаются — появляется возможность регулировать то, какие гены будут «работать», а какие — «молчать». Этим руководят АТФ-зависимые ферменты, ремоделирующие хроматин [6]. Кроме того, такая минимальная компактизация защищает тонкую нить ДНК от повреждения.
Про роль гистонов и про то, что такое «шаперон гистонов», можно прочитать на «Биомолекуле»: «Катится, катится к ДНК гистон» [7] и «Это FACT» [6].
Менее ясно, как складки хроматина образуют структуры более высокого порядка, к примеру, хромосомы. Кроме того, хотя после обертывания вокруг гистонов нить ДНК становится примерно в пять раз короче, все же в таком виде длина «бусин на нити» — 40 см, и чтобы поместиться в ядро размером 10 микрон, ей надо сложиться еще в 40 000 раз. «Классическая версия укладки» описывала происходящее так: «бусины на нити» составляют фибриллы диаметром 10 нм, а те в свою очередь уложены в фибриллы диаметром 30 нм, причем нуклеосомы оказываются близко друг к другу (иллюстрацию к старой модели можно увидеть, например, в «Википедии»). Однако эта версия уже опровергнута [8]: как комментирует Илья Флямер, исследователь из Эдинбургского университета, специализирующийся на пространственной организации генома, фибриллу диаметром 30 нм видели исключительно in vitro, а в живой клетке ее, по крайней мере, в классическом виде, нет. Более того, в только что вышедшей в Science статье под авторством Клода О’Ши (Clodagh O’Shea) и коллег описано, что хроматин образует гибкие цепи диаметром от 5 до 24 нм без каких-либо фибрилл (рис. 3) [9].
Рисунок 3. Ультраструктура хроматина in situ, трехмерная упаковка и организация ДНК. Хроматин — это структурно неупорядоченная цепочка диаметром от 5 до 24 нм, плотность которой при свертывании варьирует.
В любом случае, в конденсации хроматина в метафазе перед делением (наглядно на видео 1), как считается, задействованы в том числе и два структурно связанных белковых комплекса — конденсин I и II. Совместные действия конденсинов и топоизомеразы II приводят к сборке отдельных митотических хромосом, которые состоят их двух соединенных сестринских хроматид, расходящихся в анафазе. Роль топоизомеразы II в конденсации митотической хромосомы — это удаление «сцепок» внутри любой хромосомы, между сестринскими хроматидами или любой другой парой запутавшихся хромосом.
Видео 1. Уплотнение хромосом и разделение сестринских хроматид в профазе (показан процесс выпетливания)
Очевидно, что для уплотнения митотической хромосомы важно и связывание конденсина с хроматином. Однако детали механизма петлеобразования до последнего времени не прояснялись и активно исследовались учеными [5], [10].
Вейся, веревочка.
То, что ДНК образует петли, известно еще с 1970–80-х годов [11]. Так, опыты по электронной микроскопии метафазных хромосом показали, что большие петли ДНК заякорены в некоторой белковой структуре. Более того, их прикрепление к ней носит регулярный характер [12]. Такие петли — «строительные блоки хромосомы» — можно найти в геноме во время интерфазы у различных видов, например, у человека или дрожжей [13]. При транскрипции в интерфазе подобная организация позволяет регуляторным элементам находиться в непосредственной близости от тех генов, которыми они управляют. Но долгое время оставалось тайной, как же эти петли образуются.
Различные группы ученых независимо друг от друга изучали этот вопрос и разрабатывали свои модели петлевой организации хроматина [2]. Термин DNA reeling — буквально «наматывание ДНК» — предложил американец Артур Риггс (Arthur Riggs) в статье 1990 года [14]. Однако обычно автором всего концепта считают Кима Насмита из Оксфордского университета (Великобритания), который упоминался выше. Его исследовательская группа выяснила, что когезин (комплекс белков, одна из функций которого — скрепление сестринских хроматид) имеет кольцеобразную форму. Насмит в свободное время занимался альпинизмом, и, по его словам, озарение пришло во время восхождения в итальянских Альпах. Глядя на свое снаряжение и то, как веревка была пронизана сквозь карабин, он подумал, что, возможно, то же самое происходит с хромосомой и когезином, не только «обнимающим» кольцом сестринские хроматиды, но и участвующим в формировании петель, которые позволили бы митотическим хромосомам конденсироваться и разделяться. Эта гипотеза был выдвинута в статье 2001 года [15], но ее никто не заметил.
Десять лет спустя появилась математическая модель конденсации хромосом в метафазе за счет loop extrusion («выпетливания»), дополнявшая предположение Насмита. Ее автор — Джон Марко (John Marko) из Северо-западного университета (штат Иллинойс, США) — тоже, по-видимому, не знал о работе британского ученого. И Марко, и Насмит интересовались вопросом плотной упаковки хромосом для клеточного деления.
Здесь стоит упомянуть еще одного исследователя — Джоба Деккера (Job Dekker) из Медицинской школы Массачусетского университета в Вустере. Его и коллег интересовали взаимосвязи активности генов и хромосомной организации — причем в масштабе всего генома. Для изучения этих вопросов ученые из лаборатории Деккера разработали метод Hi-C [16] (видео о том, как он работает, дано в разделе про методы изучения генома), который позволяет обнаружить то, как часто какие-либо участки генома оказываются рядом, даже если они расположены далеко друг от друга на одной хромосоме или даже на разных хромосомах.
«Это единственный подход, который позволяет анализировать пространственную организацию всего генома одновременно, — комментирует Илья Флямер, специалист из лаборатории Венди Бикмор (Wendy Bickmore) Эдинбургского университета. — С помощью этого метода в лаборатории Бинга Рена (Bing Ren) обнаружили, что геном поделен на участки длиной 0,2–1 млн пар нуклеотидов с повышенной частотой контактов внутри самих себя [17]. Их назвали TADs, topologically associating domains — „топологически ассоциированные домены“». Интересно, что открытие ТАДов тоже было совершено двумя группами параллельно — другой работой руководили Джоб Деккер и Эдит Херд (Edith Heard) [18].
Только что открытые домены заинтересовали одного из главных героев нашего рассказа — Леонида Мирного, биофизика из MIT. Мирный встретился на конференции с Марко, где тот рассказывал о своей модели образования петель для плотной упаковки ДНК в метафазе. В этот момент сотрудники лаборатории Мирного и Деккера пытались построить компьютерную модель, объясняющую Hi-C-данные для плотноупакованной метафазной хромосомы. «Тогда мы поняли, что механизм, предложенный Марко — активное формирование петель молекулярными моторами, — может позволить создать ряды петель ДНК, которые мы получали в своей модели, — делится Леонид Мирный. — Опубликованная в конце 2013 года статья показала, что метафазные хромосомы в клетке состоят из таких рядов плотно уложенных петель, которые видели еще в 80-е годы».
Мирный погрузился в изучения ТАДов — и далее наш рассказ смещается из метафазы хромосом в интерфазу, то есть из той фазы клеточного цикла, когда происходит деление клетки, в фазу роста клетки и синтеза белков. Как ученый рассказал «Биомолекуле», он с коллегами пытался объяснить образование ТАДов с помощью компьютерного моделирования: «В 2014 году сотрудники нашей лаборатории Максим Имакаев и Джеф Фюденберг занимались поиском модели формирования ТАДов. Они решили проверить, нет ли и в интерфазе молекулярных моторов, подобных тем, что упаковывают ДНК в плотные метафазные хромосомы. Эта гипотеза получила название model of loop extrusion. Как оказалось, такой механизм возникновения доменов — рост петель за счет активности молекулярных моторов и их остановка на границах доменов — идеально воспроизводила многие данные, полученные с помощью Hi-C. Физический же акт формирования петель хорошо организовывал локальные домены. Параллельно другой сотрудник моей лаборатории, Антон Голобородько в сотрудничестве с Марко показал, что в компьютерных моделях молекулярные моторы, создающие петли (видео 2), действительно могут формировать плотные и длинные метафазные хромосомы (видео 3), и при помощи топоизомеразы II разделять сестринские хромосомы (видео 4), как и предполагал Насмит».
Видео 2. Введение в модель loop extrusion
Видео 3. Формирование одиночной метафазной хромосомы
Видео 4. Сегрегация сестринских хроматид
Итак, в мае 2015 года Мирный рассказывает о своей работе на конференции в Институте Вейцмана (Weizmann Institute of Science) в Израиле, где встретились все ведущие ученые из этой области, включая Эреза Либермана Айдена, Эдит Херд и других героев этой истории. В августе того же года статья Мирного и коллег нашла своего читателя на сайте bioRxiv в виде препринта, а в 2016 году была опубликована в Cell Reports [3]. Главной загадкой было и остается то, что же это за моторы, которые растят петли, и как они это делают. Как предполагалось в тот момент, когезин играл свою роль в удержании сестринских хромосом, скорее, как карабин Насмита, чем как мотор.
Лаборатория Мирного же выдвинула гипотезу, что когезин играет главную роль в создании петель в интерфазе как мотор, способный наращивать петли, когда хромосомы «распущены». Конденсин же, как оговаривалось в совсем недавней статье Деккера и Мирного [10], выполнял ту же функцию во время деления клеток при плотной конденсации хромосом.
Новая модель loop extrusion объясняет физическое взаимодействие частей генома, наблюдаемое в экспериментах: и регуляцию экспрессии генов, и многие аспекты развития клеток и различных болезней. Это достигается за счет способности новой гипотезы показывать, как ДНК может образовывать петли с помощью специальных молекулярных машин. Такой метод компактизации генома не только придает форму и структуру хромосомам, но и сближает нужные участки ДНК друг с другом.
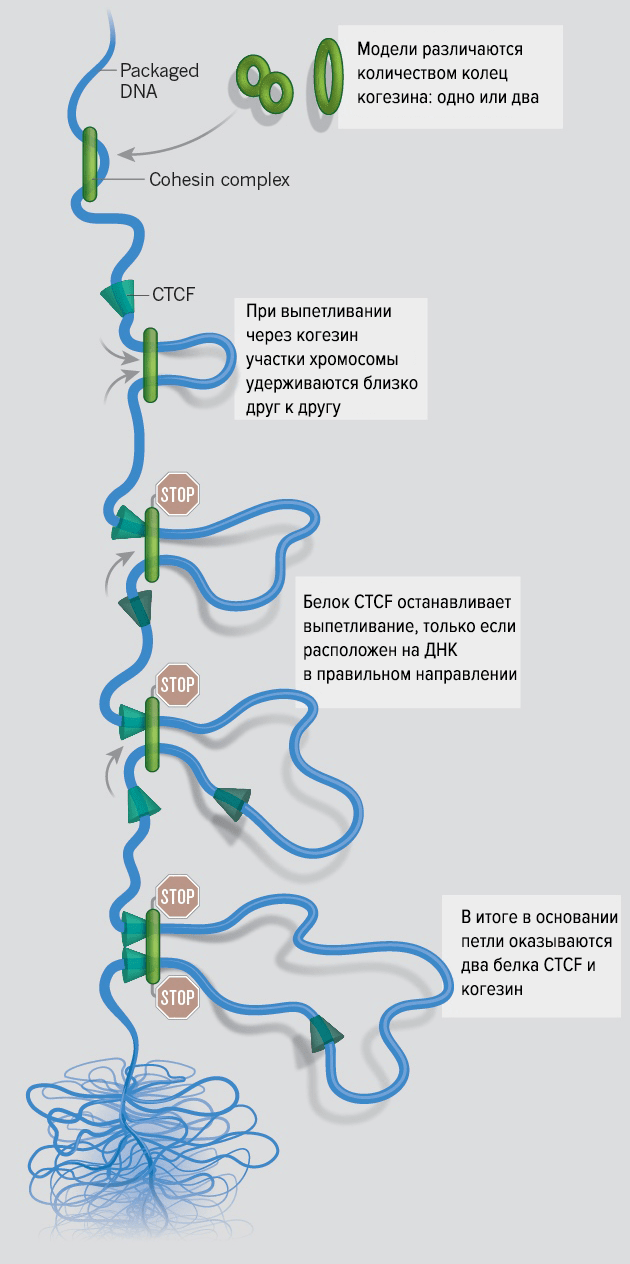
Одним из главных действующих лиц оказался белок CTCF. Было известно, что он взаимодействует с когезином в основании петель неконденсированных хромосом. Долгое время считалось, что петли ДНК образуются тогда, когда любые CTCF случайно сталкиваются друг с другом и соединяются вместе.
Как рассказывает Илья Флямер, в работе лаборатории Либермана Айдена 2014 года с использованием Hi-C метода были были картированы петли в очень высоком разрешении [19]. Установили, что в основании петель CTСF находится на сайтах строго определенной ориентации: «Сайт посадки CTCF асимметричен, и это определяет возможное направление петель, которые этот сайт может образовать. Такая преференция не может возникнуть при случайной диффузии и встрече белков — они будут встречаться случайными сторонами и формировать петли вне зависимости от направления их сайта посадки».
Как предполагается в модели Мирного и коллег, белки CTCF — это знаки «стоп» для когезина. Если когезин доходит до определенным образом ориентированного CTCF с каждой стороны растущей петли, то эти белки оказываются сведенными вместе, и когезин прекращает пропускать ДНК (рис. 4).
Рисунок 4. Наглядное изображение модели петлеобразования в геноме и роль CTCF и когезина. Модель геномной организации loop extrusion помогает объяснить, как определенные участки хромосом в интерфазе оказываются сближены и почему кольца протеинового комплекса когезина часто находятся в контакте с белками CTCF, которые связываются с определенными последовательностями ДНК.
Такое описание функции когезина помогает объяснить некоторые экспериментальные данные. Например, что когезин влияет на размер хроматиновых петель [20]. Повышенная его активность приводит к производству такого количества петель, что хромосомы становятся похожи на маленьких червячков (за это их даже окрестили «вермишельками» — vermicelli [21], видом пасты, которая с итальянского буквально переводится как «маленькие червячки»; увидеть их при окрашивании ДНК можно в только что вышедших препринтах [22], [23]).
Теперь остается ждать прямого подтверждения, что этот комплекс белков работает именно так. Ведь пока что утверждение о роли когезина как мотора, способного наращивать петли, приходится принять на веру, поскольку его поведение, описанное в модели, еще не подтверждили ни в живых клетках, ни даже in vitro [2]. Совсем недавняя работа, однако, показала, что близкий родственник когезина — конденсин, необходимый для упаковки хромосом и главный герой гипотез Насмита, Марко и Мирного про метафазные хромосомы, — ведет себя как мотор in vitro [24].
«Всю важность процесса петлеобразования ученые пока оценить не могут, — рассказывает „Биомолекуле“ Илья Флямер, — однако есть предположение, что это — ключ к разгадке механизма действия энхансеров. Также он может участвовать в поддержании незапутанного состояния хромосом и предотвращении двухцепочечных разрывов, особенно при делении. Более того, вероятно, что аналогичный процесс с конденсином вместо когезина обеспечивает конденсацию хромосом».
Как изучают геном?
Изучать биологические системы крайне трудно из-за того, что все процессы в них динамические, разноуровневые (например, на уровне молекул, клеток или целого организма) и протекают с разной скоростью. Их детализация помогает создать биофизические модели, описывающие функционирование генома. Сейчас способов изучения динамических систем множество: от визуализации живых клеток до 3C-методов анализа трехмерной организации генома (3C = Chromosome Conformation Capture — фиксация конформации хромосомы) [25]. Вторую группу методов, к которой относится и упомянутый Hi-C (видео 5), применяют для улучшения понимания организации хромосом и опосредованно — регуляции активности генов, репарации ДНК и деления. Про 3C- и Hi-C-методы «Биомолекула» уже разговаривала раньше с Ильей Флямером [26].
Видео 5. Наглядный пластилиновый мультик о технологии Hi-C
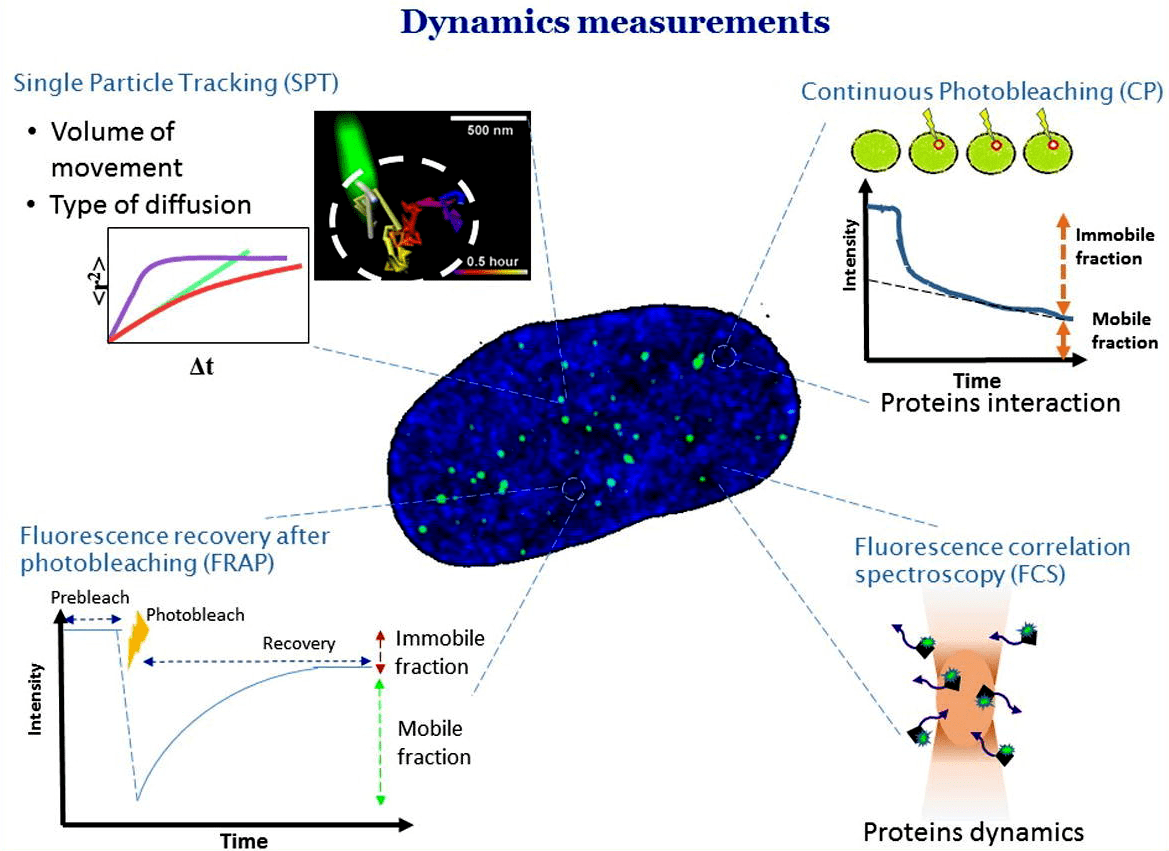
Также для изучения белков, РНК, ДНК, отдельных локусов генов и ядерных телец используют флуоресцентную гибридизацию in situ (fluorescence in situ hybridization, FISH), трекинг отдельных частиц (single particle tracking, SPT), непрерывное фотообесцвечивание (continuous photobleaching, CP), восстановление флуоресценции после фотообесцвечивания (fluorescence recovery after photobleaching, FRAP) и флуоресцентную корреляционную спектроскопию (fluorescence correlation spectroscopy, FCS). Подробнее о них можно почитать в специальной статье, посвященной этой теме [27].
Рисунок 5. Методы изучение структуры генома в живой клетке. SPT — трекинг отдельных частиц; CP — непрерывное фотообесцвечивание; FRAP — восстановление флуоресценции после фотообесцвечивания; FCS — флуоресцентная корреляционная спектроскопия.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Версия Либермана Айдена: параллельная гипотеза
Как уже было сказано, параллельно гипотезу петлеобразования разрабатывал Эрез Либерман Айден из Хьюстонского Медицинского колледжа Бейлора (видео 6). По его словам, догадка о роли когезина и CTCF возникла у него во время телефонной конференции в марте 2015 года при обсуждении подробностей структуры генома, полученных с помощью Hi-C-метода им и его бывшим руководителем Эриком Ландером.
Видео 6. Модель петлеобразования в ДНК, предложенная группой Либермана Айдена
После многочисленных проверок гипотезы его группа подала статью на публикацию в июле 2015 года. В итоге работа была опубликована три месяца спустя (см. видео 6) [4]. В общем, обе модели — и Мирного, и Либермана Айдена — приходят примерно к одинаковым выводам.
Хотя экспериментальных данных в работе Мирного было меньше, его группа для подкрепления своей гипотезы включила в работу компьютерную модель. Некоторых это заставляет сомневаться в том, что работа Либермана Айдена (который, по словам Мирного, слышал его доклад в Институте Вейцманна и не сослался на статью из биоархива) была разработана полностью самостоятельно. Сам же ученый непреклонен. Он утверждает, что заявка на публикацию была подана до того, как он увидел труд Мирного и его группы.
Различия гипотез
Расхождения двух моделей незначительны [2]. Например, в гипотезе Мирного количество колец не уточняется. В версии Либермана Айдена же — это два соединенных кольца. Хотя различие выглядит довольно механическим, специалисты называют его крайне важным для определения роли этого комплекса.
Другое различие гипотез — по мнению Мирного, у когезина есть моторная функция, не имеющая отношения к кольцевой форме когезина-карабина. Либерман Айден, в целом, эту идею отвергает. Однако оба предположения возможны, и существуют данные, поддерживающие каждую из сторон. В частности, то, что когезин работает как мотор, подтверждает эксперимент под руководством Дэвида Руднера (David Rudner) — биолога, изучающего бактериальные клетки на медицинском факультете Гарварда (штат Массачусетс, США). Его группа сделала карту разных моментов складывания хромосомы бактерии Bacillus subtilis при использовании метода Hi-C. На ней исследователи увидели работу комплексов структурного поддержания хромосом (SMC) — бактериальных родственников когезина и конденсина — и то, что при этом создаются петли со скоростью более 50 000 пар нуклеотидов в минуту. По мнению ученых, этот темп примерно совпадает с тем, который должен бы быть в модели Мирного, примененной к клеткам человека. Пока что затрата АТФ в этом процессе не доказана, но Руднер считает, что он близок к этому. Более того, по его словам, он был бы шокирован, если бы когезин в клетках человека работал иначе.
Гипотезу Либермана Айдена поддерживают данные о малом потреблении энергии комплексом при захвате и высвобождении ДНК, что затрудняет его работу на тех скоростях, которые предполагаются в модели Мирного. Возможно, есть иные молекулы, которые помогают скольжению когезина вдоль генома на большие расстояния (например, РНК-полимеразы, которые транскрибируют гены при производстве РНК). Согласно другому мнению, моторные белки вообще не нужны для производства петель. Когезин может перемещаться по ДНК случайным образом до тех пор, пока не встретит CTCF и не сделает петлю.
Предыстория: как была разгадана структура ДНК в сложенном виде
Для научного мира гипотеза, которая не находит какое-то время экспериментального подтверждения, — отнюдь не редкость. Иногда этого приходится ждать десятилетиями! Например, теоретически «сложенная» структура ДНК была разгадана учеными задолго до аналогичных лабораторных данных.
В 1930–1940-х годах конфигурации полимерных цепей активно изучал американский физик и химик Пол Флори [28–30]. Позже, в 1960-х, Илья Лифшиц, знаменитый советский физик-теоретик и будущий лауреат Нобелевской премии, начал заниматься характеристиками макромолекул, в частности, поведением белков в растворах [31]. В 1979 году он вместе с А. Гросбергом и А. Хохловым опубликовал работу «Объемные взаимодействия в статистической физике полимерной макромолекулы» [32]. В ней они изложили модель перехода клубок—глобула, описывающую конденсацию длинной полимерной цепочки из раскрученного состояния в глобулу.
Советские ученые продолжали заниматься этой темой, и в 1988 году была напечатана статья А. Гросберга, С. Нечаева и Е. Шахновича о роли топологических ограничений для макромолекулы [33]. В 1993 году Гросберг с коллегами предположил, что ДНК в ядре для выполнения своих биологических функций должна иметь структуру «фрактальной глобулы» [34]. Согласно гипотезе, близко расположенные участки генома вероятнее всего взаимодействуют друг с другом и формируют глобулу первого порядка. Далее из близлежащих глобул первого порядка собираются глобулы второго порядка и так далее. Если полимер не будет запутываться в узлы, то он будет образовывать «комки» разных размеров и сможет быстро «сплетаться» и «расплетаться». Теоретическую возможность существования такой глобулы подтвердили в 2005 году Нечаев и Васильев, когда опубликовали статью с объяснениями стабильности конструкции и связи между наличием/отсутствием узлов и пространственной укладкой длинной цепи [35]. Долгое время все же гипотеза так и оставалась гипотезой. Ее главной соперницей была стохастическая (случайная) модель укладки [25], описанная, например, в статьях Мюнкеля и Ланговски [36] и Матеоса-Лангерака с коллегами [37].
Наконец, в 2009 году группа ученых, работающих в США под руководством Джоба Деккера, сделала первую карту Hi-C. На основе этой карты сотрудник лаборатории Мирного Максим Имакаев разработал трехмерную модель укладки ДНК, которая полностью совпадала с гипотезой Нечаева—Гросберга—Шахновича о фрактальной глобуле (видео 7). Один из соавторов модели укладки ДНК — Леонид Мирный из MIT, выпускник МИФИ и ученик Шахновича; другой — Максим Имакаев, выпускник МФТИ и MIT. (Подробнее можно почитать в новостной заметке в «Популярной механике» [38].)
Видео 7. А скорее, живая картинка — трехмерная структура генома
…конструкция представляет собой иерархическую систему складок. Полимер образует маленькие складочки, становясь более толстой и короткой «сосиской», она затем опять образует складки, становясь еще более толстой и короткой «сарделькой», и т.д. В результате получается компактная структура без узлов, плотно заполняющая все пространство. /…/ в свое время научное сообщество отнеслось к нашей теории не очень внимательно, что пусть и немного обидно, но справедливо: мало ли гипотез на свете. Но “хорошо то, что хорошо кончается”
Сергей Нечаев,
доктор физико-математических наук,
ведущий научный сотрудник ФИАН и
Центра национальных исследований Франции CNRS
Полное интервью о его работе и истории рождения теории фрактальной глобулы можно прочитать на сайте МГУ и на polit.ru.
Верить ли безоговорочно новой модели?
Среди исследователей сейчас идет академический спор: насколько признавать новую модель loop extrusion? Хотя множество факторов говорит в пользу того, что группы Мирного и Либермана Айдена правы, окончательно признавать когезин главным героем петлеобразования еще рано [13]. Многие исследователи призывают к здоровому скептицизму до окончательного подтверждения модели, как, например, Даг Кошланд (Doug Koshland) из Калифорнийского университета в Беркли. По словам ученого, его волнует преждевременное возведение гипотезы на пьедестал и то, что из-за своей простоты и элегантности она уже попадает в учебники [2].
«Я думаю, что эта модель прорывная! И, на мой взгляд, она, скорее всего, верна — слишком хорошо объясняет данные относительно когезина и CTCF», — делится с «Биомолекулой» Илья Флямер.
Однако для начала необходимо как минимум установить точные молекулярные механизмы, ведущие к «пропусканию» ДНК, и пути регуляции этого процесса. Кроме того, нужен и детальный анализ роли в формировании петель вспомогательных белков и CTCF и их взаимодействия с хроматином. По словам Мирного, на часть вопросов сможет ответить проверка функции когезина и CTCF в клетках людей, страдающими заболеваниями, где работа этих молекул нарушена, например, из-за мутации. С другой стороны, исследователь говорит, что не может объяснить образование петель никаким другим образом.