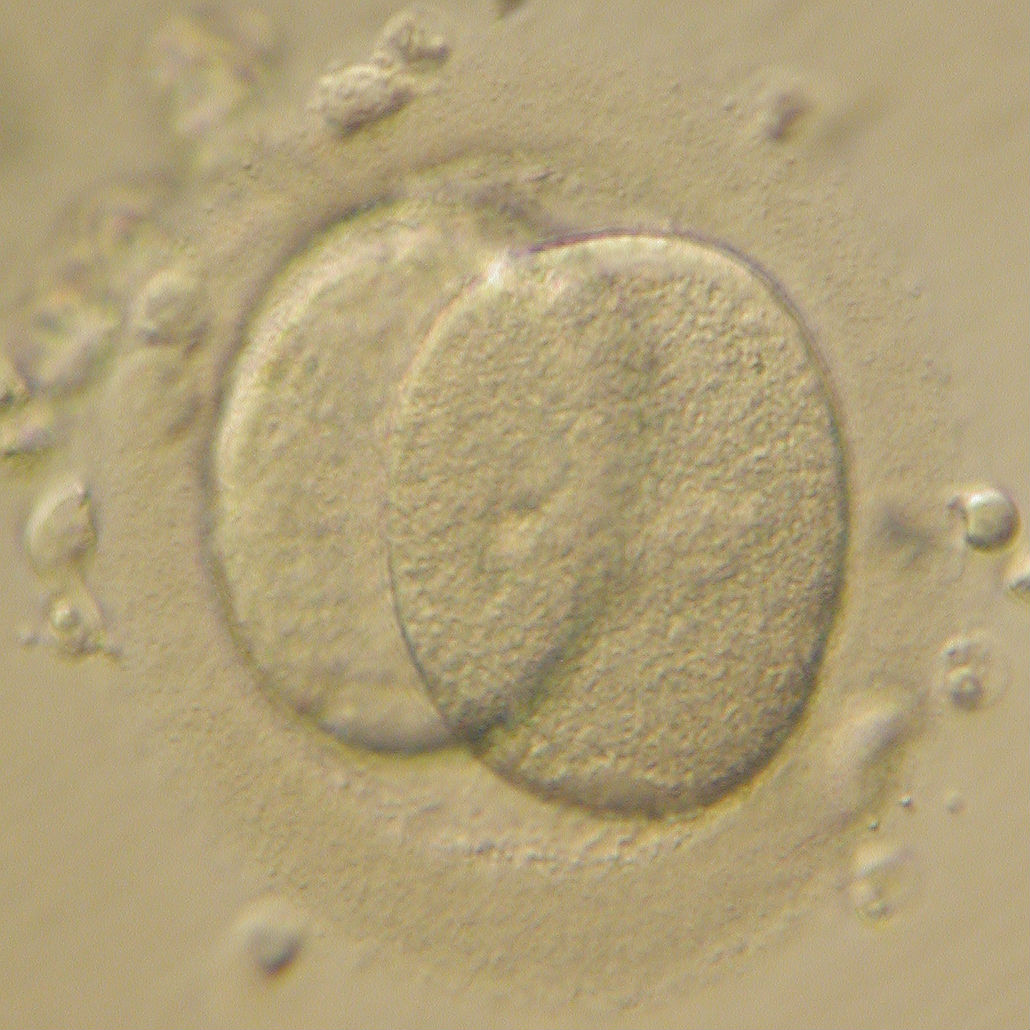
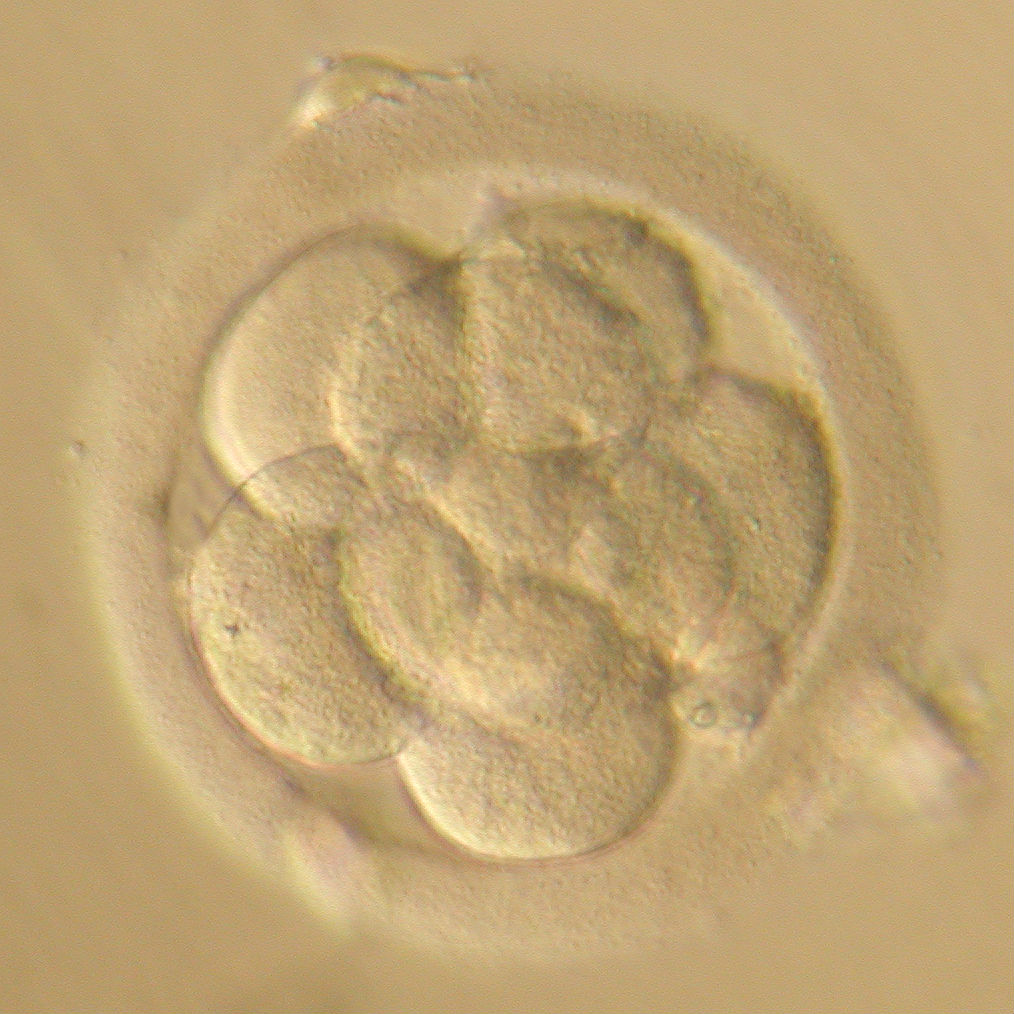
Классификация эмбрионов при ЭКО
Несмотря на старания ученых и практикующих репродуктологов, до сих пор не удается приблизиться к тому, чтобы практическая каждая попытка экстракорпорального оплодотворения заканчивалась родами. Поэтому возникает резонный вопрос – на что влияет качество эмбрионов при ЭКО, как его оценить, какие предпринять дальнейшие действия и процедуры.
Что такое качество ооцита?
Сразу после того, как получены женские и мужские половые клетки, начинается оценка их качества по морфологическим признакам. Это важно для того, чтобы эмбриолог принял правильное решение о методе оплодотворения – ЭКО или интрацитоплазматическая инъекция (ИКСИ).
Ооцит (женская половая клетка) может иметь разную степень готовности к оплодотворению. Поэтому различают следующие виды яйцеклеток – незрелые, зрелые, дегенеративные и разрушенные. Класс ооцита определяют по состоянию генетического материала в ядре клетки. Зрелые яйцеклетки, которые можно оплодотворять, имеют первое полярное тельце (такие клетки обозначаются М II).
Незрелые яйцеклетки оплодотворению не подлежат. Обычно процесс созревания женской гаметы прерывается на более ранней стадии мейотического деления вследствие внутренних или внешних причин, а также в результате неправильного введения триггера (например, хорионического гонадотропина в цикле ЭКО).
Плохое качество яйцеклеток при ЭКО – причины
Качество эмбрионов при ЭКО, с одной стороны, определяется качеством генетического материала яйцеклетки, а с другой – качеством материала сперматозоида. Причинами плохого состояния женских половых клеток могут быть следующие факторы:
Помимо внешних причин, которые рассмотрены выше, на исход беременности влияет также качество эмбриона, а не только половых клеток, из которых он состоит. Это так называемые эмбриональные факторы, роль которых высока не только при искусственном оплодотворении, но и при естественном зачатии. Так, почти 50% самостоятельных зачатий завершаются прерыванием, при этом женщина даже не догадывается об этом состоянии ввиду отсутствия задержки месячных. В большинстве случаев причиной таких сверхранних потерь беременности являются хромосомные патологии эмбриона. Как правило, они не совместимы с жизнью, поэтому и происходит их естественная гибель.
В рамках ЭКО выявить подобные состояния помогает предимплантационная диагностика, при которой исследуется хромосомный набор эмбриона перед его введением в полость матки. Проводится не всем парам, а только при наличии показаний.
Так же при развитии эмбрион может остановиться на любой стадии оплодотворения. Одной из причин может быть иссечение внутренних запасов женской гаметы, а образовавшийся эмбрион не может еще продуцировать питательные вещества, поэтому погибает.
Классификация эмбрионов по качеству ЭКО
Классификация эмбрионов по качеству при ЭКО основана на оценке ряда факторов:
Традиционно принято выделять несколько вида эмбрионов при ЭКО с учетом времени их развития. Однако это не единственный критерий, важный при применении методов вспомогательной репродукции. Существует еще классификация эмбрионов по качеству при ЭКО, которая также зависит от «возраста» зародыша.
Формирование зиготы- первые сутки развития
Примерно через 16-20 часов после соединения яйцеклетки со сперматозоидом инициируется эмбриональное развитие, о чем говорит появление пронуклеусов (шифруется в протоколе ЭКО как pN). Эти структуры соответствуют генетическому материалы полученному от родителей, в норме их два, один от матери и один от отца.
качества эмбрионов при ЭКО в первые сутки выглядит следующим образом:
В классификации эмбрионов при ЭКО используются буквенные и числовые обозначения. Так, число указывает на количество клеток (бластомеров), а буква латинского алфавита – на их качество:
.
Хорошими эмбрионами на третьи сутки развития считаются те, которые имеют более 5 бластомеров, качество которых соответствует категории А и В.
В оценке «трехдневок» один из главных критериев – это степень фрагментации эмбрионального материала. Эта классификация предполагает выделение 4 подтипов:
Начиная с 3 суток Эмбрионы можно заморозить, чтобы использовать при последующих ЭКО. Криоконсервация позволяет проводить подсадку в цикле без стимуляции яичников гормональными препаратами, а это повышает шансы успешного развития беременности и последующих родов.
Компактизация до стадии морулы – с третих по пятые сутки развития.
С конца третьих суток между клетками зародыша постепенно стираются границы. Этот процесс называется компактизацией и знаменует начало формирования морулы.
Оценка состояния эмбриона на данном этапе развития не используются, т.к. малоинформативны. Единственное, что можно оценить – есть компактизация или нет.
Образование и рост бластоцисты – с четвертых по седьмые сутки развития.
С 4-х суток начинает формироваться бластоциста. Классификация эмбрионов выглядит несколько иным образом. В расчет берутся следующие критерии:
Расшифровка оценки эмбрионов при ЭКО в этом случае такова:
Начиная со стадии бластоцисты, развитие эмбриона должна уже осуществляться в матке. Для этого должен пройти хетчинг, который условно можно сравнить с процессом «вылупления из яйца», когда разрушается наружная оболочка, выполняющая роль «скорлупы».
Как улучшить качество эмбрионов при ЭКО?
Чтобы еще до вступления в программу ЭКО улучшить качество будущих эмбрионов, пара проходит расширенную диагностику. При выявлении различных отклонений от нормы проводится их коррекция. Помимо этого, назначается предгравидарная подготовка, в которую входят препараты фолиевой кислоты, омега-3 кислоты, йод и другие минералы, витамины.
В репродуктивном центре «СМ-Клиника» оказывается полный спектр услуг в рамках методов вспомогательной репродукции, подготовки к предстоящей беременности и ее ведению. В клинике внедрены современные протоколы, что позволяет добиваться высоких показателей эффективности ЭКО. Записывайтесь на прием и становитесь родителями здоровых малышей!
СТРАТЕГИИ И МЕТОДЫ ВЫБОРА ЭМБРИОНА
Успех в программе экстракорпорального оплодотворения зависит от многих факторов и определяется сочетанием правильно подобранных методик на разных этапах цикла: стимуляции суперовуляции, трансвагинальной пункции, обработки эякулята или биоптата яичек, выбора подходящей процедуры оплодотворения ооцитов (ЭКО, ИКСИ, ПИКСИ,ИМСИ), переноса эмбриона/ов в полость матки, гормональной поддержки после переноса.
Очень важным моментом является выбор эмбриона/ов, который будет перенесен в полость матки. После процедуры экстракорпорального оплодотворения эмбриолог внимательно наблюдает за развитием эмбрионов, при этом оценивает развитие каждого из них индивидуально. Основными характеристиками являются наличие оплодотворения, темп развития и качество эмбрионов.
На основании информации о развитии эмбрионов, их количестве и состояния эндометрия, а также дальнейшей тактики лечения врач и эмбриолог принимают решение:
Рассмотрим основные подходы, применяющиеся для ответа на эти вопросы, в случае, если перенос все же состоится в данном лечебном цикле. Отмена переноса случается довольно часто и может быть связана с развитием у пациентки синдрома гиперстимуляции, необходимостью в проведении дополнительных генетических обследований эмбрионов, недостаточностью функционального состояния эндометрия и др.
По каким признакам выбирается эмбрион для переноса?
Традиционно качество эмбрионов и процесс их развития принято оценивать визуально: после оплодотворения ооцитов (это происходит в день пункции, его принято считать нулевым) эмбриолог при помощи микроскопа с высоким разрешением и специальным контрастом наблюдает за эмбрионами и классифицирует их в соответствии с принятой системой. Качество эмбриона оценивают по разным критериям в зависимости от суток развития.
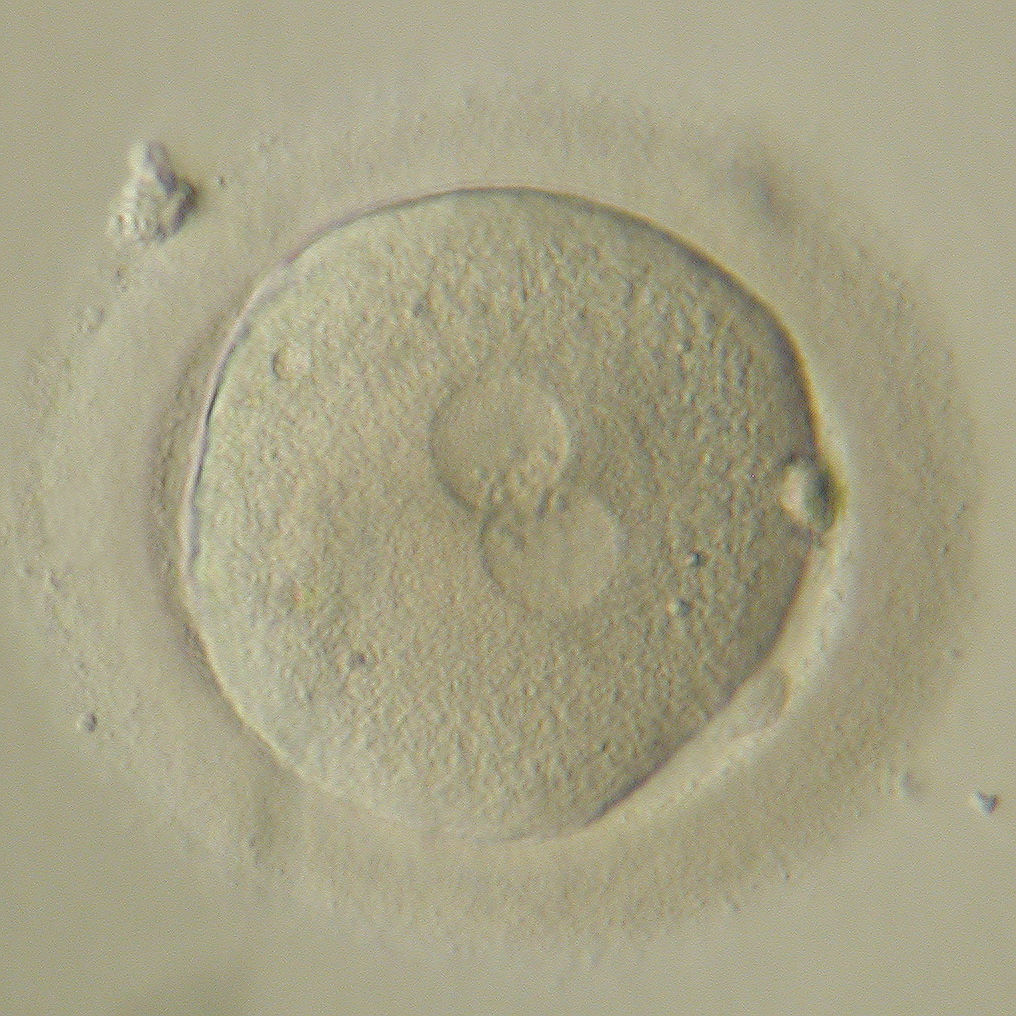

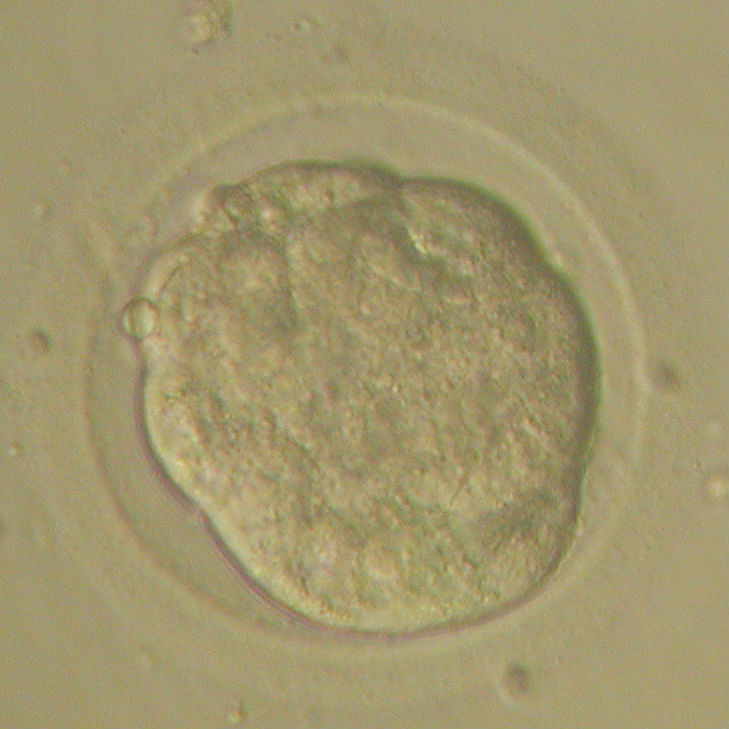
К пятым суткам начинается процесс кавитации (в эмбрионе образуется полость, клетки делятся на две группы – трофобласт и внутреннюю клеточную массу в зависимости от их положения в эмбрионе и дальнейших функций), в результате на 5-6 сутки развития формируется бластоциста – эмбрион, готовый к имплантации в стенку матки.
Классификация, разработанная для бластоцист более сложная, чем для эмбрионов более ранних стадий, и сводится к оценке количества и качества клеток в различных частях бластоцисты, а также размеров полости (Рис.6). В целом такая система оценки эмбрионов по внешнему виду оправдывает себя, так как имеется корреляция между качеством переносимых эмбрионов и частотой наступления беременности. Тем не менее, выбор качественного эмбриона – сложная задача, и чем больше современных методик и средств анализа доступно эмбриологу в клинике, тем выше вероятность, что этот выбор будет наиболее точным.
С недавних пор у эмбриологов появилась возможность наблюдать за развитием эмбриона практически непрерывно, благодаря новой технологии time-lapse микроскопии. В инкубатор, где развиваются эмбрионы, помещается специальный прибор, который через определенные интервалы времени фотографирует эмбрионы и сохраняет изображения. В итоге эмбриолог получает своеобразный фильм о развитии каждого эмбриона.
Преимуществом этого подхода является то, что появляется возможность оценивать не только внешний вид эмбриона, но и динамику его клеточных делений и видоизменений во времени. Кроме того, для анализа развития эмбриона не нужно доставать его из инкубатора, что снижает стресс от резкой перемены внешних условий. Соотнеся полученную запись с имеющимися данными о нормальном временном ходе развития, эмбриолог может выбрать для переноса эмбрион не только с наилучшими внешними характеристиками, но и с наиболее оптимальной “историей” развития.
Если у пары есть показания, связанные с риском передачи наследственных заболеваний, либо повышенной вероятностью возникновения генетических аномалий при оплодотворении и развитии эмбрионов, необходимо проводить не только оценку качества (внешних характеристик) эмбрионов, но также анализ их генетического материала. В таких случаях кроме визуальной оценки проводят также преимплантационную генетическую диагностику (ПГД).
После проведения ПГД эмбриолог может выбрать для переноса в полость матки эмбрионы без генетических отклонений, что существенно увеличивает вероятность наступления беременности и снижает частоту невынашивания.
При первом обращении к врачу-репродуктологу супругам нужно будет подробно рассказать, были ли в роду у каждого из них наследственные заболевания. Однако даже если пара не знает о наличии у них генетических заболеваний, нужно провести ряд обследований (генетическая диагностика перед планированием беременности): кариотипирование и тест на носительство наиболее часто встречающихся моногенных заболеваний у обоих супругов.
По результатам этих тестов можно определить, показано ли паре проведение преимплантационной диагностики эмбрионов. Помимо этого важную роль играет возраст будущей матери – с возрастом (особенно после 36 лет) повышается вероятность рождения ребенка с хромосомными аномалиями. В каждом случае набор генетических аномалий, на которые будет проводиться тестирование эмбрионов, определяется для каждой пары индивидуально, в зависимости от показаний и наличия риска развития тех или иных генетических отклонений.
Сколько эмбрионов переносить?
Вопрос о выборе количества эмбрионов для переноса всегда является предметом детального обсуждения между репродуктологом, эмбриологом и пациентом. Ответ на этот вопрос в каждом конкретном случае зависит от количества имеющихся эмбрионов, стадии их развития (так, вероятность имплантации повышается при переносе бластоцисты по сравнению с дробящимся эмбрионом), оценкой риска имплантации двух и более эмбрионов.
При отсутствии единого решения для всех случаев, общемировой тенденцией является снижение количества единовременно переносимых в полость матки эмбрионов с целью снижения вероятности наступления многоплодной беременности.
На какой день переносить эмбрионы?
Важным решением является и то, на какой день осуществлять перенос эмбриона. Оно также требует тщательного анализа всех факторов. В том числе, важную роль здесь играют: количество и качество полученных эмбрионов, анамнез пары, информация о предыдущих попытках ЭКО/ИКСИ. Обычно перенос эмбрионов в полость матки проводится с 3 по 6 сутки развития.
По сравнению с более ранними стадиями, к 3-м суткам развития уже активируется собственный геном эмбриона, а значит – снижается вероятность остановки в развитии из-за ошибок в этом процессе. Кроме того, оценка эмбрионов на 3 и 5 сутки развития более удобна с точки зрения строения эмбриона, чем на 4-е сутки (стадия компактизации).
Не вдаваясь в детали, можно выделить следующие общие принципы, влияющие на выбор дня переноса эмбрионов:
Таким образом, перенос эмбриона в полость матки проводится только после принятия специалистами целого ряда тщательно взвешенных решений. Чем больше информации окажется в руках у репродуктологов и эмбриологов, тем более оптимальным будет выбор всех слагаемых, необходимых для успешного наступления беременности и рождения здорового ребенка.
Факторы, влияющие на процесс ранней компактизации эмбрионов человека в культуре
| Первые деления эмбрионов человека – деления дробления – проходят, как и у большинства видов животных, без увеличения размеров образующихся клеток. Это приводит к тому, что размеры эмбриональных клеток – бластомеров – уменьшаются до уровня соматических. Однако процесс дробления у млекопитающих имеет ряд специфических особенностей, в частности, относительно медленный темп делений, своеобразное расположение бластомеров по отношению друг к другу, асинхронность раннего дробления, а также наличие процесса компактизации эмбрионов, в ходе которого ранее рыхло расположенные бластомеры сближаются, площадь контакта между ними увеличивается и они образуют компактный клеточный шар с трудноразличимыми при прижизненном наблюдении границами между отдельными бластомерами. В ходе компактизации между клетками эмбриона устанавливается более совершенная система межклеточных связей, заключающаяся в появлении щелевых, а затем плотных межклеточных контактов [1]. Для осуществления процесса компактизации необходимы ионы кальция, также в нем участвуют цитоскелет и специфические молекулы межклеточной адгезии увоморулины [2, 3]. |
Вопрос о продолжительности первого клеточного цикла в ходе дробления у человека был изучен в ряде работ. По данным A.Trounson и соавт. [4], первые эмбрионы на стадии двух бластомеров в культуре можно наблюдать через 27 ч после инсеминации ооцитов. Однако, по данным H.Balakier и соавт. [5], длительность этого периода составляет 20–22 ч, а по результатам работы G.Capmany и соавт. [6] – примерно 25 ч. Показано также, что некоторые эмбрионы человека обладают способностью к более быстрому дроблению в культуре [5, 7]. Продолжительность последующих клеточных циклов составляет около 18 ч [2]. Первые компактизованные эмбрионы в культуре можно наблюдать уже на стадии 8 бластомеров (ранняя компактизация эмбрионов). Однако начало этого процесса более характерно для эмбрионов, находящихся на стадии 16 клеток.
Вопрос о факторах, оказывающих влияние на появление в культуре эмбрионов c ранней компактизацией, фактически не изучен. Выявление этих факторов явилось целью настоящей работы.
Анализ факторов, влияющих на появление в культуре эмбрионов с ранней компактизацией, проведен на основе результатов лечения бесплодия методом экстракорпорального оплодотворения (ЭКО) у 470 пациенток Международного центра репродуктивной медицины НИИ акушерства и гинекологии им. Д.О. Отта РАМН. Показаниями к ЭКО явились трубно-перитонеальное бесплодие вследствие непроходимости или отсутствия маточных труб, а также отклонение показателей спермограммы от нормы.
Для стимуляции суперовуляции использованы кломифенцитрат (клостилбегит) и человеческий менопаузальный гонадотропин (хумегон, пергонал). Для индукции овуляции вводили хорионический гонадотропин при достижении лидирующими фолликулами диаметра 17–18 мм. Для инсеминации ооцитов в среду культивирования вводили 100 000 сперматозоидов. Контроль оплодотворения проводили через 18 ч после инсеминации. Зиготы с двумя пронуклеусами переносили в свежую питательную среду. Через 24 ч с момента контроля оплодотворения (первая оценка) эмбрионы анализировали под микроскопом и определяли число бластомеров и степень фрагментации. Выделяли три основные типа эмбрионов: без фрагментации бластомеров, а также с легкой и тяжелой степенью фрагментации цитоплазмы. Эмбрионы первой группы характеризовались индексом фрагментации 3, второй – 2 и третьей – 1. Вторая оценка развития эмбрионов происходила перед переносом их в полость матки через 48 ч с момента контроля оплодотворения ооцитов (66 ч после инсеминации ооцитов). При этом наряду с оценкой числа и морфологии бластомеров определяли наличие ранней компактизации эмбрионов.
Исследование влияния морфологии сперматозоидов на появление в культуре эмбрионов с ранней компактизацией проведено по результатам лечения бесплодия методом ЭКО у 85 женщин. Для анализа морфологии сперматозоидов на препарате клетки отделяли от семенной жидкости. Для этого 0,2 мл нативной спермы помещали в центрифужную пробирку и добавляли 1,5 мл буфера, состоящего из 10 мМ трис-HCl, pH 7,5, 5 мМ MgCl2 и 10 мМ KCl, после чего проводили центрифугирование при 100 000 об/мин в течение 5 мин. Cупернатант сливали и отмывку повторяли дважды, затем осадок ресуспендировали до концентрации 106 клеток в 1 мл, наносили тонким слоем на стекло и высушивали. Препараты фиксировали в 70% этаноле в течение 10 мин, после чего высушивали и окрашивали гематоксилином Харриса и бенгальским розовым (фирма «Fisher Scientific»).
Для оценки морфологии сперматозоидов использовали модифицированную классификацию Крюгера [8, 9]. Определение доли клеток с различными морфологическими характеристиками проводили при увеличении 1000 (об. 100, ок. 10), просчитывая по 200 клеток на каждом препарате. Для морфологически нормального сперматозоида характерна овальная форма головки, длина ее составляет 5–6 мкм, ширина 2,5–3,5 мкм, акросомальный участок занимает от 40 до 70% площади головки, при этом отсутствуют аномалии в области шейки, хвоста, срединное тело не выражено. К пограничным формам относили клетки с хорошо выраженным акросомальным участком, имеющие слегка удлиненную головку диаметром 2–2,5 мкм или небольшие утолщения в области шейки.
Для обработки полученных данных использовали t-критерий Стьюдента, а также критерий c2.
Ранняя (через 66 ч с момента инсеминации ооцитов) компактизация отмечена у 2,9% (у 57 из 1922) эмбрионов. Эмбрионы на стадии компактизации в среднем имели 7,6±0,3 бластомера, что было достоверно выше (р меньше 0,0001), чем число клеток у некомпактизованных (5,2±0,1). Несмотря на низкую частоту встречаемости данного явления, у некоторых женщин было отмечено одновременное появление нескольких (максимум 4, в среднем 1,74±0,21) компактизованных эмбрионов, что может свидетельствовать о существовании индивидуальной предрасположенности к их формированию.
В зависимости от наличия ранней компактизации эмбрионов были выделены две группы женщин. В 1-ю группу были включены 437 пациенток, эмбрионы которых не имели признаков ранней компактизации, во 2-ю – 33 женщины, у которых этот процесс был отмечен.
Возраст больных в группах не различался и составлял 31,6±0,2 и 30,8±0,8 года соответственно. Отличий по числу пунктированных фолликулов и полученных ооцитов также не было выявлено, в то же время число зигот и, как следствие этого, полученных и перенесенных в полость матки эмбрионов были достоверно выше во 2-й группе женщин (табл. 1). Выявленные различия могут быть обусловлены влиянием со стороны показателей сперматогенеза мужа. По данным спермограммы мужа, доля прогрессивно-подвижных форм, а также морфологически нормальных сперматозоидов и сперматозоидов с легкой патологией была выше во 2-й группе женщин (табл. 2).
Таблица 1. Результаты стимуляции суперовуляции и оплодотворения в культуре
|
Примечание. *– p меньше 0,05; **– p меньше 0,01.
Таблица 2. Показатели сперматогенеза
|
Примечание. *– p меньше 0,05.
При оценке характера развития эмбрионов было показано, что эмбрионы пациенток 2-й группы как через 24 ч, так и через 48 ч после контроля оплодотворения ооцитов имеют большее число бластомеров с менее выраженной фрагментацией цитоплазмы. Аналогичные различия обнаруживаются и при анализе эмбрионов, перенесенных в полость матки (табл. 3). При сравнении частоты наступления беременности у женщин исследуемых групп различий не выявлено. В то же время доля многоплодных беременностей в подгруппе беременных была достоверно выше в тех случаях, когда среди перенесенных в полость матки эмбрионов были эмбрионы с признаками ранней компактизации (табл. 4).
Таблица 3. Индекс фрагментации и число бластомеров у эмбрионов
| |||||||||||||||||||||||||||
Примечание. Первое наблюдение – 24 ч, второе – 48 ч после контроля оплодотворения. *– p меньше 0,0001.
Таблица 4. Частота наступления беременности в исследуемых группах
|
Примечание. *– p меньше 0,01.
Число бластомеров и степень выраженности процесса фрагментации цитоплазмы в настоящее время являются основными критериями для прижизненной оценки развития эмбрионов человека в программе ЭКО [2]. В последнее время в литературе появились данные о том, что традиционная схема контроля оплодотворения по наличию пронуклеусов через 18 ч после инсеминации ооцитов и последующего прижизненного наблюдения за развитием эмбриона через 24 и 48 ч после контроля оплодотворения не позволяет достаточно надежно выявить различия в темпах дробления эмбрионов в культуре. Например, в работе [7] показано, что уже через 25 ч после инсеминации в культуре можно наблюдать появление первых эмбрионов на стадии двух бластомеров. Эти эмбрионы, названные авторами «эмбрионами с ранним дроблением», при последующем переносе в полость матки имплантируются чаще, чем те, у которых процесс дробления начинается позднее. Отбор таких эмбрионов для переноса позволяет существенно повысить частоту наступления беременности. Однако при традиционной схеме контроля оплодотворения выявить такие эмбрионы практически не представляется возможным. Асинхронность развития эмбрионов в культуре обычно связывают с различиями во времени проникновения сперматозоидов в ооциты. Основная причина этого – гетерогенность по степени зрелости женских половых клеток, полученных в результате стимуляции фолликулогенеза. Оплодотворение дозревающих в культуре ооцитов приводит к задержке дробления эмбрионов [4]. Появление эмбрионов с ранним дроблением не зависит от характеристик сперматогенеза, особенностей фолликулогенеза или же схемы стимуляции суперовуляции. Цитируемая выше работа является фактически единственной публикацией, в которой обоснован метод отбора эмбрионов по темпам развития для повышения частоты наступления беременности в программе ЭКО.
Явление ранней компактизации эмбрионов в культуре еще детально не было проанализировано в литературе. Не изученным остается основной вопрос – что представляют собой такие эмбрионы? Является ли их ранняя компактизация отражением ускоренных темпов дробления или же это процесс, связанный со спецификой развития эмбрионов в условиях культуры? Тем не менее в большинстве программ ЭКО при наличии таких эмбрионов их, как правило, отбирают для переноса в полость матки. В связи с этим нами в настоящей работе были проанализированы факторы, влияющие на появление в программе ЭКО эмбрионов с ранней компактизацией (через 66 ч после инсеминации ооцитов). Возраст женщины и ответ яичника на стимуляцию суперовуляции (число пунктированных фолликулов) не оказывали влияния на частоту ранней компактизации эмбрионов в культуре. В то же время такие показатели спермограммы мужа, как доля прогрессивно-подвижных сперматозоидов, морфологически нормальных клеток и доля сперматозоидов с легкой патологией, были выше в группе женщин, у которых отмечены эмбрионы с ранней компактизацией. В этой же группе оплодотворяющая способность сперматозоидов мужа также была выше. Это проявилось в том, что при равном числе пунктированных фолликулов и ооцитов, число зигот, а также число полученных и перенесенных эмбрионов у женщин с компактизацией эмбрионов было достоверно выше, чем у женщин, у которых это явление не отмечено. Таким образом, на появление через 66 ч после инсеминации ооцитов эмбрионов на стадии компактизации влияет характер сперматогенеза.
В настоящей работе показано, что явление ранней компактизации отмечается в популяции более динамично развивающихся эмбрионов, имеющих лучшие морфологические характеристики. Наличие компактизованных эмбрионов в числе перенесенных в полость матки не оказывает влияния на частоту наступления беременности, однако в этом случае обнаружена тенденция к повышению частоты многоплодия в подгруппе беременных женщин.
В литературе показано, что такое явление, как раннее дробление, не зависит от клинических показателей сперматогенеза и фолликулогенеза [7]. По нашим данным, на процесс ранней компактизации эмбрионов человека в культуре влияет характер сперматогенеза.
Возраст женщины и ответ яичника на стимуляцию суперовуляции (число пунктированных фолликулов) не оказывают влияния на частоту ранней компактизации эмбрионов в культуре. На процесс ранней компактизации эмбрионов человека в культуре влияет характер сперматогенеза.
О.А. Воробьева, О.А. Леонтьева, А.А. Кирсанов
Институт акушерства и гинекологии им. Д.О. Отта РАМН, Международный центр репродуктивной медицины, Санкт-Петербург