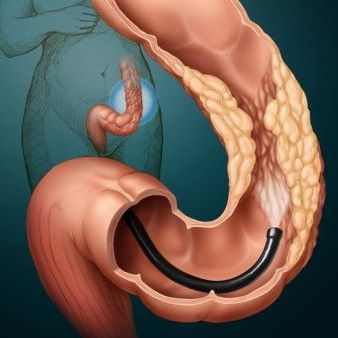
Показания
Эндоскопическое обследование показано для диагностики заболеваний кишечника и своевременного их лечения. К нему следует прибегать в следующих случаях:
Ректороманоскопия позволяет выполнить осмотр слизистой оболочки кишечника на расстоянии 15-30 см от ануса, диагностировать патологии, сделать забор ткани и выполнить несложные операции. Аппаратное исследование также может выступать в качестве подготовительной процедуры перед другими медицинскими манипуляциями.
Возможные риски
Эндоскопическое обследование – абсолютно безопасный метод диагностики. Однако существуют некоторые противопоказания. Если у Вас диагностированы острые воспалительные процессы в области заднего прохода, лучше сделать РРС после стабилизации состояния. При остром парапроктите, глубоких трещинах, остром геморрое с тромбозом узлов не стоит прибегать к эндоскопическому обследованию прямой кишки.
Прямым противопоказанием к процедуре является тяжелое состояние пациента (выраженная сердечно-сосудистая недостаточность, нарушения мозгового кровообращения, тяжелая степень дыхательной недостаточности). То есть случаи, когда риск нанесения ущерба здоровью превышает целесообразность проведения аппаратного осмотра.
Польза
Исследование проводится с профилактической, диагностической и лечебной целями. Чтобы вовремя выявить опухоль, полипы или другие образования, не допустить их развития, людям старше 40 лет рекомендуется 1 раз в год проходить обследование.
Если пациенту предстоит рентгенологическая томография толстой кишки, также предварительно рекомендуется сделать RRS. Многие незначительные, но серьезные изменения в кишечнике диагностируются исключительно эндоскопически.
Подготовка к ректороманоскопии
Перед проведением процедуры необходимо выполнить очистку кишечника. Также рекомендуется за 24-48 часов до обследования соблюдать диету (не употреблять фрукты, овощи и грубую пищу). Часто процедуру проводят только натощак. Для предварительной очистки кишечника выполняются клизмы (вечером накануне и утром в день обследования) или микроклизмы со слабительным эффектом (за 30-40 мин. до процедуры). Также могут применяться слабительные медикаменты.
Этапы
При проведении манипуляции пациент занимает коленно-локтевую позу или ложится на левый бок. Тубус обильно смазывается вазелином и вводится в прямую кишку на глубину 4-5 см. Для расправления складок слизистой в ректороманоскоп нагнетается воздух. При грамотном и внимательном поведении врача удается сделать RRS абсолютно безболезненно и нетравматично для пациента.
Радиационный контроль в медицинских учреждениях
Радиационный контроль в медицинских учреждениях – это комплекс мероприятий, направленный на обеспечение безопасности персонала рентгенорадиологической службы медицинского учреждения, проводящего рентгенологические исследования, и пациентов, которые данные исследования проходят. Его целью является не превышение установленных пределов доз облучения при работе с источниками ионизирующего излучения, а также предотвращение возникновения стохастических и детерминированных эффектов после прохождения рентгенологических и радиологических процедур.
Радиационный контроль включает в себя:
— контроль мощности дозы излучения на рабочих местах персонала, в помещениях и на территории, смежных с процедурной рентгеновского кабинета;
— контроль технического состояния и защитной эффективности передвижных и индивидуальных средств радиационной защиты;
— индивидуальный дозиметрический контроль персонала групп А и Б;
— контроль дозовых нагрузок пациентов.
Контроль мощности дозы излучения на рабочих местах персонала, в помещениях и на территории, смежных с процедурной рентгеновского кабинета (дозиметрический контроль рентгеновского кабинета) проводится при технической паспортизации рентгеновского кабинета, получении санитарно-эпидемиологического заключения на работу с рентгеновским аппаратом.
Проведение дозиметрического контроля осуществляется аккредитованными в установленном порядке организациями (лабораторными центрами), имеющими необходимое дозиметрическое оборудование, а также лицензию на работу с источниками ионизирующего излучения. Оценка результатов дозиметрического контроля проводится в соответствии с СанПиН 2.6.1.1192-03 «Гигиенические требования к устройству и эксплуатации рентгеновских кабинетов, аппаратов и проведению рентгенологических исследований». Целью дозиметрического контроля является установление соответствия защитных свойств стационарных средств радиационной защиты (стены, перекрытия, защитные окна и двери) значениям, заложенным в проектной документации на размещение рентгеновского кабинета.
Контроль технического состояния и защитной эффективности передвижных и индивидуальных средств радиационной защиты (защитные ширмы, защитные фартуки, воротники, перчатки и др.) проводится не реже 1 раза в 2 года, также аккредитованными в установленном порядке организациями. Для проведения данного вида работ необходимо наличие эталонного рентгеновского аппарата. Целью данного контроля является определение соответствия защитных свойств средств защиты их заявленным (заводским) характеристикам.
Индивидуальный дозиметрический контроль персонала групп А (лица непосредственно проводящие исследования) и Б (лица находящиеся по условиям работы в сфере их воздействия) проводится постоянно с регистрацией результатов измерений 1 раз в квартал. Ответственной за проведение данного мероприятия является администрация учреждения, осуществляющего работу с источниками ионизирующего излучения. Регистрацию результатов также проводит аккредитованная организация, для чего на каждого сотрудника из персонала групп А и Б заводится карточка учета доз, куда заносятся результаты. Карточка заводится в 2-х экземплярах, один находится в лечебном учреждении, второй в лабораторном центре, проводящем данные исследования и должна хранится 50 лет. Целью индивидуального дозиметрического контроля персонала групп А и Б является контроль получаемых ими доз, а в случае превышения допустимых уровней – решение вопроса о необходимости перевода такого сотрудника на работу, не связанную с ионизирующим излучением.
Контроль дозовых нагрузок пациентов проводится при каждом рентгенологическом исследовании. Контроль проводится либо при помощи установленном на рентгеновском аппарате дозиметрическом оборудовании (например дозиметр ДРК-1) либо расчетным способом при помощи МУ 2.6.1.2944-11 «Контроль эффективных доз облучения пациентов при проведении медицинских рентгенологических исследований». Целью контроля является определение получаемой пациентом дозы облучения. При профилактических исследованиях (профосмотры) установленный норматив – 1 мЗв в год. Пределы доз облучения пациентов с диагностическими (в том числе по жизненным показаниям) и лечебными целями не устанавливаются. Полученная пациентом доза должна быть зарегистрирована в карте амбулаторного больного, истории болезни и выписке. Пациент имеет право отказаться от медицинских рентгенологических процедур, за исключением профилактических исследований, проводимых в целях выявления заболеваний, опасных в эпидемиологическим отношении. Не подлежат профилактическим рентгенологическим исследованиям дети до 14 лет и беременные, а также лица прошедшие профилактическое исследование в течение предшествующего года.
В чем разница между рентгенографией легких и флюорографией
Современные методы лучевой диагностики резко расширили границы визуализации внутренних структур тела. Сегодня в медицинской практике практически все анатомические зоны доступны для исследований. Как правило, лечащий врач определяет метод диагностики для постановки диагноза и при динамическом наблюдении пациента. Он также формирует план лечения и этапы сопровождения пациента на основании принципов надлежащей врачебной практики и доказательной медицины.
Однако не всегда вид медицинского исследования определяется только врачом, пациент сам вправе выбирать метод диагностики при профилактическом или диспансерном наблюдении. Примером самостоятельного принятия зачастую он основывает свои предпочтения исключительно на обилии «медицинской информации» в социальных ресурсах.
Сравним данные виды исследований
Рентгенография органов грудной клетки (рентгенография ОГК) – основной метод рентгенологического исследования, который проводится для диагностики патологии органов грудной клетки (легких, дыхательных путей, сердца, кровеносных сосудов, костей грудной клетки и позвоночника, пищевода). При данном исследовании изображение формируется в зависимости от поглощающей способности тканей, находящихся на пути прохождения рентгеновских лучей. Оно фиксируется на специальной рентгеновской пленке или на цифровом носителе информации.
Очевидным преимуществом метода является высокая разрешающая способность – рентгенографическое изображение определяет тени размером 1,5-2 мм. А в случае цифровых рентгенологических установок, еще и низкая лучевая нагрузка – эффективная эквивалентная доза (ЭЭД) облучения равна 0,1-0,2 мЗв. Метод цифрового рентгенологического исследования ОГК применяется как при массовых и скрининговых исследованиях, так и в качестве основного метода лучевой диагностики патологии органов грудной полости.
Флюорография – исключительно массовый (диспансерный) метод рентгенологического исследования заболеваний легких, в первую очередь рака и туберкулеза. При нем изображения теней фиксируется с рентгенографического экрана или оптического прибора на пленку маленького формата, которое в дальнейшем оценивается врачом рентгенологом с использованием средств увеличения изображения.
По сравнению с рентгенографией ОКГ разрешающая способность флюорографии позволяет определять тени размерами от 5 мм. Если выявляются негативные рентгенологические синдромы или подозрения на них, пациент направляется на дальнейшую диагностику, именно на выполнение рентгенографии ОГК. Пленочная флюорография получила широкое распространение лишь в массовых профилактических мероприятиях на территории советского и постсоветского пространства, прежде всего из экономической целесообразности, поскольку обладала низкой себестоимостью.
В корпусе клиники «Семейный доктор» на Бауманской рентген-диагностика выполняется с помощью полнофункционального рентген-аппарата последнего поколения ARCOMA Intuition (Швеция). Его использование позволяет добиться безошибочной диагностической точности получаемых изображений. Это первый в мире потолочный рентген-комплекс с полностью автоматическим позиционированием.
Лабораторная диагностика ревматических заболеваний
Общая информация
Краткое описание
Общероссийская общественная организация Ассоциация ревматологов России
Федеральные клинические рекомендации по лабораторной диагностике ревматических заболеваний
По современной классификации ревматические заболевания (РЗ) относятся к континууму иммуновоспалительных болезней человека, в патогенезе которых ключевую роль играют аутоиммунитет и аутовоспаление, связанные с генетически детерминированными и индуцированными факторами внешней среды (инфекции, курение и др.) дефектами активации приобретенного и врожденного иммунного ответа.
Лабораторная диагностика
ОБЩИЕ РЕКОМЕНДАЦИИ
1. Основная цель лабораторной диагностики РЗ – получение объективной информации о наличии и характере иммунопатологических изменений у обследуемого пациента, что является важным инструментом для ранней диагностики, оценки активности, тяжести течения, прогноза болезни и эффективности проводимой терапии (A)*.
2. Важной задачей стандартизации лабораторной диагностики РЗ является сопоставление и гармонизация иммунологических тестов с международными и национальными референтными материалами (аттестованными стандартными образцами) и методами исследований, базами данных о референтных пределах анализируемых биомаркеров, алгоритмами оценки полученных результатов (A).
3. Центральное место в лабораторной диагностике РЗ занимают серологические тесты, связанные с обнаружением циркулирующих аутоантител (A).
Комментарий. Положительные результаты определения аутоантител входят в число диагностических критериев системных РЗ; используются для оценки активности и прогноза этих заболеваний; играют важную роль в диагностике РЗ на ранней стадии; позволяют идентифицировать отдельные клинико-лабораторные субтипы РЗ; служат предикторами развития аутоиммунных РЗ у бессимптомных пациентов.
4. При аутоиммунных РЗ тестирование аутоантител проводится, в первую очередь, с целью подтверждения диагноза у пациентов с недостаточным числом клинических проявлений. Обнаружение аутоантител при отсутствии клинических признаков не является достаточным для постановки диагноза аутоиммунного заболевания (А). Комментарий. Отмечено нарастание частоты выявления аутоантител у лиц пожилого и старческого возраста, на фоне приема лекарственных препаратов, при вирусных и бактериальных инфекциях, злокачественных новообразованиях, у здоровых родственников больных аутоиммунными заболеваниями.
6. Аутоантитела, специфичные только для одного РЗ, встречаются очень редко. Аутоиммунные РЗ характеризуются одномоментным присутствием нескольких типов аутоантител в одной сыворотке, так называемым профилем аутоантител, оценка которого существенно увеличивает диагностическую ценность определения данных биомаркеров (B).
Комментарий. Разработаны стандартные профили аутоантител для диагностики системных РЗ (табл. 2).
Таблица 2. Стандартные профили аутоантител для диагностики системных РЗ
7. Неспецифические нарушения иммунитета (гипериммуноглобулинемия, снижение концентрации комплемента) могут косвенно указывать на развитие системного РЗ и служат показаниями для исследования аутоантител (С).
8. Основными диагностическими лабораторными маркерами РЗ являются антинуклеарные антитела (АНА), ревматоидный фактор (РФ), антитела к цитруллинированным белкам (АЦБ), антинейтрофильные цитоплазматические антитела (АНЦА), антифосфолипидные антитела (АФЛ) (А).
Комментарий. Разработан перечень первичных (скрининговых), вторичных (подтверждающих) и дополнительных серологических тестов для диагностики аутоиммунных РЗ (табл. 3). Cкрининговые тесты должны обладать высокой ДЧ, а подтверждающие тесты – высокой ДС.
9. Наиболее полезными маркерами острофазового ответа при РЗ являются СОЭ и С-реактивный белок (СРБ) (А).
Комментарий. По данным РПКИ, когортных и описательных исследований СОЭ и СРБ позволяют оценить воспалительную активность заболевания, характер прогрессирования и прогноз исходов хронического воспалительного процесса, а также эффективность противовоспалительной терапии.
Таблица 3. Алгоритм лабораторной диагностики аутоиммунных ревматических заболеваний
10. Другие лабораторные биомаркеры РЗ (цитокины, маркеры активации эндотелия, иммуноглобулины, иммунные комплексы, криоглобулины, компоненты системы комплемента, субпопуляции лимфоцитов, генетические маркеры, показатели метаболизма костной и хрящевой ткани, маркеры апоптоза и др.) имеют меньшее клиническое значение по сравнению с аутоантителами и показателями острой фазы воспаления (C).
Комментарий. Могут быть полезными для мониторирования активности заболевания и ответа на проводимое лечение (данные описательных исследований)
АУТОАНТИТЕЛА
Антинуклеарные антитела (АНА) – гетерогенная группа аутоантител, реагирующих с различными компонентами ядра.
1. «Золотым стандартом» и первичным скрининговым методом определения АНА в сыворотке крови является непрямая реакция иммунофлюоресценции (НРИФ) с использованием в качестве субстрата криостатных срезов мышиной или крысиной печени (почек), либо клеток линии HЕp-2 (эпителиальные клетки рака гортани человека).. При тестировании АНА методом НРИФ их традиционно обозначают как антинуклеарный фактор (АНФ). Оценка результатов НРИФ проводится с указанием максимального титра обнаружения АНФ в исследуемых сыворотках, а также интенсивности и типа иммунофлюоресценции. Характер свечения отражает присутствие различных типов АНА, в определенной степени специфичных для ряда аутоиммунных РЗ (табл. 4) (А).
Таблица 4. Характеристика АНФ
| Тип свечения | Тип аутоантител | Связь с заболеваниями |
| Гомогенное | Антитела к ДНК (двух и односпиральной), ДНП, гистонам (H1, H2A,H2B, H3, H4) | СКВ, лекарственная волчанка, любые аутоиммунные ревматические заболевания и неревматические болезни |
| Периферическое (краевое) | Антитела к двухспиральной, нативной ДНК (анДНК) | СКВ |
| Крапчатое | Антитела Sm, РНП, SS-A/Ro, SS-B/La, Jo-1 | СКВ, СЗСТ, синдром Шегрена, ПМ/ДМ |
| Сетчатое крапчатое | Антитела к Scl-70 | ССД (диффузная форма) |
| Дискретное крапчатое | Антицентромерные антитела (АЦА) | CREST синдром, синдром Рейно |
| Нуклеолярное | Антитела к РНК-полимеразе 1, PM/Scl, U3РНП | ССД (диффузная форма) |
4. Положительные результаты обнаружения IgM РФ в сыворотке крови служат диагностическим критерием РА (А). При использовании общепринятой ВГН (15-20 МЕ/мл) ДЧ составляет 50-90%, ДС: 80-93%, ОППР: 4,86, ОПОР: 0,38. IgM РФ – чувствительный, но недостаточно специфичный маркер для диагностики РА, так как обнаруживается в сыворотках при других РЗ, хронических инфекциях, злокачественных новообразованиях и в пожилом возрасте. Применение высоко позитивных уровней IgМ РФ (>3 ВГН, т.е. ≥40-50 МЕ/мл) сопровождается значительным увеличением его ДС (91-98%) и ОППР (22,7) при РА.
5. IgM РФ в высокой концентрации является полезным маркером для прогнозирования быстропрогрессирующего деструктивного поражения суставов (А) и системных проявлений при РА (С).
6. Тестирование IgM РФ позволяет прогнозировать эффективность терапии ГИБП у больных РА. Серопозитивность по IgM РФ и высокий уровень этого маркера в крови до начала лечения рассматривается в качестве предиктора хорошего ответа на терапию РТМ (A) при РА.
1. АЦБ обладают высокой ДС при РА (А/B/C). Среди АЦБ ведущую роль в клинической практике имеет определение АЦЦП, которые являются наиболее стандартизованным маркером для ранней диагностики и оценки прогноза РА (А/B/C)
2. Стандартными методами определения АЦЦП в сыворотке крови служат ИФА с использованием в качестве антигена синтетических циклических цитруллинированных пептидов второго и третьего поколения, имеющих высокую связывающую активность в отношении широкого спектра антител, ассоциирующихся с РА (АЦЦП2 и АЦЦП3), а также хемилюминисцентный анализ на основе микрочастиц и электрохемилюминисцентный анализ (А). В качестве скринингового теста может применяться полуколичественный иммунохроматографический экспресс-метод (С).
3. ВГН при определении АЦЦП в сыворотке крови составляет 5-25 ЕД /мл в зависимости от фирмы-изготовителя коммерческих наборов реагентов. Рекомендуется выделение негативных (≤ВГН); низко позитивных (≤3 ВГН) и высоко позитивных (>3 ВГН) уровней АЦЦП (А).
4. Положительные результаты обнаружения АЦЦП в сыворотке крови служат диагностическим критерием РА (А). АЦЦП – более высокоспецифичный диагностический маркер РА (ДЧ: 49-91%, ДС: 73-99%, ОППР: 12,46-17,3, ОПОР: 0,36-0,2), особенно, на ранней стадии болезни (ДЧ: 39-71%, ДС: 93-99%, ОППР: 6,04, ОПОР: 0,74) по сравнению с IgМ РФ (А). Определение АЦЦП имеет важное значение для диагностики серонегативного по IgМ РФ РА (частота обнаружения АЦЦП у IgМ РФ-отрицательных больных РА составляет 20-40%) (А), дифференциальной диагностики РА с другими РЗ (А/B/C).
5. Серопозитивность по АЦЦП является прогностическим маркером тяжелого эрозивного поражения суставов при РА (А/B/C). Прогностическая ценность АЦЦП в отношении развития выраженной суставной деструкции у больных РА значительно возрастает при совместном определении данного маркера c “shared epitope” (SE) HLA DRB1*0101, 0104, 0404 (А/B/C).
6. Обнаружение АЦЦП в сыворотке крови служит предиктором развития РА у здоровых лиц (ОР:15,9) и у пациентов с ранним недифференцированным артритом (ОР: 25-37,8) (А/B/C).
7. Тестирование АЦЦП позволяет прогнозировать эффективность терапии ГИБП у больных РА. Серопозитивность по АЦЦП и высокий уровень этого маркера в крови до начала лечения рассматривается в качестве предиктора хорошего ответа на терапию РТМ (A) при РА.
8. На поздней стадии РА исследование АЦЦП нецелесообразно. У серонегативных по АЦЦП пациентов рекомендуемая кратность определения АЦЦП на ранней стадии РА составляет 1 раз в 6 месяцев, на развернутой стадии – однократно. У АЦЦП-низко позитивных больных исследование АЦЦП на ранней стадии РА следует проводить 1 раз в 3-6 месяцев, на развернутой стадии – 1 раз в год. При высокой позитивности по АЦЦП на ранней и развернутой стадиях РА рекомендуется однократное исследование АЦЦП.
(D).
Комментарий. При оценке кратности определения АЦЦП учитывались данные систематического обзора и описательных исследований о большей стабильности АЦЦП по сравнению с IgM РФ (отсутствие выраженной корреляции с клинико-лабораторными показателями воспалительной активности заболевания, сероконверсии в течение заболевания и на фоне проводимой терапии, увеличения частоты обнаружения в пожилом возрасте) и необходимости выделения АЦБ-положительного фенотипа РА, характеризующегося ускоренной рентгенологической прогрессией деструктивного поражения суставов, тяжелым течением РА с повышением общей летальности и более частым развитием коморбидных состояний, с целью выбора соответствующего метода эффективной терапии.
9. Стандартным методом определения АМЦВ в сыворотке крови является ИФА (А). В качестве скринингового теста применяется полуколичественный иммунохроматографический экспресс-метод на сухих тест-полосках для измерения АМЦВ в цельной крови (C).
10. Верхняя граница нормы при определении АМЦВ с помощью ИФА составляет 20 ЕД /мл (А). Рекомендуется выделение негативных (≤ВГН); низко позитивных (≤3 ВГН) и высоко позитивных (>3 ВГН) уровней АМЦВ (А).
11. Положительные результаты определения АМЦВ в сыворотке крови служат дополнительным диагностическим маркером РА при отрицательных результатах определения IgM РФ и АЦЦП в сыворотке крови (C). АМЦВ обладают более высокой или сходной ДЧ, но меньшей ДС для диагностики РА (ДЧ: 77%, ДС: 89%, ОППР: 7,24, ОПОР: 0,28) по сравнению с АЦЦП (С).
12. АМЦВ являются полезным маркером для прогнозирования тяжелого эрозивного поражения суставов у больных РА (ОР: 7,3) (B).
13. Повышение уровня АМЦВ в большей степени ассоциируется с клинико-лабораторными показателями воспалительной активности РА, чем АЦЦП (B/С).
14. На поздней стадии РА исследование АМЦВ нецелесообразно. У серонегативных по АЦЦП пациентов рекомендуемая кратность определения АМЦВ на ранней стадии РА составляет 1 раз в 6 месяцев, на развернутой стадии – однократно. У низко/высоко позитивных больных по АМЦВ исследование АМЦВ на ранней стадии РА следует проводить 1 раз в 3-6 месяцев, на развернутой стадии – 1 раз в 6 месяцев – 1 год (D).
Комментарий. При оценке кратности определения АМЦВ учитывались данные систематического обзора, метаанализа и описательных исследований о большей связи АМЦВ с клинико-лабораторными показателями воспалительной активности заболевания по сравнению с АЦЦП, снижении уровня АМЦВ на фоне терапии ГИБП и необходимости выделения АЦБ-положительного фенотипа РА, характеризующегося ускоренной рентгенологической прогрессией деструктивного поражения суставов, тяжелым течением РА с повышением общей летальности и более частым развитием коморбидных состояний, с целью выбора соответствующего метода эффективной терапии.
Антифосфолипидные антитела (АФЛ) – гетерогенная популяция аутоантител, распознающих антигенные детерминанты анионных и нейтральных фосфолипидов, и комплексные эпитопы, образующиеся в процессе взаимодействия фосфолипидов и фосфолипидсвязывающих белков плазмы крови.
1. АФЛ являются серологическим маркером антифосфолипидного синдрома (АФС) и фактором риска развития тромботических осложнений и акушерской патологии при данном заболевании. В число лабораторных диагностических критериев АФС входят положительные результаты обнаружения антител к кардиолипину (АКЛ) классов IgG/IgM, антител к β2-гликопротеину I (аβ2-ГП I) классов IgG /IgM и волчаночного антикоагулянта (ВА) (А).
2. IgG/IgM АКЛ должны определяться в сыворотке в титрах, превышающих 40 GPL/MPL (или 99-ый процентиль у здоровых доноров), в 2 и более исследованиях с интервалом не менее 12 недель с помощью стандартного ИФА, позволяющего выявлять β2 – ГП I-зависимые АКЛ (А).
IgG/IgM аβ2-ГП I должны определяться в сыворотке с помощью стандартного ИФА в диагностических титрах, превышающих 99-ый процентиль у здоровых доноров, в 2 и более исследованиях с интервалом не менее 12 недель (А).
ВА должен определяться в плазме в 2 или более исследованиях с интервалом не менее 12 недель в фосфолипидзависимых коагуляционных тестах стандартным методом, включающим несколько этапов (А):
(а) Удлинение фосфолипидзависимого свертывания крови при использовании скрининговых коагуляционных тестов (АЧТВ, каолиновый тест, тест с ядом гадюки Рассела);
(б) Отсутствие нормализации времени свертывания по данным скрининговых тестов при смешивании с нормальной, лишенной тромбоцитов плазмой;
(в) Нормализация удлиненного времени свертывания крови при добавлении избытка фосфолипидов;
(г) Исключение других коагулопатий (наличия в крови ингибиторов фактора VIII или гепарина).
При отрицательных результатах определения ВА, IgG/IgM АКЛ, IgG/IgM аβ2-ГП I и подозрении на наличие АФС рекомендовано дополнительное исследование АКЛ и аβ2-ГП I класса IgA (С).
Диагноз АФС не может быть установлен, если промежуток между выявлением АФЛ и клиническими признаками заболевания составляет менее 12 недель и более 5 лет (А).
Для постановки диагноза АФС достаточно одного из трех лабораторных критериев (ВА, АКЛ или аβ2-ГП I), наличие у больного нескольких лабораторных критериев АФС сопровождается значительным увеличением риска тромботических осложнений (А).
3. Антитела к другим ФЛ и кофакторным белкам (фосфатидилсерину, фосфатидилинозитолу, фосфатидилэтаноламину, фосфатидилхолину, смеси ФЛ, протромбину, белкам C, S, Z и аннексину V) не имеют доказанного значения для диагностики АФС. В ряде случаев обнаружение этих АФЛ ассоциируется с «пре-АФС» (или «вероятным» АФС), который характеризуется наличием у больных сетчатого ливедо, хореи, тромбоцитопении, потерь плода, поражения клапанов сердца и может предшествовать развитию тромботических осложнений (С).
8. Рекомендуемая кратность определения ВА, IgG/IgM АКЛ, IgG/IgM аβ2-ГП I при АФС составляет 1 раз в 3-6 месяцев.
Антинейтрофильные цитоплазматические антитела (АНЦА) – гетерогенная популяция аутоантител, реагирующих с ферментами цитоплазмы нейтрофилов. Различают два основных типа АНЦА – цитоплазматические АНЦА (цАНЦА), взаимодействующие с протеиназой 3 (ПР3), и перинуклеарные АНЦА (пАНЦА), специфичные в отношении миелопероксидазы (МПО). В некоторых случаях выявляются атипичные АНЦА (аАНЦА), направленные к неизвестным цитоплазматическим белкам и ламинам А, В1, С.
4. Обнаружение цАНЦА методом НРИФ является высокоспецифичным диагностическим маркером ГВ (ДЧ: 63-91%, ДС: 95-99%) и менее полезно для диагностики МПА и синдрома Черджа – Строс (А). Положительные результаты определения пАНЦА методом НРИФ в сочетании с ИФА МПО-АНЦА служат полезным диагностическим маркером МПА (ДЧ: 50-75%, ДС: 80-98%), синдрома Черджа – Строс, а также быстропрогрессирующего гломерулонефрита и идиопатического альвеолярного геморрагического синдрома (А).
5. ДЧ АНЦА варьирует от 34% до 92% в зависимости от активности, формы, стадии заболевания, распространенности патологического процесса и проводимой терапии (А).
6. Отсутствие АНЦА при узелковом полиартериите позволяет дифференцировать данную форму васкулита от МПА (А).
7. Повышение уровня цАНЦА/ПР3-АНЦА является фактором риска развития обострений ГВ на фоне ремиссии болезни (В).
8. Рекомендуемая кратность определения цАНЦА/ПР3-АНЦА и пАНЦА/МПО-АНЦА составляет 1 раз в 3-6 месяцев.
ЛАБОРАТОРНЫЕ МАРКЕРЫ ВОСПАЛЕНИЯ
1. Рекомендуется международный метод определения СОЭ по Вестергрену как наиболее чувствительный при повышении СОЭ (А). Верхняя граница СОЭ в норме по Вестергрену зависит от возраста и пола, рассчитывается по формуле: для женщин СОЭ (мм/час)=(возраст в годах+10)/2; для мужчин СОЭ (мм/час) = (возраст в годах)/2 (А).
2. Увеличение СОЭ служит лабораторным классификационным критерием РА (А).
3. Повышение СОЭ>50 мм/час является классификационным критерием гигантоклеточного артериита (ДЧ: 95%) (B)
4. Повышение СОЭ>35 мм/час является диагностическим признаком ревматической полимиалгии (ДЧ: 95%) (С).
5. Определение СОЭ может быть полезным для оценки активности воспаления при гигантоклеточном артериите (C), ревматической полимиалгии (используется при подсчете индекса SDAI PMR) (C) и РА (используется при подсчете индекса DAS) (А).
6. Наиболее важными факторами несовпадения результатов определения СОЭ и СРБ у больных РА и др. системными РЗ служат инфекция, почечная недостаточноcть и низкий уровень альбумина в крови (С).
7.Рекомендуемая кратность определения СОЭ составляет 1 раз в 1-3 месяца (А).
C-реактивный белок (СРБ) – классический острофазовый белок плазмы крови, который рассматривается как наиболее чувствительный лабораторный маркер инфекции, воспаления и тканевого повреждения.
1. В зависимости от цели исследования определение концентрации СРБ проводится классическими и высокочувствительными методами. Классические методы количественного анализа СРБ в сыворотке крови, включая радиальную иммунодиффузию, иммунотурбидиметрию и иммунонефелометрию, предназначены для выявления повышенного уровня СРБ при остром воспалении и тканевом повреждении в пределах диапазона концентраций 5-500 мг/л (А).
Высокочувствительный анализ СРБ (вчСРБ), основанный на усилении аналитической чувствительности иммунохимических методов (иммуноферментного, иммунотурбидиметрического и иммунонефелометрического) в 10 и более раз с помощью специальных реагентов, позволяет измерять концентрации СРБ ниже 5 мг/л и используется для оценки базального уровня вчСРБ и связанного с ним кардиоваскулярного риска (А).
3. Определение СРБ классическими и высокочувствительными методами является полезным тестом для оценки активности патологического процесса у больных РЗ (в том числе, при подсчете индексов активности DAS 28-СРБ и SDAI) (А/B/C); мониторирования и контроля эффективности терапии интеркуррентных инфекций при СКВ, ССД, ДМ и др. РЗ с незначительным повышением или нормальным уровнем СРБ (С); дифференциальной диагностики ряда РЗ (СКВ и РА) (С).
4. СРБ служит лабораторным классификационным критерием РА (А).
5. Увеличение базальной концентрации СРБ является предиктором развития рентгенологических изменений, свидетельствующих о тяжелом деструктивном поражении суставов при раннем РА (С).
6. Определение базального уровня вчСРБ имеет важное значение для стратификации больных ревматическими заболеваниями по степени кардиоваскулярного риска. Базальная концентрация вчСРБ менее 1 мг/л соответствует низкому, 1-3 мг/л – среднему, более 3 мг/л – высокому кардиоваскулярному риску. Уровень вчСРБ от 3 до 10 мг/л ассоциируется с субклиническим «low grade» воспалением, а более 10 мг/л – с системным персистирующим «high grade» воспалением (В).
7. Рекомендуемая кратность определения СРБ составляет 1 раз в 1-3 месяца (А).
Информация
Источники и литература
Информация
Методология
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются систематические обзоры в последней доступной версии TheCochraneLibrary, базы данных Medline, PubMed (систематические обзоры (мета-анализы), рандомизированные клинические испытания, когортные исследования или исследования случай-контроль, статьи обзорного характера. Глубина поиска 10 лет.
Методы, использованные для оценки качества и силы доказательств
· Консенсус экспертов
· Оценка значимости в соответствии с рейтинговой схемой
Таблица 1. Уровни доказательности, принятые при разработке данных рекомендаций
| A | · высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью систематической ошибки, результаты которого могут быть распространены на соответствующую российскую популяцию. |
| B | · высококачественный (++) обзор или систематический обзор когортных исследований или исследований случай-контроль или · высококачественное (++) когортное исследование или исследование случай контроль с очень низким уровнем систематической ошибки или · РКИ с невысоким (+) риском систематической ошибки, результаты которого могут быть распространены на соответствующую российскую популяцию. |
| C | · когортное исследование или исследование случай контроль или контролируемое исследование без рандомизации с невысоким уровнем систематической ошибки (+), результаты которого могут быть распространены на соответствующую российскую популяцию или · РКИ с очень низким или невысоким (+) риском систематической ошибки, результаты которого не могут быть непосредственно распространены на соответствующую российскую популяцию. |
| D | · описание серии случаев или · неконтролируемое исследование или · мнение экспертов |
Индикаторы доброкачественной практики (GoodPracticePoints–GPPs)
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций
Экономический анализ
Экономический анализ не проводился и публикации по фармакоэкономике не анализировались
Метод валидизации рекомендаций:
· Внешняя экспертная оценка
· Внутренняя экспертная оценка




