Пищевой консервант Е262: натрия ацетаты для любимых рецептов
Большинство домашних хозяек хоть раз в жизни получали пищевую добавку E 262 в домашних условиях. Познаниями в химии для этого обладать не надо. Достаточно «погасить» соду уксусной кислотой.
Результатом реакции станет натрия ацетат. Безопасное для здоровья соединение зарекомендовало себя как регулятор кислотности и консервант.
Название продукта
Химическое вещество в международной кодификации пищевых добавок числится под индексом Е 262 (в других документах может встретиться написание Е–262).
ГОСТ 54626–2011 закрепил определение Натрия ацетаты (международный синоним Sodium Acetates).
Пищевые натрия ацетаты представлены двумя химическими видами:
Немецкие наименования: Natriumacetat, Natrium salz der Essigsaure.
Французские: Acetate de Sodium, Sel de Sodium de l’aside acetique.
Тип вещества
Пищевые ацетаты натрия относятся к группе искусственных консервантов. По химическому составу представляют собой натриевые соли уксусной кислоты. Производственным сырьем выступают:
Основной способ получения сухой перегонкой древесного сырья с натриевой солью угольной кислоты. Популярна технология соединения уксусной кислоты (или ее эфиров) с карбонатом, гидрокарбонатом или гидроксидом натрия.
Свойства
Ацетат натрия (Е 262i)
| Показатель | Стандартные значения |
| Цвет | бесцветный или белый |
| Состав | натриевая соль; химические формулы: С2Н3O2Na (безводный), С2Н3O2Na3H2O (тригидрат) |
| Внешний вид | гранулы, порошок, кристаллы |
| Запах | отсутствует или слабый уксусной кислоты |
| Растворимость | хорошо в воде, умерено в этаноле, эфире |
| Содержание основного вещества | 98,5% |
| Вкус | безвкусный |
| Плотность | 2,257 г/м 3 |
| Другие | гигроскопичен, не горюч, pH водного раствора 8–9,5 |
Диацетат натрия (Е 262ii)
| Показатель | Стандартные значения |
| Цвет | бесцветный или белый, допускаются желтые оттенки |
| Состав | натриевая соль; химическая формула С4Н7O4Na |
| Внешний вид | кристаллическая твердая масса |
| Запах | уксусной кислоты |
| Растворимость | хорошо в воде, умерено в этаноле, эфире |
| Содержание основного вещества | 58–60% |
| Вкус | безвкусный |
| Плотность | 2,257 г/м 3 |
| Другие | гигроскопичен, не горюч, pH водного раствора 4,5–5,0 |
Упаковка
Согласно ГОСТ 54626–2011, для упаковки пищевых ацетатов натрия могут применяться:
Обязательное требование — наличие дополнительного вкладыша из прочного полиэтилена, предназначенного для упаковки пищевых продуктов.
Разрешено упаковывать пищевой консервант в другую безопасную тару (бочки, канистры, контейнеры).
Кроме стандартной маркировки, должен стоять знак «Беречь от влаги».
Применение
Пищевые ацетаты натрия — одна из самых востребованных добавок при производстве продуктов питания. Причина кроется в отсутствии токсичных свойств и низкой стоимости.
Пищевой консервант E 262 допустимо применять без ограничения суточных норм потребления.
В качестве консерванта, ароматизатора, регулятора кислотности используют преимущественно диацетат натрия в следующих продуктах:
Кодекс Алиментариус разрешает добавку Е 262 в майонезах, бульонных кубиках, сублимированных супах быстрого приготовления.
На втором месте по потреблению пищевого консерванта стоят фармакология и медицина:
Добавка E 262 популярна в животноводстве как консервант для фуражного зерна и зеленых кормов. Ацетаты натрия добавляют для увеличения надоев и лучшего привеса рогатого скота. В птицеводстве для увеличения яйценоскости.
Другие сферы применения ацетатов натрия:
Ацетаты натрия играют важную роль в экологии. Вещество добавляют в сточные воды для нейтрализации токсичного действия отработанной серной кислоты.
Знакомый всем по школьным химическим опытам «горячий лед» — это не что иное, как сильно охлажденный раствор ацетата натрия в правильно подобранном соотношении компонентов.
Пищевая добавка E 262 разрешена к применению во всех странах.
Польза и вред
Ацетаты натрия имеют выраженные бактерицидные и дезинфицирующие свойства. Пищевой консервант Е 262 хорошо усваиваются организмом. Ацетат натрия признан абсолютно безопасным (4 класс по ГОСТ 12.1.007–76).
Диацетат натрия отнесен к умеренно опасным продуктам (3 класс). При длительном вдыхании паров или употреблении большого количества внутрь может:
С осторожностью следует употреблять продукты с кодом Е 260 людям, чувствительным к уксусу.
Детям и беременным женщинам стоит исключить из своего рациона пищевой краситель Е151!
Детские ланч-боксы очень красивые и разноцветные. Если вы часто устраиваете детские праздники в своем заведении, то этот вид посуды для вас просто необходим! Подробнее в этой статье.
Формальдегид не должен использоваться при производстве пищевых продуктов, так как это очень опасный консервант. Подробнее о нем вы можете прочитать здесь.
Основные производители

Большой объем продукции производит китайская компания Fooding, включающая 35 химических предприятий из нескольких регионов страны.
Высоким качеством отличается продукция немецкой компании W. Urlich GmbH, имеющей 70‑летнюю историю развития.
Утверждение, что при попадании в организм пищевая добавка Е 262 превращается в канцерогенные нитриты, не выдерживает критики.
Ацетаты натрия находятся внутри клеток растений и живых организмов. Являются естественными консервантами всех кисломолочных продуктов как прямой результат бактериальной ферментации. Если не употреблять соду ложками, не пить уксус литрами, пищевая добавка E 262 будет полезным и безопасным компонентом продуктов.
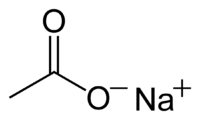
Ацетат натрия
| Ацетат натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат |
| Химическая формула | CH3COONa |
| Эмпирическая формула | C2H3O2Na |
| Физические свойства | |
| Состояние (ст. усл.) | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Термические свойства | |
| Температура разложения | 324 °C |
| Удельная теплота плавления | 264—289 к Дж/кг |
| Химические свойства | |
| Растворимость в воде | 76 г/100 мл |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, производится и широко применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
На этом свойстве основан довольно красивый опыт — «горячий лёд»
Способы получения
Ацетат натрия недорог и его легче приобрести в хим. магазинах, чем синтезировать в лабораторных условиях. В лабораторных условиях получается при взаимодействии уксусной кислоты, например, с карбонатом натрия, гидрокарбонатом натрия или гидроксидом натрия.
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 грамма гидрокарбоната натрия реагируют с 750 граммами 8 % винного уксуса (или же с 86 граммами 70 % уксусной эссенции) с образованием 82 грамм ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия или его концентрированный раствор.
Характерные реакции
Ацетат натрия может быть использован для образования эфира с алкил галогенидами такими как бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
Одновременно может проходить разложение до оксида натрия, ацетона и диоксида углерода:
Галерея
Химический обогреватель, содержащий перенасыщенный раствор ацетата натрия, выделяющего тепло при фазовом переходе в кристаллическую форму тригидрата ацетата натрия.
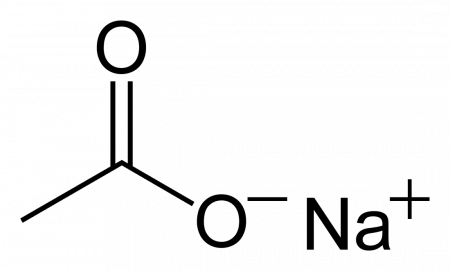
Ацетат натрия
| Ацетат натрия | |
|---|---|
 | |
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат натрий уксуснокислый |
| Хим. формула | C2H3O2Na |
| Рац. формула | CH3COONa |
| Состояние | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Температура | |
| • плавления | 328 °C |
| • разложения | 324 °C |
| Удельная теплота плавления | 264—289 кДж/кг |
| Растворимость | |
| • в воде | 76 г/100 мл |
| Рег. номер CAS | 127-09-3 |
| PubChem | 517045 |
| Рег. номер EINECS | 204-823-8 |
| SMILES | |
| Кодекс Алиментариус | E262 |
| ChEBI | 32954 |
| ChemSpider | 29105 |
| Токсичность | ирритант, малотоксичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
Также ацетат натрия является источником углерода для бактерий, выращиваемых на питательной среде.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
Ацетат натрия также используется в быту как составная химических грелок (англ. heating pad ) или химических обогревателей (англ. Hand warmer ), применяется как составная часть смеси «горячего льда» (англ. «hot ice» ), при кристаллизации ацетата натрия выделяется тепло — это экзотермический процесс. При нагреве тригидрата ацетата натрия (имеющего точку плавления в 58 °C) до 100 °C (обычно ёмкость с ним кладут в кипящую воду) он расплавляется (вернее, растворяется в собственной кристаллизационной воде) и переходит в водный раствор ацетата натрия. При охлаждении этого раствора образуется перенасыщенный раствор ацетата натрия в воде. Этот раствор прекрасно переохлаждается до комнатной температуры без образования твёрдой фазы, затем нажатием на металлический диск в ёмкости образуется центр кристаллизации, который, вырастая, заставляет перенасыщенный раствор переходить в твёрдую фазу тригидрата ацетата натрия. Этот процесс сопровождается значительным выделением тепла (экзотермическая реакция), теплота фазового перехода составляет 264-289 кДж/кг.
На этом свойстве основан довольно красивый химический опыт — «горячий лёд».
Способы получения
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 г гидрокарбоната натрия реагируют с 750 г 8%-го винного уксуса (или же с 86 г 70%-й уксусной эссенции) с образованием 82 г ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия. Для получения тригидрата ацетата натрия без выпаривания необходимо смешать 84 г гидрокарбоната натрия (пищевой соды) с 86 г 70%-ной уксусной кислоты и 10 г воды.
Характерные реакции
Ацетат натрия может быть использован для образования сложного эфира по реакции с алкилгалогенидами, такими как, например, бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
2CH3COONa → Na2CO3 + (CH3)2CO 
Влияние на организм
Ацетат натрия может всасываться в организм при проглатывании. Является ирритантом. LD50 25956 мг/кг. По другим данным из того же источника: LD50(крысы, орально): 3500 мг/кг, LD50(мыши, орально): 4960 мг/кг.
Натрий уксуснокислый — реактив, востребованный промышленностью в больших количествах
Натрий уксуснокислый (ацетат натрия, натрия этаноат) — органическое соединение, соль уксусной кислоты, традиционно называемая ацетатом. Формула CH3COONa или C2H3O2Na. 
Кристаллическое вещество с гигроскопичными кристаллами белого, светло-желтого, желтого, коричневого цвета; со слабым запахом уксуса. Водорастворимое, плохо растворяется в спиртах и эфирах.
Процесс кристаллизации экзотермический. При нагревании ацетат натрия разлагается с образованием ацетона и углекислого натрия. Считается малотоксичным, огне- и взрывобезопасен. Взаимодействует с кислотами. Реакция с серной кислотой приводит к образованию нерастворимого осадка — это свойство используется для нейтрализации серной кислоты. Образует сложные эфиры.
 |  |
| Натрий уксуснокислый (ацетат) б/в | Натрий уксуснокислый 3-вод. (ацетат) |
«Горячий лед», который используется в бытовых химических грелках, — это 3-водный ацетат натрия. Он плавится при температуре +58 °С. При помещении грелки в кипяток, вещество становится жидким, сохраняя это состояние и при комнатной температуре. Для начала процесса кристаллизации достаточно нажать на небольшой металлический диск внутри грелки. Он становится центром кристаллизации и запускает процесс. По мере кристаллизации реактива выделяется значительное количество тепла. Тепло выделяется до тех пор, пока все вещество внутри грелки не станет твердым (поэтому и называют — «горячий лед»). Чтобы вернуть грелку в исходное состояние, ее нужно опять прокипятить в воде, чтобы расплавить содержимое.




 Детям и беременным женщинам стоит исключить из своего рациона пищевой краситель Е151!
Детям и беременным женщинам стоит исключить из своего рациона пищевой краситель Е151!