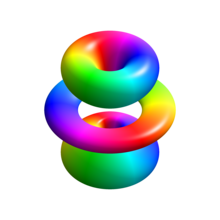Атомарный водород
При высокой температуре молекулы водорода диссоциируют на атомы:
Вследствие большой прочности и высокой энергии диссоциации (436 кДж/моль) распад молекул водорода на атомы происходит в заметной степени лишь при 2000 °C степень диссоциации 0,1%. Осуществить эту реакцию можно, например, раскаляя током вольфрамовую проволоку в атмосфере сильно разреженного водорода. Реакция обратима, и чем выше температура, тем сильнее равновесие сдвинуто вправо. Так, при 2500 °C степень диссоциации водорода 0,13%, при 3000 °C 9%, при 4000 °C 62,5%, а при 5000 °C 94,7% (при давлении 101325 Па).
Атомарный водород можно получить не только термической диссоциацией молекулярного водорода или при химических реакциях, но также и действием тихого (тлеющего) электрического разряда или ультрафиолетового излучения на молекулярный водород, находящийся под давлением около 70 Па.
Атомарный водород существует около 1 секунды. Сравнительная устойчивость атомарного водорода обусловлена тем, что двойные столкновения атомов водорода не приводят к образованию молекул водорода, т.к. возникают неустойчивые частицы, имеющие избыточную энергию. Эти частицы мгновенно распадаются вновь с образованием атомов водорода. Для образования молекул водорода необходимо столкновение трех атомов водорода (или столкновение со стенкой сосуда, примесями), чтобы выделяющаяся при образовании водорода энергия была сообщена в виде кинетической энергии третьему атому или молекуле (т.н. тройное соударение), который уходит из сферы реакции. Поэтому атомы водорода обычно претерпевают миллионы столкновений прежде, чем образуют устойчивую молекулу. Практически промежуток времени, в течение которого половинное число атомов соединиться в молекулы составляет, примерно, 1/3 сек.
При разложении водорода на атомы поглощается большое количество теплоты:
H2(г) = 2H(г) ΔH = 436 кДж/моль
Отсюда понятно, что атомы водорода должны быть гораздо активнее его молекул. Чтобы молекулярный водород вступил в какую-либо реакцию, молекулы должный распасться на атомы, для чего необходимо затратить большое количество энергии. При реакциях же атомарного водорода такой затраты энергии не требуется. См. химические свойства водорода.
Атом водорода
Из Википедии — свободной энциклопедии
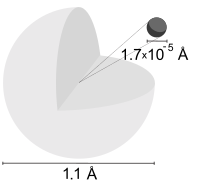
А́том водоро́да — физико-химическая система, состоящая из атомного ядра, несущего элементарный положительный электрический заряд, и электрона, несущего элементарный отрицательный электрический заряд. В состав атомного ядра как правило входит протон или протон с одним или несколькими нейтронами, образуя изотопы водорода. Электрон преимущественно находится в тонком концентрическом шаровом слое вокруг атомного ядра, образуя электронную оболочку атома. Наиболее вероятный радиус электронной оболочки атома водорода в стабильном состоянии равен боровскому радиусу a 0 = 0,529 <\displaystyle a_<0>=0<,>529> 
Атом водорода имеет специальное значение в квантовой механике и релятивистской квантовой механике, поскольку для него проблема двух тел имеет точное или приближенное аналитическое решение. Эти решения применимы для разных изотопов водорода, с соответствующей коррекцией.
В квантовой механике атом водорода описывается двухчастичной матрицей плотности или двухчастичной волновой функцией. Также упрощённо рассматривается как электрон в электростатическом поле бесконечно тяжёлого атомного ядра, не участвующего в движении (или просто в кулоновском электростатическом потенциале вида 1/ r ). В этом случае атом водорода описывается редуцированной одночастичной матрицей плотности или волновой функцией.
В 1913 году Нильс Бор предложил модель атома водорода, имеющую множество предположений и упрощений, и вывел из неё спектр излучения водорода. Предположения модели не были полностью правильны, но тем не менее приводили к верным значениям энергетических уровней атома.
Результаты расчётов Бора были подтверждены в 1925—1926 годах строгим квантово-механическим анализом, основанном на уравнении Шрёдингера. Решение уравнения Шрёдингера для электрона в электростатическом поле атомного ядра выводится в аналитической форме. Оно описывает не только уровни энергии электрона и спектр излучения, но и форму атомных орбиталей.
 | |
| Общий | |
|---|---|
| Условное обозначение | 1 ч |
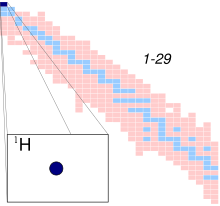
| Имена | атом водорода, H-1, протий, ¹H |
| Протоны | 1 |
| Нейтронов | 0 |
| Данные о нуклидах | |
| Природное изобилие | 99,985% |
| Изотопная масса | 1.007825 ед. |
| Вращаться | 1 / 2 |
| Избыточная энергия | 7288,969 ± 0,001 кэВ |
| Связующая энергия | 0,000 ± 0,0000 кэВ |
| Изотопы водорода Полная таблица нуклидов | |
СОДЕРЖАНИЕ
Изотопы
Тритий содержит два нейтрона и один протон в своем ядре и не является стабильным, распадаясь с периодом полураспада 12,32 года. Из-за своего короткого периода полураспада тритий не существует в природе, кроме как в следовых количествах.
Приведенные ниже формулы действительны для всех трех изотопов водорода, но для каждого изотопа водорода должны использоваться немного разные значения постоянной Ридберга (корректирующая формула, приведенная ниже).
Ион водорода
Одинокие нейтральные атомы водорода в нормальных условиях встречаются редко. Однако нейтральный водород является обычным явлением, когда он ковалентно связан с другим атомом, и атомы водорода также могут существовать в катионных и анионных формах.
Теоретический анализ
Неудачное классическое описание
Модель Бора – Зоммерфельда
В 1913 году Нильс Бор получил уровни энергии и спектральные частоты атома водорода, сделав ряд простых предположений, чтобы исправить неудавшуюся классическую модель. Предположения включали:
Бор предположил, что угловой момент электрона квантован с возможными значениями:
Точное значение постоянной Ридберга предполагает, что ядро бесконечно массивно по отношению к электрону. Для водорода-1, водорода-2 ( дейтерия ) и водорода-3 ( трития ), которые имеют конечную массу, константа должна быть немного изменена, чтобы использовать приведенную массу системы, а не просто массу электрона. Это включает в себя кинетическую энергию ядра в задаче, потому что полная (электронная плюс ядерная) кинетическая энергия эквивалентна кинетической энергии приведенной массы, движущейся со скоростью, равной скорости электрона относительно ядра. Однако, поскольку ядро намного тяжелее электрона, масса электрона и приведенная масса почти одинаковы. Постоянная Ридберга R M для атома водорода (один электрон), R определяется выражением
С моделью Бора все еще были проблемы:
Уравнение Шредингера
Уравнение Шредингера позволяет вычислять стационарные состояния, а также временную эволюцию квантовых систем. Для нерелятивистского атома водорода доступны точные аналитические ответы. Прежде чем мы перейдем к представлению формального отчета, мы дадим элементарный обзор.
и есть три состояния: 2 п <\ Displaystyle 2 \ mathrm
>
e ^ <\ pm i \ varphi>.>
Электрон в состоянии или, скорее всего, находится на второй боровской орбите с энергией, определяемой формулой Бора. 2 s <\ Displaystyle 2 \ mathrm > 
>
Волновая функция
Разложив лапласиан по сферическим координатам:
Квантовые числа могут принимать следующие значения:
Кроме того, эти волновые функции нормированы (т. Е. Интеграл от их квадрата модуля равен 1) и ортогональны :
Волновые функции в импульсном пространстве связаны с волновыми функциями в позиционном пространстве через преобразование Фурье.
что для связанных состояний приводит к
Поскольку уравнение Шредингера справедливо только для нерелятивистской квантовой механики, решения, которые оно дает для атома водорода, не совсем верны. Уравнение Дирака релятивистской квантовой теории улучшает эти решения (см. Ниже).
Результаты уравнения Шредингера
Математическая сводка собственных состояний атома водорода
Уровни энергии
Когерентные состояния
В когерентных состояниях были предложены в качестве
который удовлетворяет и принимает вид d Ω ¯ ≡ грех θ ¯ d θ ¯ d φ ¯ d ψ ¯ / 8 π 2 <\ displaystyle d <\ bar <\ Omega>> \ Equiv \ sin <\ bar <\ theta>> \, d <\ bar <\ theta>> \, d <\ bar <\ varphi>> \, d < \ bar <\ psi>> / 8 \ pi ^ <2>>
Визуализация водородных электронных орбиталей
« Основное состояние », то есть состояние самой низкой энергии, в котором электрон обычно находится, является первым, 1 сек состояние ( главного квантового уровня п = 1, ℓ = 0).
В квантовых числах определяют расположение этих узлов. Есть:
Особенности, выходящие за рамки решения Шредингера
Есть несколько важных эффектов, которые не учитываются уравнением Шредингера и которые ответственны за некоторые небольшие, но измеримые отклонения реальных спектральных линий от предсказанных:
Обе эти особенности (и многие другие) включены в релятивистское уравнение Дирака с предсказаниями, которые еще ближе подходят к эксперименту. Опять же, уравнение Дирака может быть решено аналитически в частном случае системы двух тел, такой как атом водорода. Квантовые состояния результирующего решения теперь должны быть классифицированы по полному угловому моменту j (возникающему из-за связи между спином электрона и орбитальным угловым моментом ). Состояния одного и того же j и того же n по-прежнему вырождены. Таким образом, прямое аналитическое решение уравнения Дирака предсказывает 2S ( 1 / 2 ) и 2P ( 1 / 2 ) уровни водорода должны иметь одинаковую энергию, что противоречит наблюдениям ( эксперимент Лэмба – Ретерфорда ).
Для этих разработок было важно, чтобы решение уравнения Дирака для атома водорода могло быть получено точно, так что любое экспериментально наблюдаемое отклонение должно было восприниматься серьезно как сигнал несостоятельности теории.
Альтернативы теории Шредингера
Возбужденные атомы: 6. Водородная линия 21 см
Основное состояние атома водорода расщепляется на два очень близких энергетических уровня, которые отличаются лишь взаимной ориентацией спина ядра и электрона. При переходе с верхнего состояния на нижнее излучается фотон с длиной волны 21 см
Наконец, существуют настолько долгоживущие атомные состояния, что их время жизни даже не удается измерить экспериментально. Формально, атом в таком состоянии нестабилен и, будучи предоставлен самому себе, он рано или поздно излучил бы фотон. Но только ждать этого пришлось бы очень долго, да и затруднительно в лабораторных условиях настолько идеально изолировать атом от внешних воздействий.
Однако это вовсе не значит, что излучение, испущенное таким долгоживущим состоянием, вообще не удается наблюдать! В таких ситуациях иногда на помощь человеку приходит Вселенная. В глубоком космосе существуют условия, в которых огромные облака газа в возбужденном состоянии могут начать светиться: то излучение, которого мы не смогли дождаться в лабораторном эксперименте, мы видим в космосе.
Один пример такой ситуации — это знаменитая радиолиния водорода. Это излучение в радиодиапазоне с длиной волны примерно 21 см, которое идет из глубин космоса, от гигантских облаков холодного нейтрального атомарного водорода. Это линия излучения между двумя очень близкими уровнями энергии атома водорода, которые во всём похожи друг на друга и отличаются лишь тем, как спин электрона и протона ориентированы друг относительно друга. Одна ориентация обладает чуть-чуть большей энергией, чем другая, и из-за этого «основное» состояние электрона расщепляется на два: «по-настоящему основное» и чуть-чуть возбужденное. В атомной физике это явление называется забавным термином сверхтонкое расщепление. Радиолиния водорода — это излучение, которое испускает атом, возвращаясь из возбужденного состояния в «по-настоящему основное».
Когда физики теоретически рассчитали этот переход, они смогли оценить время жизни этого возбужденного состояния — примерно 11 млн лет. Обнаружить его в лабораторных условиях нереально — по крайней мере, если речь идет о самопроизвольном излучении (а вот вынужденное излучение водорода на длине волны 21 см, наоборот, изучено вдоль и поперек; на нем основан водородный мазер, микроволновой аналог лазера). Зато в глубоком космосе существуют настолько протяженные облака нейтрального водорода, что радиоизлучение от всего облака целиком видно отлично. Наблюдения галактик в радиолинии водорода — это один из главных инструментов исследования в радиоастрономии. С его помощью зачастую можно увидеть такие особенности строения галактик, которые незаметны другими методами.
Строение и свойства атома водорода
Конспект лекции с демонстрациями
Аннотация: традиционное изложение темы, дополненное двумя демонстрациями на компьютерных моделях и доказательством актуальности изучения водородоподобных систем в настоящее время.
Надежные сведения о свойствах атомов получены при спектральном анализе излучения, испускаемого атомами при возбуждении. Еще в XIX-ом веке Бальмер показал, что длины волн четырех линий излучения водорода, лежащих в видимой части, могут быть очень точно представлены эмпирической формулой

где вместо n следует подставлять целые числа 3, 4, 5 и 6, а B – эмпирическая константа. Закономерность, выражаемая формулой Бальмера, становится особенно наглядной, если записать ее для частот линий

Классическая физика не давала объяснения существованию линейчатых спектров. Трудности только возросли после опытов Э.Резерфорда, показавших, что в атоме есть массивное положительно заряженное ядро. Электроны, движущиеся с ускорением как планеты вокруг Солнца, должны излучать непрерывный спектр и терять энергию. Следовательно, атом должен быстро прекратить свое существование. Глубокий смысл этой формулы и подобных ей для серий Лаймана, Пашена. открылся после формулировки Н.Бором квантовых постулатов (1913 г.). В то время ему пришлось действовать логически противоречивым методом: сначала задача о движении электрона в атоме решалась при помощи классической механики, а затем из непрерывного множества состояний отбирались на основании специального постулата избранные, квантовые состояния. Успех модели произвел потрясающее впечатление на современников.
Теперь теория Н.Бора утратила свое значение. Но в свое время она была революционной: до 1913 г. представление о стационарных состояниях атома отсутствовало, после 1913 г. оно вошло в жизнь.
В 1922 г. Нильсу Бору была присуждена Нобелевская премия :
N IELS B OHR for his services in the investigation of the structure of atoms and of the radiation emanating from them.
(за заслуги в исследовании строения атомов и испускаемого ими излучения)
Вы можете посмотреть текст лекции, с которой при вручении премии выступил Н.Бор «The structure of the atom»( файл pdf 333 кб).

Мы имеем задачу о движении двух тел. Из курса механики известно, что такие задачи сводятся к задаче о движении тела с приведенной массой
Этот пример приведен исключительно для иллюстрации пользы оценочных расчетов. Грубые физически оправданные оценки дают правильный порядок величин.
Точное решение задачи о движении электрона:
Выпишем уравнение Шредингера

Поскольку нас интересует связанное состояние электрона, в этом уравнении E 0 соответствуют задаче о рассеянии электрона ядром). Подставим выражение для потенциальной энергии (1):

Т.к. потенциальная энергия зависит только от расстояния до центра взаимодействия, удобно решать задачу в сферической системе координат <r, θ, φ>. Волновую функцию в этом случае можно представить в виде произведения Ψ(r, θ, φ) = R(r)·Y(θ, φ). Функция R(r) зависит только от радиуса и является решением для сферически симметричных состояний атома, для которых угловая часть Y(θ, φ) = const. В приложении показано, как найти решение для сферически симметричных состояний (функцию R(r)). Там показано: чтобы полученное решение удовлетворяло требованиям, предъявляемым к волновым функциям, необходимо принять дискретность значений энергии

где n = 1, 2, 3. – так называемое главное квантовое число, определяющее энергию атома.
Основное состояние водородоподобного атома
Самая простая волновая функция атома водорода имеет вид ( n = 1, l = 0, m = 0, состояние 1s ):

Здесь введена постоянная ρ, равная


Элемент объема dV – это шаровой слой радиуса r и толщиной dr, величина его быстро растет с увеличением r (значения |Ψ| 2 при бóльших r имеют бóльший вес).
Рассчитаем еще среднее значение потенциальной энергии в 1s состоянии

Оно равно точно удвоенному значению полной энергии. Следовательно, среднее значение кинетической энергии равно модулю полной энергии

Возбужденные состояния водородоподобного атома
Энергии, которые может иметь атом водорода, отображены на схеме. Энергия E зависит только от главного квантового числа n. При данном n возможно
Наиболее простой вид имеет волновая функция возбужденного состояния 2s

Значение квантового числа l определяет величину момента количества движения (момента импульса) M

Сравним размеры атома в различных состояниях. С помощью волновых функций электрона можно подсчитать средний радиус атома в каждом состоянии

Наглядное представление волновых функций, описывающих движение электрона в возбужденных состояниях атома водорода, дает интересный апплет (разработка davidson.edu, адаптировано автором, не требует Java).
Излучение водородоподобного атома
Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое. Возможные переходы показаны на схеме уровней.


Как это не странно, интерес к водородоподобным атомам до сих пор сохраняется. Высоковозбужденные атомы, когда n >> 1, называют ридберговскими. Для атомов всех элементов высоковозбужденные состояния водородоподобны. Причина в том, что при n >> 1 внешний электрон почти все время удален от иона на очень большие расстояния. Тем самым он движется в поле положительно заряженного атомного остатка (как в водородном атоме вокруг ядра). Отклонения от этой модели заметны только на близких расстояниях от центра. Энергии ридберговского атома весьма точно описываются формулой

Если возникли какие-либо вопросы, напишите мне.